2,2 раза больше измеренного в тех же условиях объема водорода необходимого для гидрирования того же количества смеси. Найти количество молекул бензола и орто-ксилола
Дано:
V(CO2)/V(H2) = 2,2
Найти:
n-?
Решение:
2C6H6 + 15O2->12CO2 + 6H2O
2C8H10 + 21O2->16CO2 + 10H2O
Пусть количество смеси углеводородов равно 1 моль
n(C6H6)= х моль
n(C6H10)= 1-x моль
Гидрирование;
1. C6H5 + 3H2-> C6H12
2. C8H10 + 3H2-> C8H16
1. n(CO2)=6x
2. n(CO2)=8(1-x)
n(CO2)= 6x+8-8x= 8-2x
1. n(H2)=3x
2. n(H2)= 3(1-x)
n(H2)= 3x+3-3x=3
V(CO2)/V(H2)= nCO2*Vm/nH2*Vm = nCO2/nH2= 8-2x/3
8-2x/3 = 2,2
X= 0,7
n(C6H6)=0,7
n(C6H10)=1-0,7=0,3
Ответ: n(C6H6)=0,7; n(C6H10)=0,3













 Металлы в природе. Общие способы их получения
Металлы в природе. Общие способы их получения Классификация органических соединений
Классификация органических соединений Степень окисления в соединениях
Степень окисления в соединениях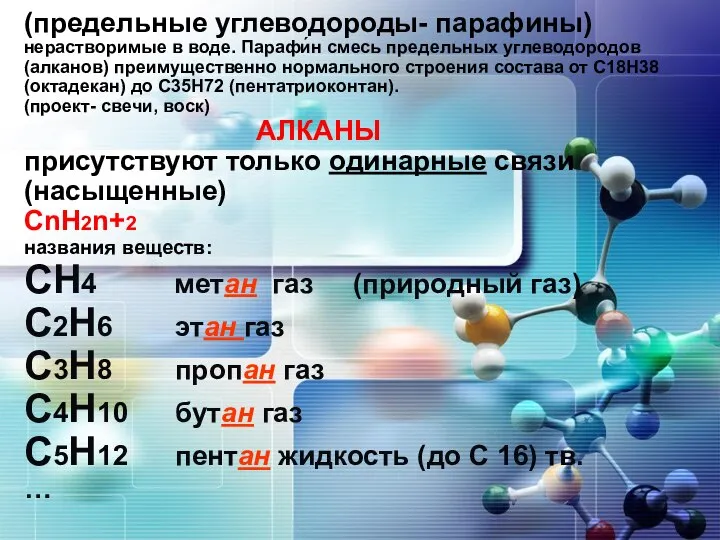 Углеводороды
Углеводороды Periodická soustava prvků
Periodická soustava prvků Выход продуктов пиролиза бензина
Выход продуктов пиролиза бензина Исследование концентрированных заквасок для сметаны
Исследование концентрированных заквасок для сметаны Осмотическое давление
Осмотическое давление Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Составление формул оксидов, оснований, солей
Составление формул оксидов, оснований, солей Алкены. Этилен C2H4
Алкены. Этилен C2H4 Метил-трет-бутиловый эфир
Метил-трет-бутиловый эфир Элемент магний
Элемент магний Ovr-1
Ovr-1 Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы 10_Valentnost_khimicheskikh_elementov
10_Valentnost_khimicheskikh_elementov Применение центрифугирования
Применение центрифугирования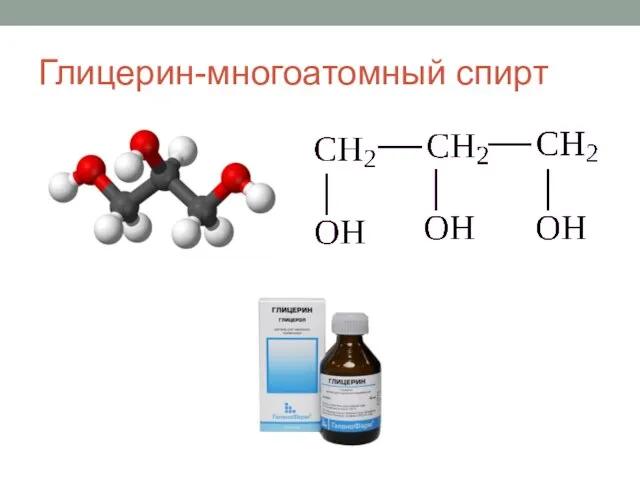 Жиры. Классификация жиров
Жиры. Классификация жиров Презентация на тему Металлы в периодической системе
Презентация на тему Металлы в периодической системе  Валентность
Валентность Строение веществ
Строение веществ Углеводороды. 9 класс
Углеводороды. 9 класс Ароматические углеводороды
Ароматические углеводороды Химическая связь. Лекция №3
Химическая связь. Лекция №3 Метод молекулярных орбиталей для координационных соединений
Метод молекулярных орбиталей для координационных соединений 10-2 основные положения теории Бутлерова
10-2 основные положения теории Бутлерова Общая характеристика элементов А-группы
Общая характеристика элементов А-группы Путешествие по городу химиков
Путешествие по городу химиков