Содержание
- 2. Я, Кузьмина Ирина Викторовна, кандидат технических наук с большим опытом преподавания в высшей школе, обобщила полезную
- 3. Вернуться к содержанию Для выхода из программы нажмите «Esc» на клавиатуре Переход к тому действию, о
- 4. Содержание Практическая работа № 5 «Влияние температуры на скорость реакции». Практическая работа № 6 «Реакции обмена».
- 5. Практическая работа № 5 «Влияние температуры на скорость реакции»
- 6. Цель – Познакомиться с влиянием температуры на скорость реакции. Приборы и реактивы: химическая посуда, H2SO4, Zn,
- 7. Опыт 1. В два сосуда Ландольта опускаем по 3 гранулы цинка и добавляем раствор серной кислоты.
- 8. Прибор позволяет выявить влияние на скорость химической реакции следующих факторов: природы реагирующих веществ; концентрации; площади соприкосновения
- 9. Принцип работы прибора состоит во взаимодействии твердой фазы (гранул цинка) и жидкой (раствора кислоты) в сосудах
- 10. Прибор состоит из двух сосудов Ландольта (1), связанных с поворотным устройством (2), двух силиконовых трубок (3)
- 11. Опыт 2. В три стакана наливаем раствор серной кислоты, в 3 другие – раствор тиосульфата натрия.
- 12. H2SO4 + Na2S2O3 → Na2SO4 + H2SO3S +6 –2 +4 0 H2SO3S → H2SO3 + S↓
- 13. Практическая работа № 6 «Реакции обмена»
- 14. Цель – Познакомиться с условиями протекания обменных реакций. Приборы и реактивы: химическая посуда, NaOH, KOH, H2SO4,
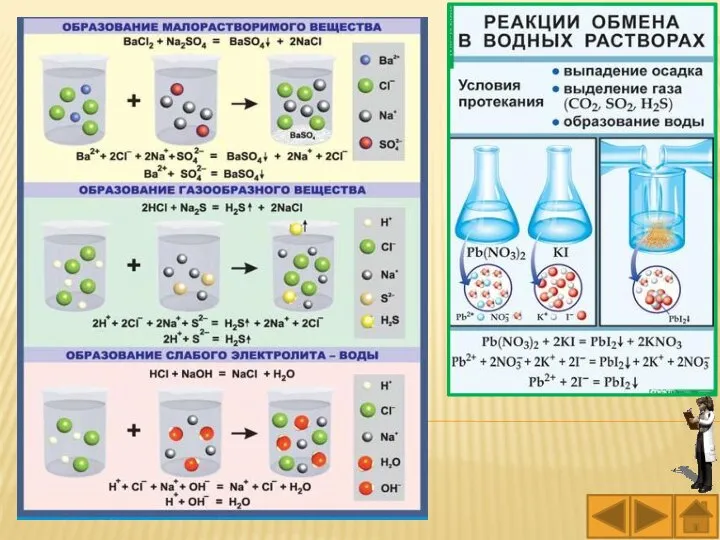
- 15. Обменные реакции в растворах электролитов протекают в направлении связывания ионов, в направлении образования более слабых электролитов,
- 18. Задание. Определите между какими парами веществ, приведенных в таблице, возможно химическое взаимодействие и почему? Напишите молекулярное,
- 19. Опыт 1. В пробирку внесите несколько капель раствора сульфата меди (II), а затем добавьте несколько капель
- 20. Аналогично оформите остальные опыты.
- 21. Гидролиз
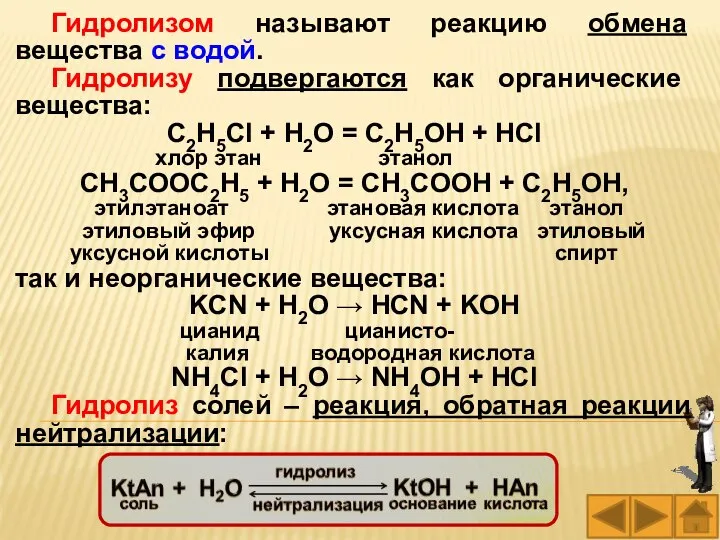
- 22. Гидролизом называют реакцию обмена вещества с водой. Гидролизу подвергаются как органические вещества: C2H5Cl + H2O =
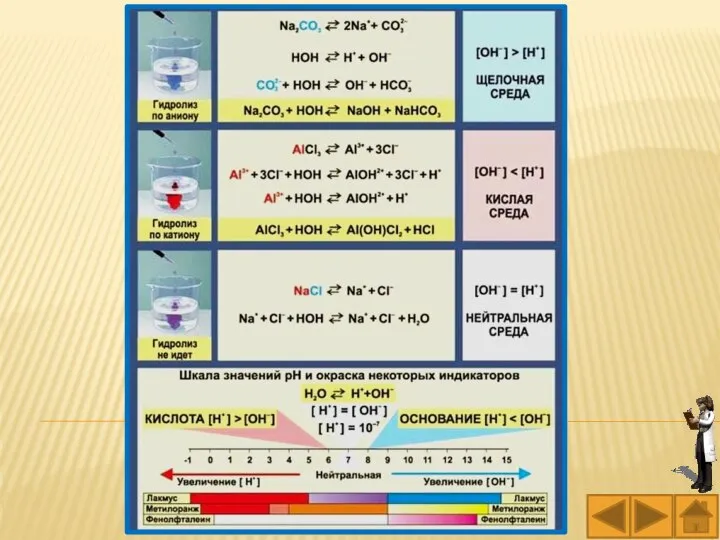
- 23. Гидролизу не подвергаются соли, образованные катионом сильного основания (Li+, Na+, K+, Rb+, Cs+, Ba2+, Sr2+, Ca2+
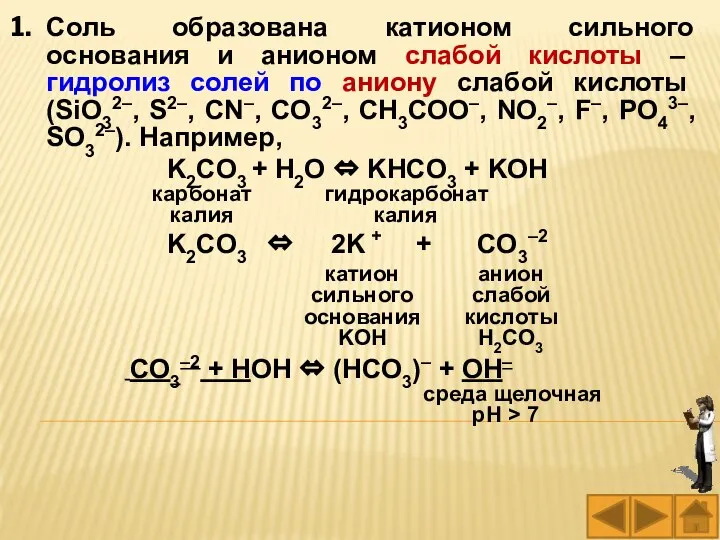
- 24. Соль образована катионом сильного основания и анионом слабой кислоты – гидролиз солей по аниону слабой кислоты
- 25. Гидролиз солей, образованных анионом слабой кислоты, усиливается (то есть равновесие смещается вправо) при: а) нагревании, так
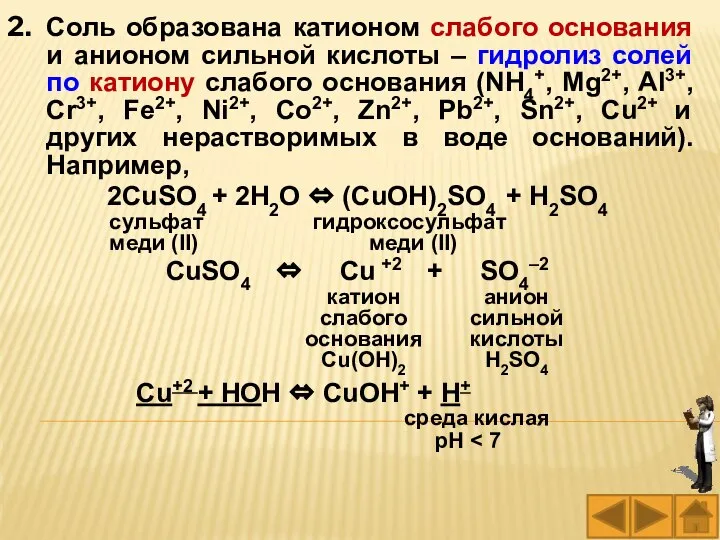
- 26. Соль образована катионом слабого основания и анионом сильной кислоты – гидролиз солей по катиону слабого основания
- 27. В растворе солей, гидролизующихся по катиону, среда кислая, pH Гидролиз таких солей усиливается при а) нагревании,
- 28. Соль образована катионом слабого основания и анионом слабой кислоты – гидролиз солей по катиону слабого основания
- 29. В растворе таких солей pH определяется силой образующихся кислоты и основания. В растворе ацетата аммония среда
- 30. Степень и константа гидролиза Степень гидролиза (h) – доля вещества, подвергшаяся гидролизу (отношение числа молекул, подвергшихся
- 31. Степень гидролиза зависит от: константы диссоциации образующегося слабого электролита (чем слабее образующиеся кислота и/или основание, тем
- 32. Константа гидролиза – константа равновесия обратимого процесса гидролиза: KF + H2O ⇔ HF + KOH F
- 33. HF – слабая кислота, диссоциирует обратимо: HF ⇔ H+ + F –. Подставляя эту величину в
- 34. Константа гидролиза зависит от природы соли и от температуры, но не зависит от концентрации соли. Для
- 35. Для солей, гидролизующихся и по катиону, и по аниону Чем слабее образующиеся кислота и/или основание, то
- 39. Практическая работа № 7 «Гидролиз солей»
- 40. Цель – Познакомиться с условиями протекания реакций гидролиза. Приборы и реактивы: химическая посуда, AlCl3, Na2CO3, KI,
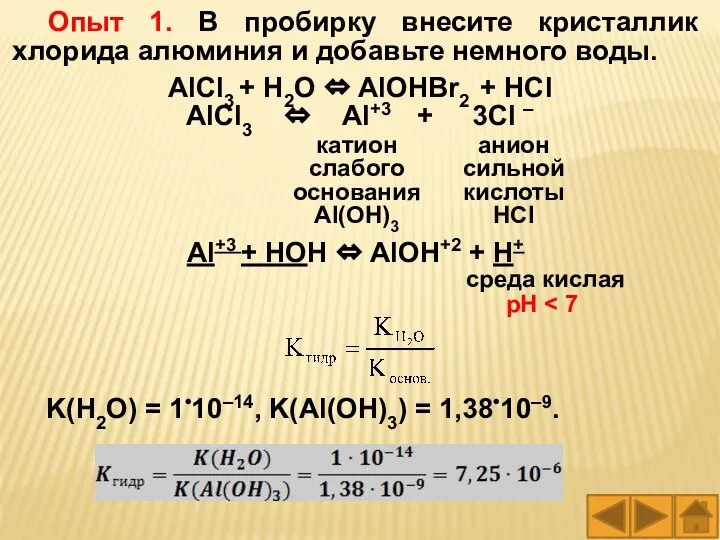
- 41. Опыт 1. В пробирку внесите кристаллик хлорида алюминия и добавьте немного воды. АlCl3 + H2O ⇔
- 42. Наблюдаемый эффект: с помощью универсаль-ного индикатора установили , что рН = 3. Константа гидролиза: Kгидр.(АlCl3) =
- 43. Практическая работа № 8 «Химическое равновесие в гомогенных системах»
- 44. Цель – Познакомиться с условиями смещения химического равновесия в гомогенных системах. Приборы и реактивы: химическая посуда,
- 45. Опыт 1. Влияние концентрации реагирующих веществ на химическое равновесие Для изучения влияния концентрации реагирующих веществ на
- 46. FeCl3 + 3NH4CNS ⇔ Fe(CNS)3 + 3NH4Cl. Из веществ этой системы Fe(CNS)3 интенсивно окрашен в красный
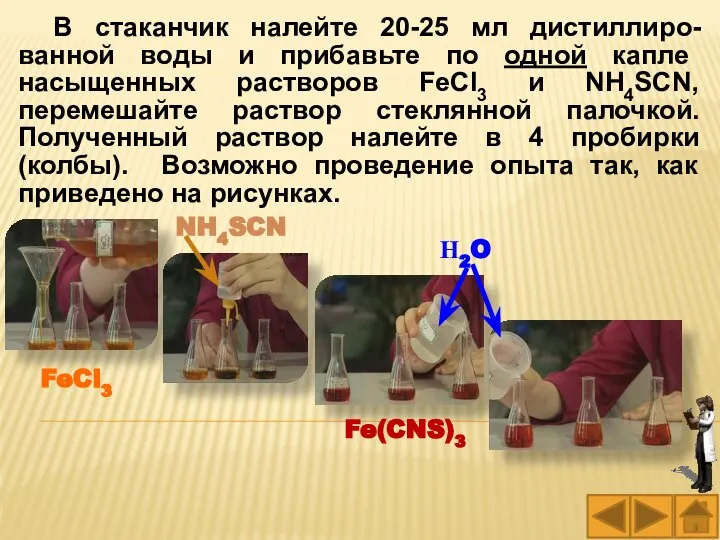
- 47. В стаканчик налейте 20-25 мл дистиллиро-ванной воды и прибавьте по одной капле насыщенных растворов FeCl3 и
- 48. Добавьте: в первую пробирку (колбу) одну каплю насыщенного раствора FeCl3, во вторую пробирку (колбу) одну каплю
- 49. Результаты эксперимента FeCl3 + 3NH4CNS ⇔ Fe(CNS)3 + 3NH4Cl 1 2 3 4
- 50. Направление смещение химического равновесия можно определить с помощью принципа Ле–Шателье: если на систему, находящуюся в равновесии,
- 51. Константа химического равновесия представляет собой дробь, в числителе которой стоит произведение равновесных концентраций (если реакция протекает
- 52. FeCl3 + 3NH4CNS ⇔ Fe(CNS)3 + 3NH4Cl В первую пробирку добавляли FeCl3 – окраска раствора усилилась,
- 53. Вывод: чтобы сместить химическое равновесие вправо, нужно увеличить концентрацию исходных веществ, а в лево – в
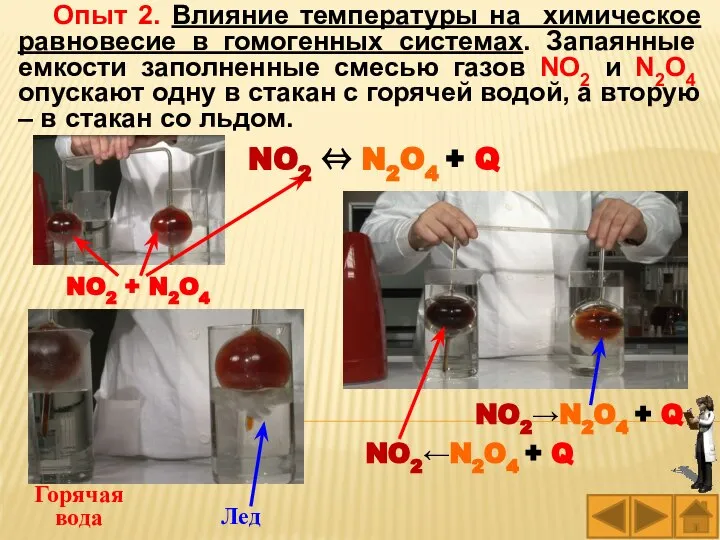
- 54. Опыт 2. Влияние температуры на химическое равновесие в гомогенных системах. Запаянные емкости заполненные смесью газов NO2
- 55. Реакция перехода оксида азота (IV) в димер этого оксида является экзотермической: NO2 ⇔ N2O4 + Q,
- 56. Практическая работа № 9 «Химическое равновесие в гетерогенных системах»
- 57. Цель – Познакомиться с условиями смещения химического равновесия в гетерогенных системах. Приборы и реактивы: химическая посуда,
- 58. Опыт 1. Влияние температуры на смещение химического равновесия. В растворе гидроксида аммония всегда соблюдается равновесие: NH3
- 59. В стакан с раствором гидроксида натрия добавляем фенолфталеин – раствор стал малиновым. NaOH NH4OH NaOH ⇔
- 60. Разольем полученные растворы в колбы.
- 61. При нагревании полученных растворов изменение окраски (обесцвечивание) происхо-дит в колбах с гидроксидом аммония – равновесие смещается
- 62. При охлаждении колбы с раствором гидроксида аммония окраска постепенно восстанавливается – равновесие смещается в сторону образования
- 63. NH3 + H2O ⇔ NH4OH ⇔ NH4+ + OH– Экзотермическая реакция Эндотермическая реакция Вывод: для увеличения
- 64. Ивчатов А. Л., Малов В. И. Химия воды и микробиология. – М.: ИНФРА-М, 2006. – 218
- 65. Габриелян О. С., Остроумов И. Г. Химия для профессий и специальностей технического профиля: учебник для студ.
- 66. Химическое равновесие – Википедия ru.wikipedia.org› Химическое равновесие в растворах.wmv youtube.com video.yandex.ru›химическое равновесие ... опыты yandex.ru/images›химическое равновесие
- 68. Скачать презентацию






















































 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Подготовка к ГИА по химии
Подготовка к ГИА по химии Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Гидроксиды металлов
Гидроксиды металлов Химические равновесия в растворах. Лекция 2 часть 2
Химические равновесия в растворах. Лекция 2 часть 2 Nazwa peptydu. Sekwencja
Nazwa peptydu. Sekwencja Полімери. Пінополістирол
Полімери. Пінополістирол 5 группа элементов
5 группа элементов Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Водородная химическая связь
Водородная химическая связь Коррозия. способы защиты от коррозии
Коррозия. способы защиты от коррозии Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Электролиз воды
Электролиз воды Генетические ряды углеводородов. Обобщение и систематизация знаний
Генетические ряды углеводородов. Обобщение и систематизация знаний Адсорбционные материалы. Цеолиты
Адсорбционные материалы. Цеолиты Химическая термодинамика
Химическая термодинамика Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Физическая химия. Вводная лекция
Физическая химия. Вводная лекция Строение вещества. ОВР. Окислительно-восстановительные реакции
Строение вещества. ОВР. Окислительно-восстановительные реакции Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Мыльная история
Мыльная история Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства алотропні модифікації неметалів
алотропні модифікації неметалів Презентация для заочников
Презентация для заочников Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Алкины. Понятие об алкинах
Алкины. Понятие об алкинах