Слайд 2ХИМИЯ
ОРГАНИЧЕСКАЯ
НЕОРГАНИЧЕСКАЯ
Слайд 3ХИМИЯ
ФИЗИЧЕСКАЯ
АНАЛИТИЧЕСКАЯ
ХИМИЧЕСКАЯ КИНЕТИКА
ХИМИЧЕСКАЯ ТЕРМОДИНАМИКА
ЭЛЕКТРОХИМИЯ
КВАНТОВАЯ ХИМИЯ
Слайд 4ИСТОРИЯ
Квантовая химия зародилась
в середине 20-х годов XX столетия.

Слайд 5ПРИЧИНЫ ВОЗНИКНОВЕНИЯ
Экспериментальный материал нуждался
в интерпретации.
Слайд 6ИССЛЕДОВАНИЯ
ВЕРНЕРА ГЕЙЗЕНБЕРГА
1926 г.

Слайд 7УРАВНЕНИЕ
ШРЁДИНГЕРА
Уравнение
описывает изменение
в пространстве
и во времени
чистого состояния.

Слайд 8ГИПОТЕЗА
ДЕ БРОЙЛЯ
Дуализм не является особенностью только оптических явлений,
а имеет универсальный

характер. Частицы вещества также обладают волновыми свойствами
Слайд 9МЕТОД ХАРТРИ-ФОКА
Дуглас Рейнер Хартри
Владимир Александрович Фок

Слайд 11+
относительная простота
помогает легко представить молекулу
описывает неорганическую химию

Слайд 12-
даёт правильное описание в малой области химических соединений
малая предсказательная способность
не даёт магнитных

свойств веществ и их геометрию
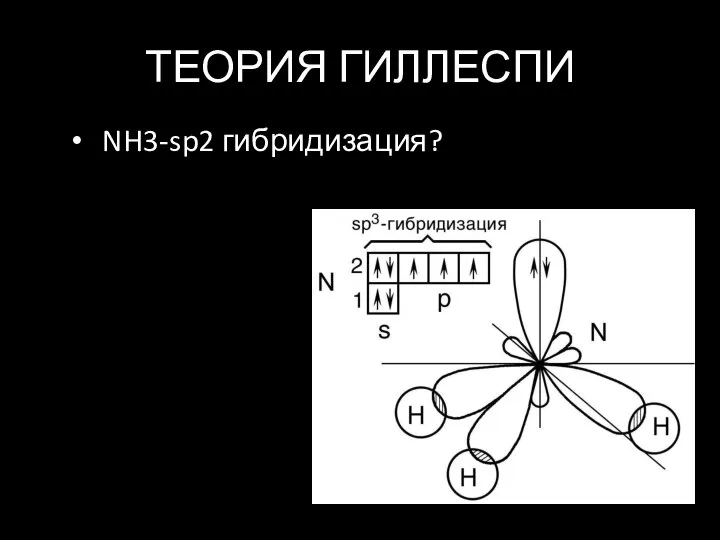
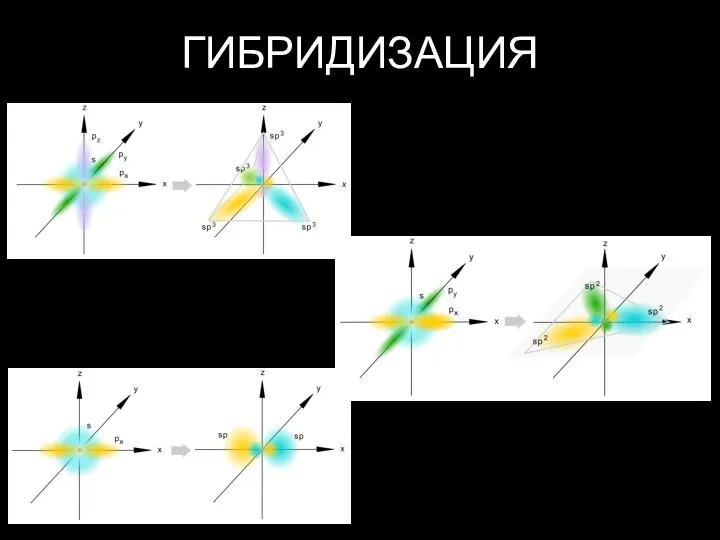
Слайд 14ТЕОРИЯ ГИЛЛЕСПИ
NH3-sp2 гибридизация?
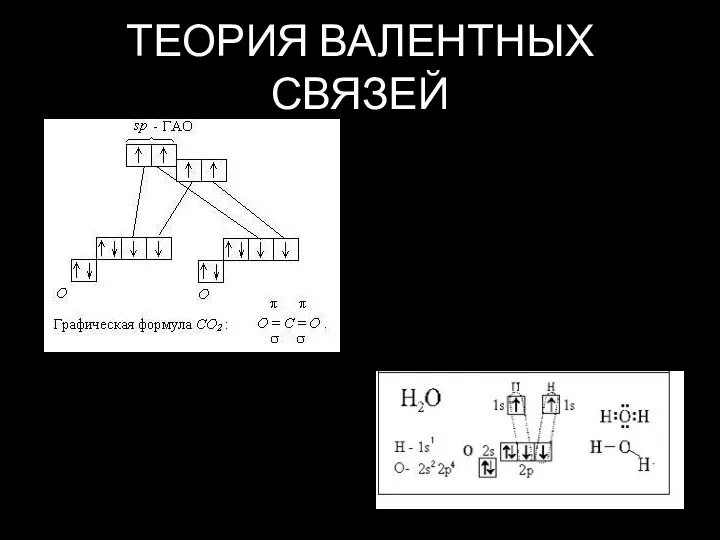
Слайд 15МЕТОД МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ
Является наиболее универсальным широко используемым методом описания природы химической связи.

Этот метод базируется на последних достижениях в области квантовой механики.
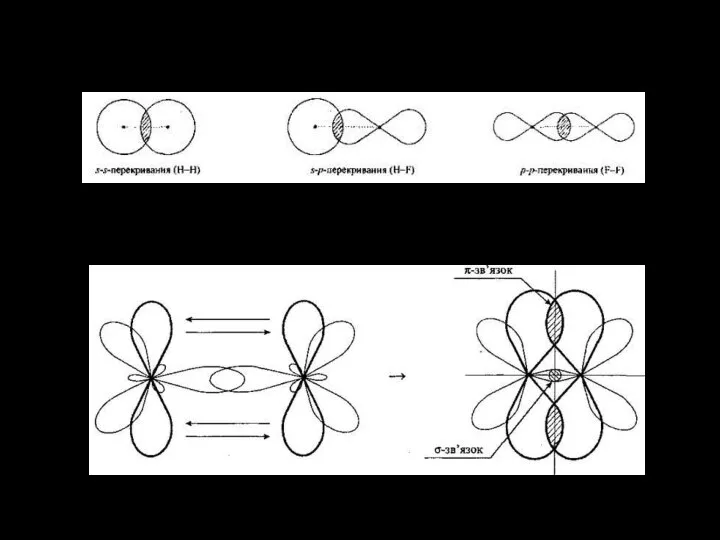
Слайд 16МЕТОД ЛИНЕЙНОЙ КОМБИНАЦИИ АТОМНЫХ ОРБИТАЛЕЙ
-ПРОСТЕЙШИЙ МЕТОД ОПРЕДЕЛЕНИЯ ВОЛНОВЫХ ФУНКЦИЙ МОЛЕКУЛЯРНЫХ ОРБИТАЛЕЙ.

Слайд 17+
даёт геометрию молекулы
объективнее отражает реальность
имеет сильную предсказательную способность, даже без расчёта
предсказывает магнитные

свойства молекул
относительная простота математики
Слайд 18-
сложность подбора коэффициента для атомной обретали
рост сложности расчёта молекул с ростом количества

атомов
Слайд 20ЭЛЕКТРОННЫЕ ЭФФЕКТЫ
-смещение электронной плотности в молекуле, ионе или радикале под влиянием

заместителей.
Слайд 21ИНДУКТИВНЫЙ ЭФФЕКТ
-эффект переноса электронной плотности вдоль сигма связей.


















 Химические реакции в органической химии
Химические реакции в органической химии Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Неньютоновская жидкость
Неньютоновская жидкость Язык естествознания. Химия
Язык естествознания. Химия Презентация на тему Химия и сельское хозяйство Пестициды
Презентация на тему Химия и сельское хозяйство Пестициды  Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах 12 принципов зелёной химии
12 принципов зелёной химии Алканы
Алканы Химическая связь. Строение вещества
Химическая связь. Строение вещества Диены. Понятие о диенах
Диены. Понятие о диенах Минералы и горные породы
Минералы и горные породы Типы химических реакций. 8 класс
Типы химических реакций. 8 класс Кварцевые пески
Кварцевые пески Вода как хладагент (R718)
Вода как хладагент (R718) Кроссворд по теме Металлы
Кроссворд по теме Металлы Оксиды
Оксиды Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Щелочные металлы
Щелочные металлы Органическая химия
Органическая химия Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна
Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна Кислород – основа жизни?
Кислород – основа жизни? Урок-путешествие по теме «Первоначальные химические понятия»
Урок-путешествие по теме «Первоначальные химические понятия» Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Введение в органическую химию. Состав и структура органических веществ
Введение в органическую химию. Состав и структура органических веществ Многоатомные спирты
Многоатомные спирты Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"