Содержание
- 2. Функции мышц Локомоторная 2. Обеспечение подвижности организма и сопротивление механической силе, в том числе и статическим
- 3. МОЛЕКУЛЯРНЫЕ МОТОРЫ Трансформируют химическую энергию в механическую. Используются для сокращения, транспорта органелл, подвижности клеток, клеточного деления
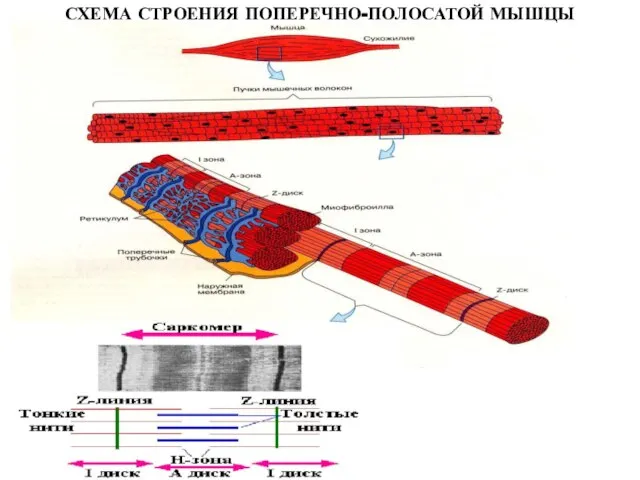
- 5. СХЕМА СТРОЕНИЯ ПОПЕРЕЧНО-ПОЛОСАТОЙ МЫШЦЫ
- 6. ХИМИЧЕСКИЙ СОСТАВ ПОПЕРЕЧНО-ПОЛОСАТЫХ МЫШЦ
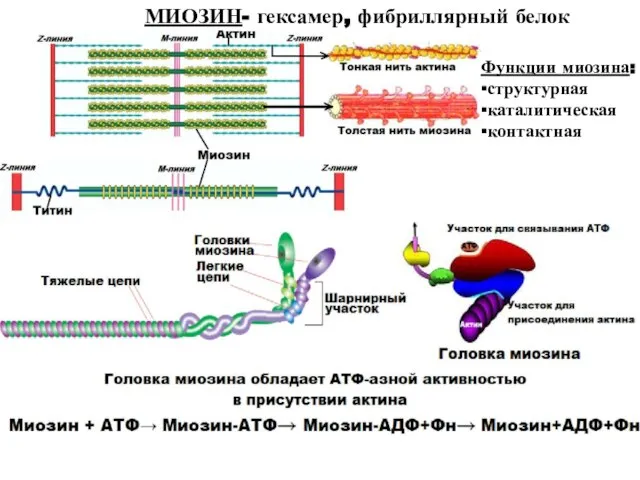
- 7. МИОЗИН- гексамер, фибриллярный белок Функции миозина: ▪структурная ▪каталитическая ▪контактная
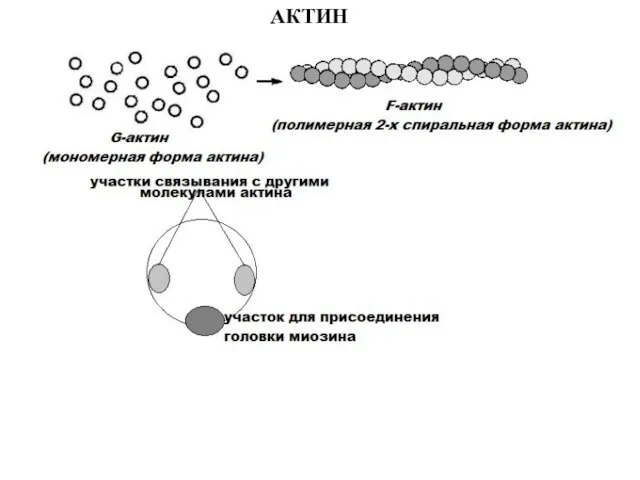
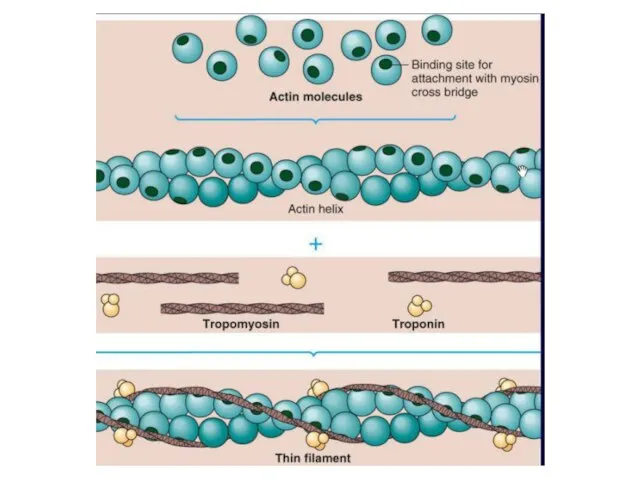
- 9. АКТИН
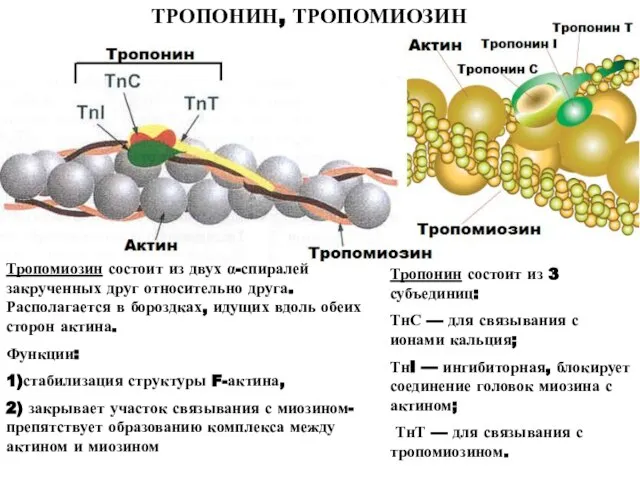
- 10. Тропомиозин состоит из двух α-спиралей закрученных друг относительно друга. Располагается в бороздках, идущих вдоль обеих сторон
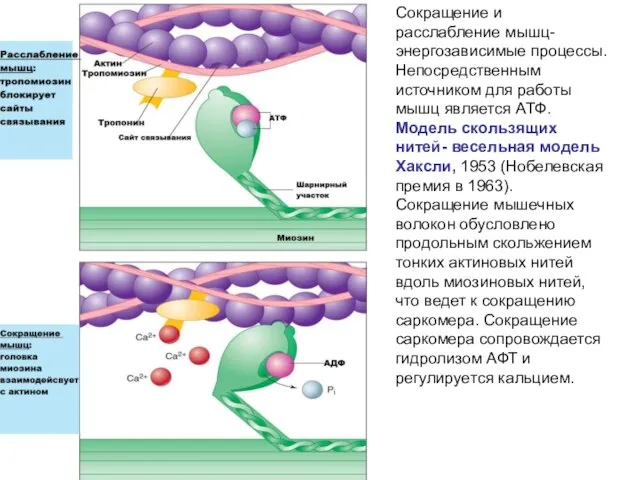
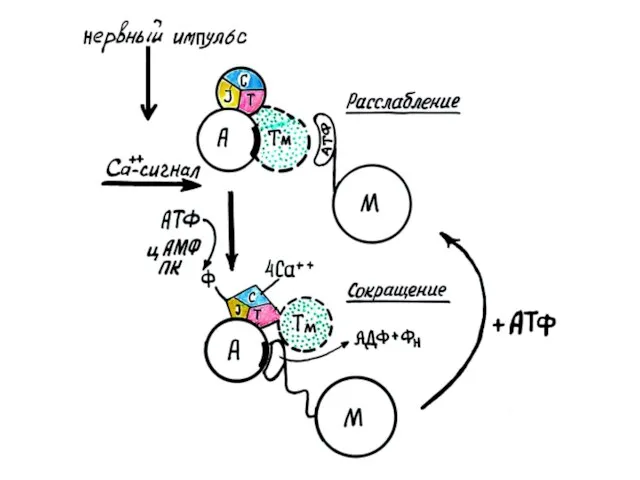
- 12. Сокращение и расслабление мышц- энергозависимые процессы. Непосредственным источником для работы мышц является АТФ. Модель скользящих нитей-
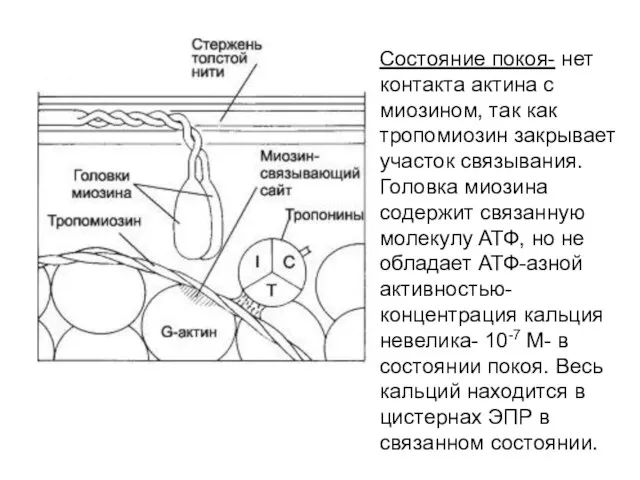
- 13. Состояние покоя- нет контакта актина с миозином, так как тропомиозин закрывает участок связывания. Головка миозина содержит
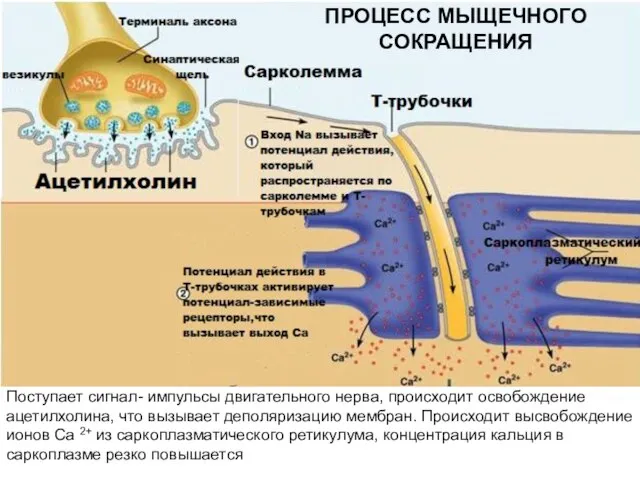
- 14. Поступает сигнал- импульсы двигательного нерва, происходит освобождение ацетилхолина, что вызывает деполяризацию мембран. Происходит высвобождение ионов Са
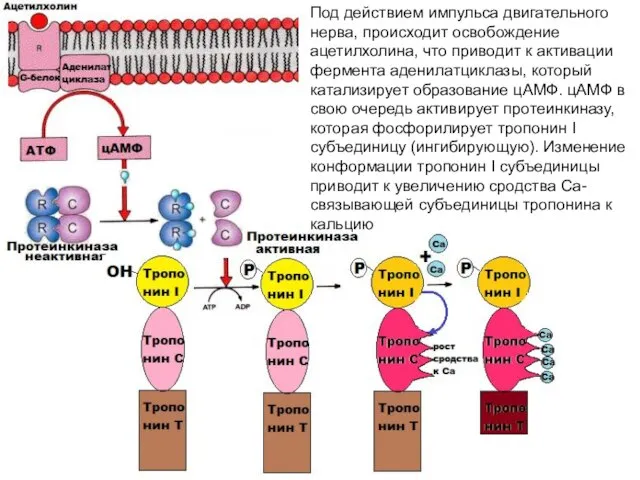
- 15. Под действием импульса двигательного нерва, происходит освобождение ацетилхолина, что приводит к активации фермента аденилатциклазы, который катализирует
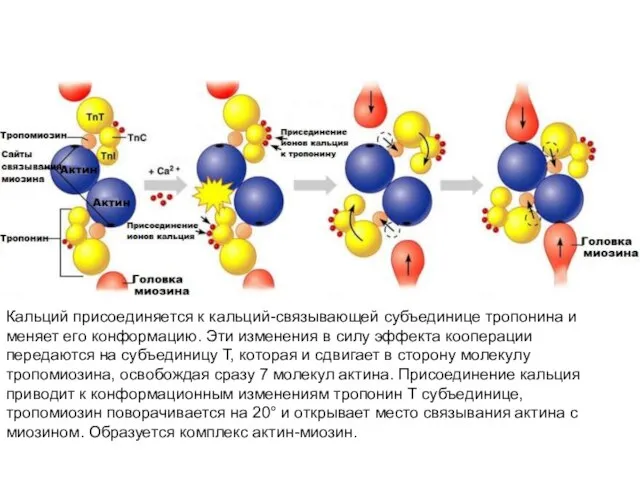
- 16. Кальций присоединяется к кальций-связывающей субъединице тропонина и меняет его конформацию. Эти изменения в силу эффекта кооперации
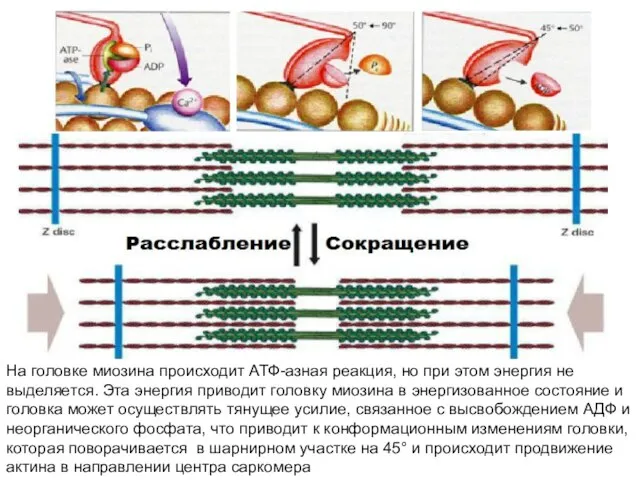
- 17. На головке миозина происходит АТФ-азная реакция, но при этом энергия не выделяется. Эта энергия приводит головку
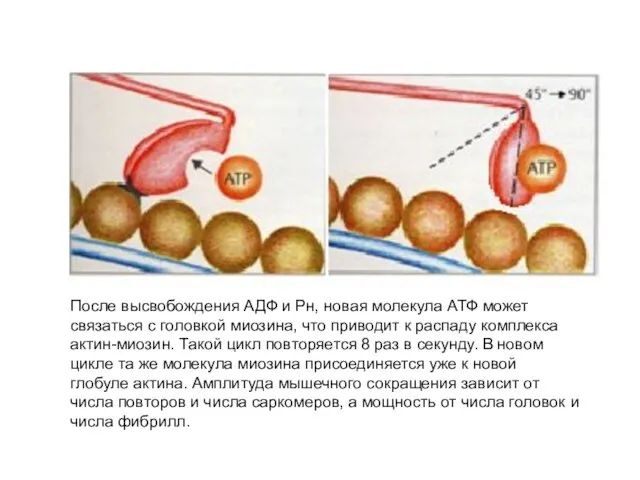
- 18. После высвобождения АДФ и Рн, новая молекула АТФ может связаться с головкой миозина, что приводит к
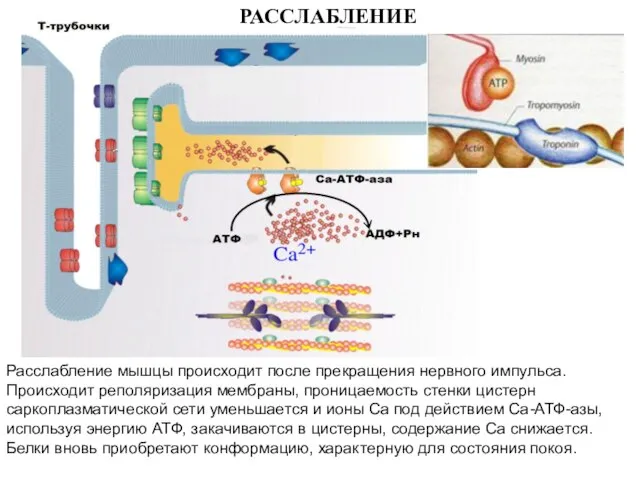
- 19. Расслабление мышцы происходит после прекращения нервного импульса. Происходит реполяризация мембраны, проницаемость стенки цистерн саркоплазматической сети уменьшается
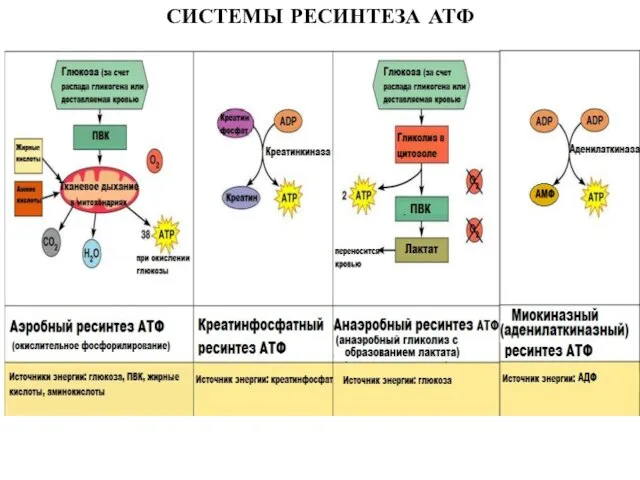
- 21. СИСТЕМЫ РЕСИНТЕЗА АТФ
- 22. на акт мышечного сокращения 2. на фосфорилирование тропонин I субъединицы 3. на синтез цАМФ 4. на
- 23. 1. Аэробный орган: 20% кислорода используется миокардом. 2. В 4 раз больше митохондрий, чем в скелетной
- 25. Скачать презентацию







 Что такое COVID-19?
Что такое COVID-19? Сестринское обследование пациентов терапевтического профиля
Сестринское обследование пациентов терапевтического профиля Этическое и правовое регулирование научных исследований
Этическое и правовое регулирование научных исследований Общая эпидемиология
Общая эпидемиология Перелом предплечья
Перелом предплечья Варикозная болезнь
Варикозная болезнь Холера. Что такое холера?
Холера. Что такое холера? Қант диабетінің қауіп факторлары
Қант диабетінің қауіп факторлары Сосудистый шов
Сосудистый шов Первая медицинская помощь при переломах
Первая медицинская помощь при переломах Эпилепсия: причины, диагностика, лечение
Эпилепсия: причины, диагностика, лечение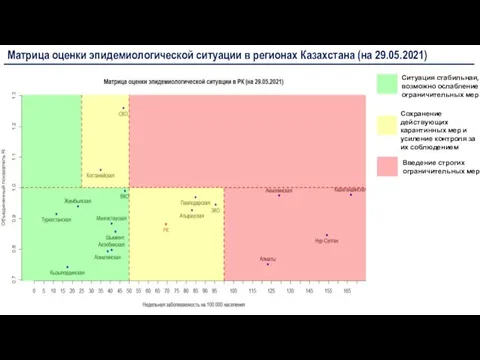 Матрица оценки эпидемиологической ситуации в регионах Казахстана
Матрица оценки эпидемиологической ситуации в регионах Казахстана Bacillus Major Reference Works
Bacillus Major Reference Works Фармацевтический рынок Украины. Что год грядущий нам готовит?.. Добранчук О.Л. Руководитель аналитической службы компании МОРИОН
Фармацевтический рынок Украины. Что год грядущий нам готовит?.. Добранчук О.Л. Руководитель аналитической службы компании МОРИОН  Физиологическое и психологическое развитие подростка
Физиологическое и психологическое развитие подростка Патологические переломы. Этиопатогенетическое лечение
Патологические переломы. Этиопатогенетическое лечение Игра. Средства, влияющие на функцию мочевыделительной системы
Игра. Средства, влияющие на функцию мочевыделительной системы Тыныс алу ағзалар ауруларының диагностикасындағы ЭКГ
Тыныс алу ағзалар ауруларының диагностикасындағы ЭКГ Количественные нарушения со стороны лейкоцитов
Количественные нарушения со стороны лейкоцитов Юкстагломерулярный аппарат почки
Юкстагломерулярный аппарат почки Трансаминирование. Тема 13
Трансаминирование. Тема 13 Бронхиальная астма
Бронхиальная астма СРС. Алгоритмы диагностики анемий и изменения гемостаза
СРС. Алгоритмы диагностики анемий и изменения гемостаза Раны, способы остановки кровотечений
Раны, способы остановки кровотечений lektsia_NMILS_FDPO_1_marta_2017
lektsia_NMILS_FDPO_1_marta_2017 Диспансеризация населения
Диспансеризация населения ВИЧ в Удмуртии: развитие эпидемии и современное состояние
ВИЧ в Удмуртии: развитие эпидемии и современное состояние Обследование больных с травмами и заболеваниями опорно-двигательного аппарата
Обследование больных с травмами и заболеваниями опорно-двигательного аппарата