Влияние ядерной ДНК на механизмы возникновения дефектов в митохондриальной днк: миделеции (точечные мутации) мтднк,
Содержание
- 2. ЦЕЛЬ, АКТУАЛЬНОСТЬ, ЗАДАЧИ Актуальность: митохондриальные болезни составляют большую группу патологических состояний, связанных с генетически детерминированными нарушениями
- 3. Строение митохондриальной ДНК СТРОЕНИЕ МИТОХОНДРИАЛЬНОЙ ДНК Митохондрии произошли от древних симбиотических бактерий, которые жили внутри примитивных
- 4. Сравнение строения митохондриальной и ядерной ДНК ПРОИСХОЖДЕНИЕ И ДЕГРАДАЦИЯ МИТОХОНДРИАЛЬНОГО ГЕНОМА В ходе коэволюции оказалось, что
- 5. СРАВНЕНИЕ МИТОХОНДРИАЛЬНОЙ И ЯДЕРНОЙ ДНК
- 6. СРАВНЕНИЕ МИТОХОНДРИАЛЬНОЙ И ЯДЕРНОЙ ДНК
- 7. МИТОХОНДРИАЛЬНАЯ ДНК ПОД КОНТРОЛЕМ ЯДЕРНОЙ Известно, что синтез мтДНК находится под контролем ядерных генов. Мутации в
- 8. КЛАССИФИКАЦИЯ ПО ПАТОГЕНЕЗУ Митохондриальные заболевания являются результатом унаследованных и/или спонтанных мутаций в митохондриальной ДНК (мтДНК) и/или
- 9. КЛАССИФИКАЦИЯ ПО ЭТИОЛОГИИ Митохондриальные болезни, обусловленные генными мутациями ядерной ДНК Митохондриальные болезни, в основе которых лежат
- 10. ФЕНОТИПЫ ЯДЕРНО-КОДИРУЕМЫХ МИТОХОНДРИАЛЬНЫХ ЗАБОЛЕВАНИЙ
- 11. МИТОХОНДРИАЛЬНЫЕ СИНДРОМЫ, КОДИРУЕМЫЕ ЯДЕРНЫМИ ГЕНАМИ
- 12. ТОЧЕЧНЫЕ МУТАЦИИ МИТОХОНДРИАЛЬНОЙ ДНК В основе патогенеза синдрома MELAS лежат точечные мутации мтДНК, преимущественно генов транспортных
- 13. Атрофия зрительного нерва ДЕЛЕЦИИ МИТОХОНДРИАЛЬНОЙ ДНК, НАСЛЕДУЕМЫЕ ПО АУТОСОМНО-РЕЦЕССИВНОМУ ТИПУ Течение заболевания в виде митохондриальной энцефаломиопатии
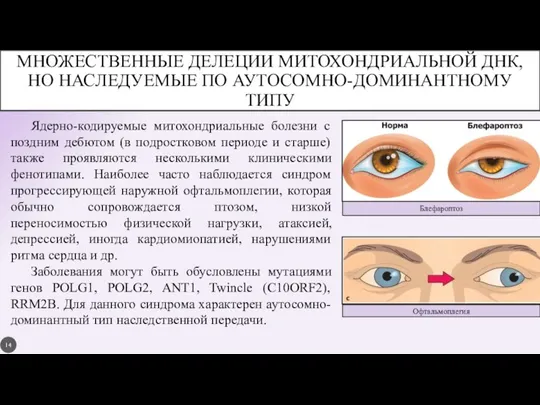
- 14. Офтальмоплегия Блефароптоз МНОЖЕСТВЕННЫЕ ДЕЛЕЦИИ МИТОХОНДРИАЛЬНОЙ ДНК, НО НАСЛЕДУЕМЫЕ ПО АУТОСОМНО-ДОМИНАНТНОМУ ТИПУ Ядерно-кодируемые митохондриальные болезни с поздним
- 15. ЗАКЛЮЧЕНИЕ Несмотря на небольшой размер, митохондриальный геном отвечает за правильное функционирование электростанций наших клеток. Этот кольцевой
- 16. СПИСОК ЛИТЕРАТУРЫ Harbauer, A.B., Zahedi, R.P., Sickmann, A., Pfanner, N., and Meisinger, C. (2014) The protein
- 18. Скачать презентацию














 Моя профессия не терпит табака
Моя профессия не терпит табака Начальные проявления нарушений мозгового кровообращения
Начальные проявления нарушений мозгового кровообращения Основы эпидемиологии при ботулизме
Основы эпидемиологии при ботулизме Симптомы при заболеваниях желудочно-кишечного тракта
Симптомы при заболеваниях желудочно-кишечного тракта Вариации п-образных швов для сшивания кожи и сосудов
Вариации п-образных швов для сшивания кожи и сосудов Плюсы и минусы перевода питания в медицинских организациях на систему аутсорсинга
Плюсы и минусы перевода питания в медицинских организациях на систему аутсорсинга Сальмонеллезы
Сальмонеллезы Заболевания кожи. Акне. Угри. Экзема. Герпес
Заболевания кожи. Акне. Угри. Экзема. Герпес Анестезиология и реанимация (АиР) на догоспитальном этапе
Анестезиология и реанимация (АиР) на догоспитальном этапе Хроническая венозная недостаточность
Хроническая венозная недостаточность Құрсақ қуысының қуысты мүшелеріне жасалатын шұғыл операциялар
Құрсақ қуысының қуысты мүшелеріне жасалатын шұғыл операциялар О концепции медицинского обеспечения населения Российской Федерации в военное время
О концепции медицинского обеспечения населения Российской Федерации в военное время Гигиена кожных покровов
Гигиена кожных покровов Местная анестезия
Местная анестезия Ишемическая болезнь сердца (ИБС). Стенокардия
Ишемическая болезнь сердца (ИБС). Стенокардия Профилактика, диагностика и лечение туберкулеза
Профилактика, диагностика и лечение туберкулеза Хламидиялық инфекция
Хламидиялық инфекция Стоматология и Психология
Стоматология и Психология Судебно-медицинская травматология. Повреждения твердыми тупыми предметами
Судебно-медицинская травматология. Повреждения твердыми тупыми предметами uporotaya_versia(1)
uporotaya_versia(1) Возрастные особенности, миелинизация. Основные пороки развития
Возрастные особенности, миелинизация. Основные пороки развития Оптимизация профилактики синдрома сухого глаза у лиц подросткового возраста
Оптимизация профилактики синдрома сухого глаза у лиц подросткового возраста Применение и эффективность использования циклоферона и цитофлавина при лечении больных острыми кишечными инфекциями
Применение и эффективность использования циклоферона и цитофлавина при лечении больных острыми кишечными инфекциями Медицинское обеспечение ночных и трансмеридианных полетов
Медицинское обеспечение ночных и трансмеридианных полетов Глаукома. Виды глаукомы
Глаукома. Виды глаукомы Акушерские кровотечения
Акушерские кровотечения Online конкурс анатомическая модель
Online конкурс анатомическая модель Добро пожаловать в ООО ГСП-2!
Добро пожаловать в ООО ГСП-2!