Слайд 2План лекции:
Основные закономерности метаболизма ксенобиотиков.
Микросомальная монооксигеназная система.
Основные реакции превращений лекарств в

организме.
Конъюгационные реакции превращения лекарств в организме.
Факторы, влияющие на метаболизм лекарственных средств.
Слайд 3Основные закономерности метаболизма ксенобиотиков
Большинство лекарственных средств является для организма чужеродными веществами -

ксенобиотиками, не входящими в биотический круговорот и способными, наряду с нормализацией физиологических процессов, оказывать токсический эффект. Вследствии этого они подвергаются метаболическим превращениям и выведению из организма. В метаболизме ксенобиотиков выделяют три основные фазы:
Всасывание
Биотрансформация
Выведение
Слайд 4Различают две фазы биотрансформации:
1.Реакции окисления, восстановления,
гидролиза;
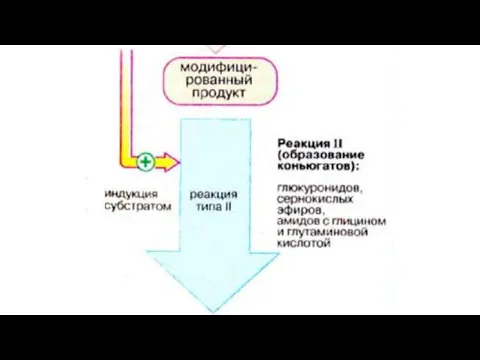
2. Реакции конъюгации – взаимодействие ксенобиотиков или

их метаболитов с различными эндогенными гидрофильными
молекулами.
Основной целью приведенных выше реакций является снижение липофильности (повышение растворимости в воде) ксенобиотиков для последующего выведения.
Слайд 8Микросомальная монооксигеназная система
Микросомальное окисление – это последовательность реакций с участием оксигеназ и

НАДФН, приводящих к внедрению атома кислорода в состав неполярной молекулы и появлению у нее гидрофильности и повышает ее реакционную способность. Окислительный метаболизм липофильных субстратов, происходящий в мембранах животных клеток (эндоплазматическом ретикулуме, миохондриях и других мембранах), играет ключевую роль во многих метаболических и регуляторных процессах и является биохимической основой многих клеточных функций: среди них такие, как синтез холестерина, десатурация жирных кислот, перекисное окисление мембранных липидов, синтез стероидных гормонов, витамина D3, метаболизм простагландинов, тироксина, метаболизм огромного числа ксенобиотиков, включая лекарства и химические канцерогены.
Слайд 9Окислительные реакции этого типа осуществляются мультиферментной системой(ферменты организуют короткие цепи, которые заканчиваются

цитохромом P450), главными компонентами которой считаются содержащая флавин НАДФН-цитохром Р-450 редуктаза и обширное семейство гомологичных гем-содержащих белков, объединяемых под именем цитохрома Р-450. Цитохром Р-450 является хромопротеином, в структуре которого заключено железо с переменной валентностью (2+ в покоящемся состоянии, 3+ при активности).
Слайд 111) восстановления кислорода до супероксидного радикала, катализируемое
НАДФН:цитохром Р-450-редуктазой внутри мембраны, где концентрация

О2 в 4-5 раз
больше, чем в окружающей мембрану водной фазе
НАДФН + 2О2 = НАДФ+ + Н+ + 2 О2-
2) реакция дисмутации О2- с образованием пероксидного аниона
О2- + О2- = О2 + О22-
В водных растворах (где достаточно высока концентрация протонов и где обычно
изучаются реакции с участием радикалов кислорода) эта реакция высокоэкзотермична и
идет с огромной скоростью, но в апротонной среде (внутри мембраны) эта реакция
должна быть резко сдвинута влево, поскольку анион перекиси водорода О22- нестабилен и
для его стабилизации требуется присоединение протона. Энергия, выделяемая при
присоединении Н+ к О22-, сравнима с энергией, необходимой для отрыва протона от
окисляемого субстрата и поэтому в присутствии липофильных субстратов (R-CH)
становится возможной реакция, приводящая к образованию соответствующих
карбанионов (R-C-)
О22- + R-CH = HO2- + R-C
Слайд 12Цитохром Р450 взаимодействует с молекулярным кислородом и включает один атом кислорода в

молекулу субстрата, способствуя появлению (усилению) у нее гидрофильности, а другой – в молекулу воды.
Работа цитохрома Р450 обеспечивается двумя ферментами:
НАДНцитохром b5‑оксидоредуктаза, содержит ФАД,
НАДФНцитохром Р450‑оксидоредуктаза, содержит ФМН и ФАД.
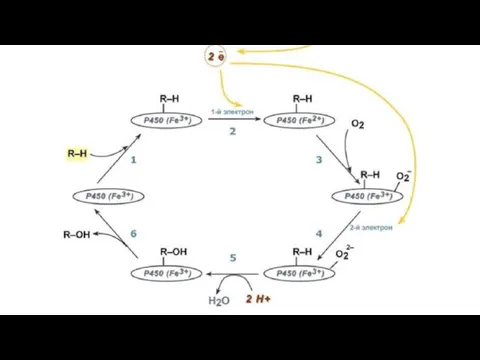
Слайд 13Последовательность реакций гидроксилирования субстратов
с участием цитохрома Р450
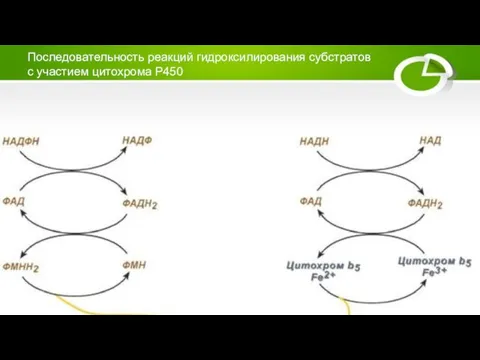
Слайд 15Основные реакции превращений лекарств в организме
Наибольшее значение придается следующим реакциям превращения лекарственных

средств:
1) гидроксилированию ароматических соединений (салициловая кислота и др.);
2) гидроксилированию алифатических соединений (мепробамат и др.);
3) окислительному дезаминированию (фенамин и др.);
4) S-дезалкилированию (6-метилтиопурин и др.);
5) О-дезалкилированию (фенацетин и др.);
6) N-дезалкилированию (ипрониазид и др.);
7) сульфоокислению (тиобарбитал и др.);
8) N-окислению (диметиланилин и др.).
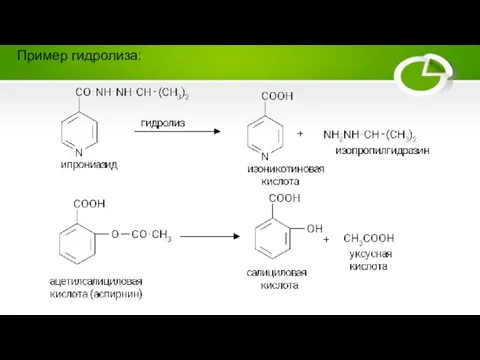
Слайд 16Метаболизацию салициловой кислоты:
Гидроксилированию ароматических соединений
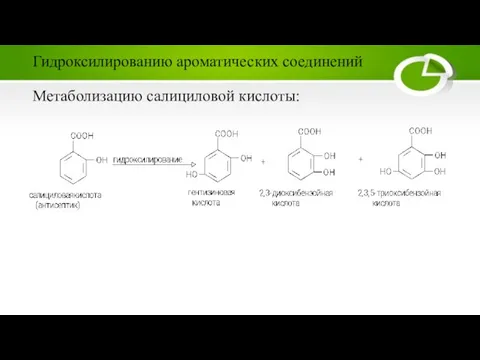
Слайд 17Превращением мепробамата:
Гидроксилированию алифатических соединений

Слайд 18Превращения фенамина:
Окислительное дезаминирование:
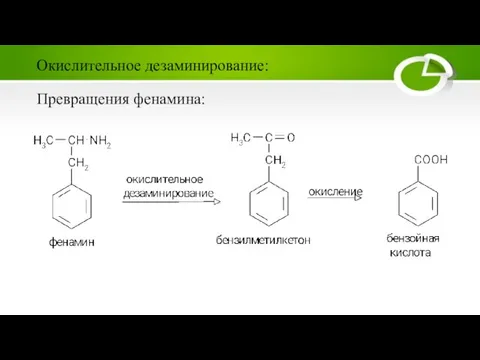
Слайд 19Метаболизм метилтиопурин, метилмеркаптан, S-метилцистеин, S-метилтиобензтиазол, метитурал и др.
S-дезалкилирование
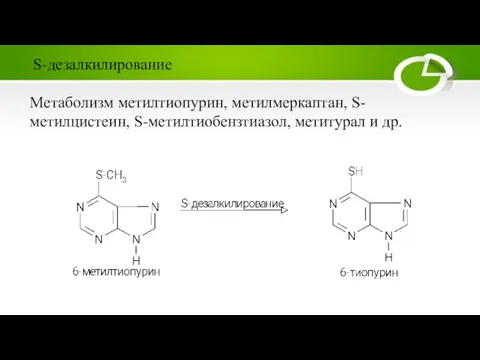
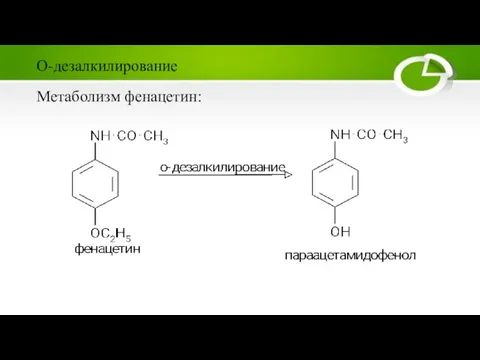
Слайд 20Метаболизм фенацетин:
О-дезалкилирование
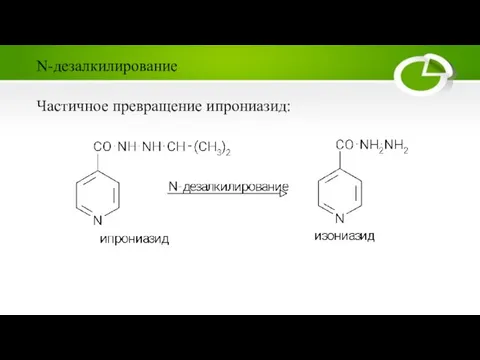
Слайд 21Частичное превращение ипрониазид:
N-дезалкилирование
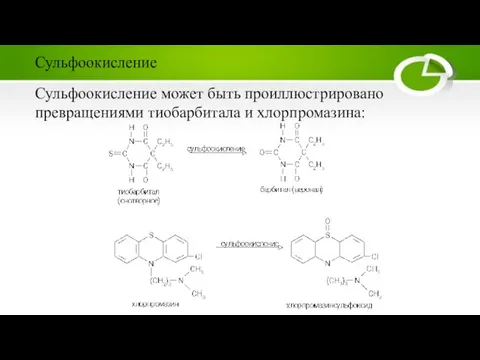
Слайд 22Сульфоокисление может быть проиллюстрировано превращениями тиобарбитала и хлорпромазина:
Сульфоокисление
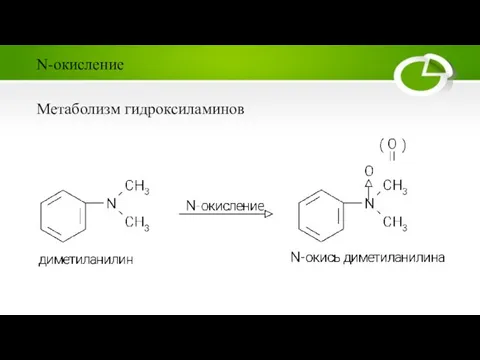
Слайд 23Метаболизм гидроксиламинов
N-окисление
Слайд 26Конъюгационные реакции превращения лекарств в организме
Продукты метаболизма чужеродных веществ, образовавшихся в первой

фазе биотрансформации, подвергаются дальнейшей детоксикации в результате каскада биохимических реакций. При этом, в реакциях первой фазы помимо повышения гидрофильности веществ происходит их активация и повышение реакционной способности перед реакциями второй фазы. Конечная цель этих реакций – маскировка токсичных групп в составе молекулы и придание ей большей гидрофильности.Соединения, обладающие активными группами, в гепатоцитах могут метилироваться при участии S-аденозилметионина, могут связываться с глицином и глутамином, с глутатионом, с глюкуроновой, серной и уксусной кислотами.
Слайд 27Последние в клетках часто находятся в связанном состоянии, например:
серная кислота связана с

3'-фосфоаденозин-5'-фосфатом и образует фосфоаденозинфосфосульфат (ФАФС),
глюкуроновая кислота связана с уридилдифосфорной кислотой и образует уридилдифосфоглюкуроновую кислоту (УДФГК),
уксусная кислота находится в виде ацетил-S-KoA.
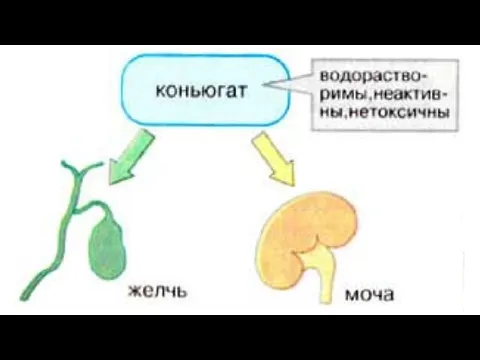
Наиболее активны в печени реакции конъюгации, катализируемые глутатион-S-трансферазой, сульфотрансферазой и УДФ-глюкуронилтрансферазой. Конъюгаты веществ с глутатионом, серной и глюкуроновой кислотами выводятся из организма преимущественно с мочой.
Слайд 29Уридиндифосфатные коферменты участвуют в образовании глюкуронидных и гликозидных (редко) коньюгатов. Уридиндифосфатглюкуроновая кислота
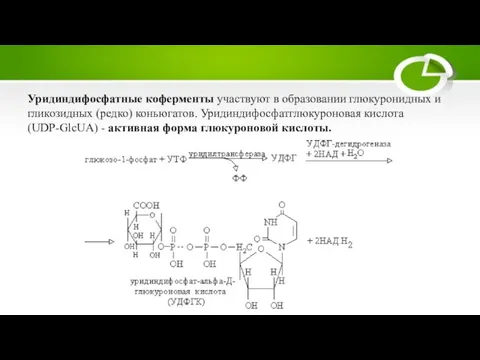
(UDP-GlcUA) - активная форма глюкуроновой кислоты.
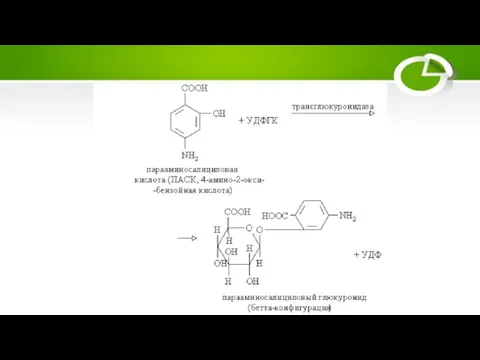
Слайд 31В качестве примера конъюгации с образванием коферментного комплекса и конъюгата может служить
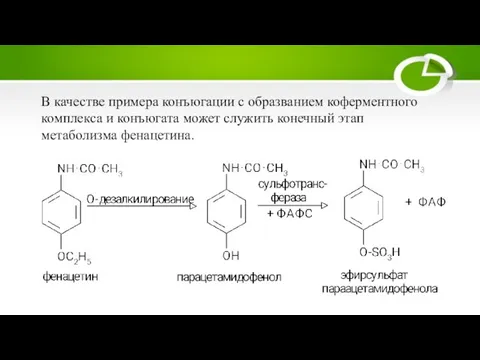
конечный этап метаболизма фенацетина.
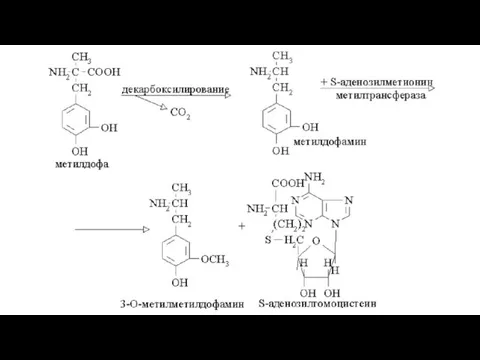
Слайд 32В качестве примера О‑метилирования лекарства можно привести один из этапов метаболизма метилдофа –

вещества, нарушающего образование адренергического медиатора и применяемого как гипотензивное средство.
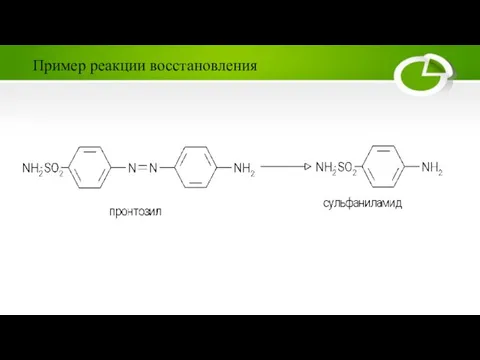
Слайд 34Как пример инактивации лекарственных веществ с помощью ацетил-КоА можно привести реакцию ацетилирования

сульфаниламидов.
Слайд 35Механизм пептидной конъюгации, заключающийся в образовании коэнзим-А-производных чужеродных карбоновых кислот (первый этап)

и с помощью реакций с глицином (второй этап), можно проследить на примере образования гиппуровой кислоты в процессе метаболизма бензойной кислоты, являющейся метаболитом некоторых лекарственных веществ (к примеру, фенамина).
Слайд 36Система глутатиона, наряду с глюкуронидной и сульфатной конъюгацией, составляет основу биохимических механизмов

поддержания гомеостаза при действии на организм лекарственных веществ.
Слайд 37Факторы, влияющие на метаболизм лекарственных средств.
Существенной особенностью микросомального окисления является способность к

индукции или ингибированию, т.е. к изменению мощности процесса.
Индукторами являются вещества, активирующие синтез цитохрома Р450 и транскрипцию соответствующих мРНК. Они бывают:
1. Широкого спектра действия: обладают способностью стимулировать синтез цитохрома Р450, НАДФН-цитохром Р450-оксидоредуктазы и глюкуронилтрансферазы. Классическим представителем являются производные барбитуровой кислоты – барбитураты, также в эту группу входят диазепам, карбамазепин, рифампицин и др.
2. Узкого спектра действия: стимулируют одну из форм цитохрома Р450 – ароматические полициклические углеводороды (метилхолантрен, спиронолактон), этанол.
Слайд 38Ингибиторы микросомального окисления связываются с белковой частью цитохрома или с железом гема.

Они делятся на:
1. Обратимые:
прямого действия – угарный газ (СО), антиоксиданты,
непрямого действия, т.е. влияют через промежуточные продукты своего метаболизма, которые образуют комплексы с цитохромом Р450 – эритромицин.
2. Необратимые ингибиторы – аллопуринол, аминазин, прогестерон, оральные контрацептивы, тетурам, фторурацил,
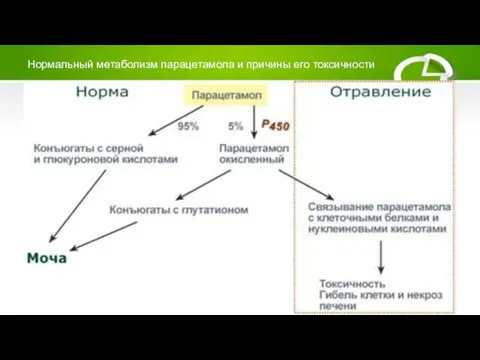
Слайд 39Нормальный метаболизм парацетамола и причины его токсичности






























 Диабетическая кардиомиопатия
Диабетическая кардиомиопатия Естественное вскармливание
Естественное вскармливание Памятка АйБолит в помощь студентам
Памятка АйБолит в помощь студентам Основы электрофизиологии
Основы электрофизиологии практический опыт
практический опыт История развития профилактики ВБИ
История развития профилактики ВБИ HFSA 2010 Подробные руководящие принципы по сердечной недостаточности
HFSA 2010 Подробные руководящие принципы по сердечной недостаточности Сестринский уход при заболевании ЛОР-органов
Сестринский уход при заболевании ЛОР-органов Лечебно-профилактическое предприятие Итальянский закат в Краснодарском крае
Лечебно-профилактическое предприятие Итальянский закат в Краснодарском крае ОФЭКТ/КТ в дифференциальной диагностике узловых образований молочных желез
ОФЭКТ/КТ в дифференциальной диагностике узловых образований молочных желез Профилактика и правила сна
Профилактика и правила сна Организация работы дошкольного и школьного отдела детской поликлиники
Организация работы дошкольного и школьного отдела детской поликлиники Острый и подострый эндокардит (инфекционный эндокардит). Лечение
Острый и подострый эндокардит (инфекционный эндокардит). Лечение Транскраниальная микрополяризация мозга ТКММ
Транскраниальная микрополяризация мозга ТКММ Ожирение и метаболический синдром
Ожирение и метаболический синдром Функции желёз внутренней секреции
Функции желёз внутренней секреции Рациональная фармакотерапия болезней, передающихя половым путем у подростков
Рациональная фармакотерапия болезней, передающихя половым путем у подростков Лейкоэнцефалит Шильдера
Лейкоэнцефалит Шильдера Основные запасы кислорода в организме
Основные запасы кислорода в организме Полный аборт
Полный аборт Требования к ситуационной задаче
Требования к ситуационной задаче Моя профессия не терпит табака
Моя профессия не терпит табака Zagadnienia kliniczne w masażu
Zagadnienia kliniczne w masażu Общая хирургия. Отёк и трофическая язва на фоне нарушения венозного кровообращения
Общая хирургия. Отёк и трофическая язва на фоне нарушения венозного кровообращения Аяқ - қолдың хирургиялық және туа біткен аурулары
Аяқ - қолдың хирургиялық және туа біткен аурулары Эклампсия и Преэклампсия Беременных
Эклампсия и Преэклампсия Беременных Анемия. Жалпы жағдайын қарау
Анемия. Жалпы жағдайын қарау Искусственные жиры - угроза здоровью
Искусственные жиры - угроза здоровью