Содержание
- 2. 1. Классификация 1.1. по положению аминогруппы 25.04.2012
- 3. 1.2. По количеству карбокси- и аминогрупп Моноаминомонокарбоновые кислоты (глицин, аланин, валин, лейцин, изолейцин, серин, треонин, цистеин,
- 4. 1.3 Классификация по встречаемости в белках 25.04.2012 20 классических протеиногенных аминокислот, информация о положении которых в
- 5. 1.4. По пищевой ценности для человека Аминокислоты делятся на заменимые и незаменимые. К незаменимым аминокислотам относят:
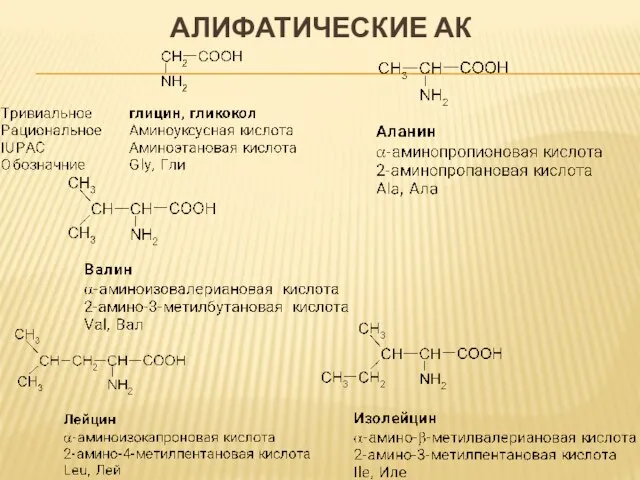
- 6. АЛИФАТИЧЕСКИЕ АК
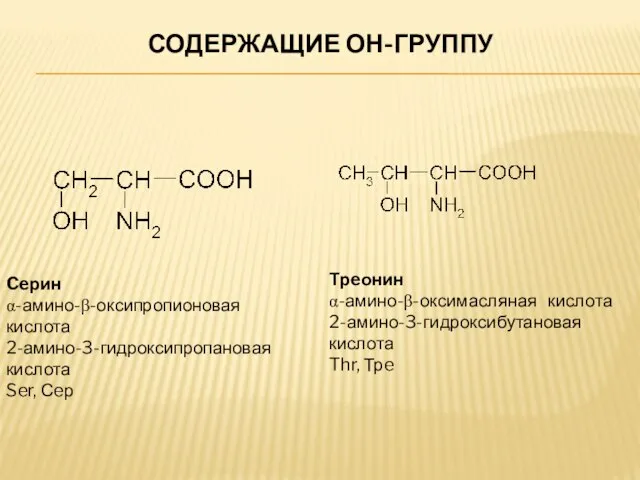
- 7. СОДЕРЖАЩИЕ ОН-ГРУППУ Ceрин α-амино-β-оксипропионовая кислота 2-амино-3-гидроксипропановая кислота Ser, Сeр Трeонин α-амино-β-оксимасляная кислота 2-амино-3-гидроксибутановая кислота Thr, Трe
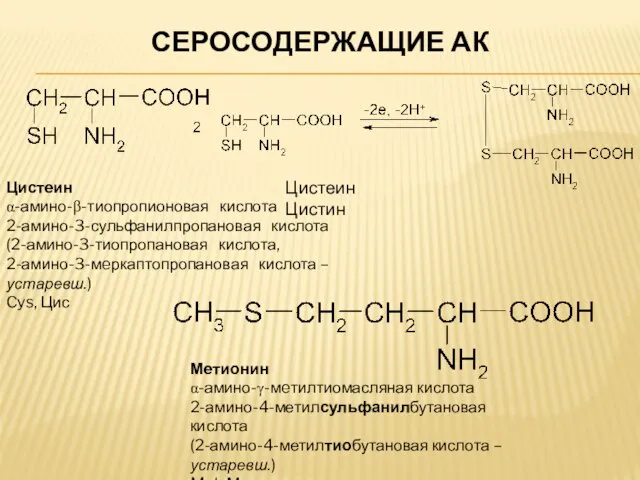
- 8. СЕРОСОДЕРЖАЩИЕ АК Цистеин Цистин Мeтионин α-амино-γ-мeтилтиомасляная кислота 2-амино-4-метилсульфанилбутановая кислота (2-амино-4-метилтиобутановая кислота – устаревш.) Met, Мет. Цистeин
- 9. МОНОАМИНОДИКАРБОНОВЫЕ КИСЛОТЫ И ИХ АМИДЫ Аспарагиновая кислота Аминоянтарная кислота Аминобутандиовая кислота Asp, Асп Глутаминовая кислота α-aминоглутаровая
- 10. СОДЕРЖАЩИЕ АМИНОГРУППУ Лизин α,ε-диаминокапроновая кислота 2,6-диаминогексановая кислота Lys, Лиз Аргинин α-амино-δ-гуанидилвалериановая кислота 2-амино-5-[амино(имино)метил]аминопентановая к-та Arg, Арг
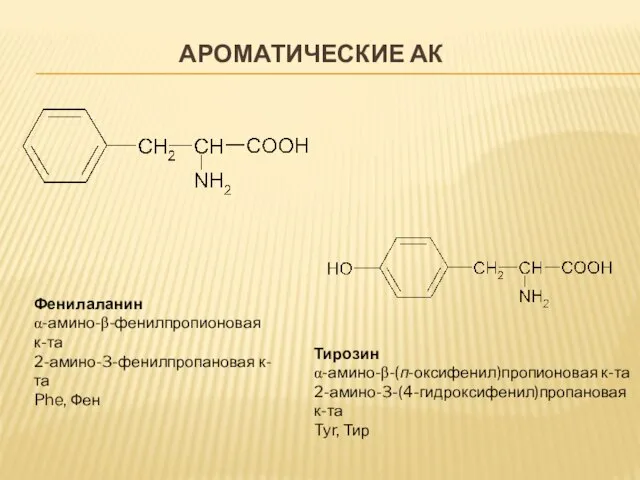
- 11. АРОМАТИЧЕСКИЕ АК Фенилаланин α-амино-β-фенилпропионовая к-та 2-амино-3-фенилпропановая к-та Phe, Фен Тирозин α-амино-β-(п-оксифенил)пропионовая к-та 2-амино-3-(4-гидроксифенил)пропановая к-та Tyr, Тир
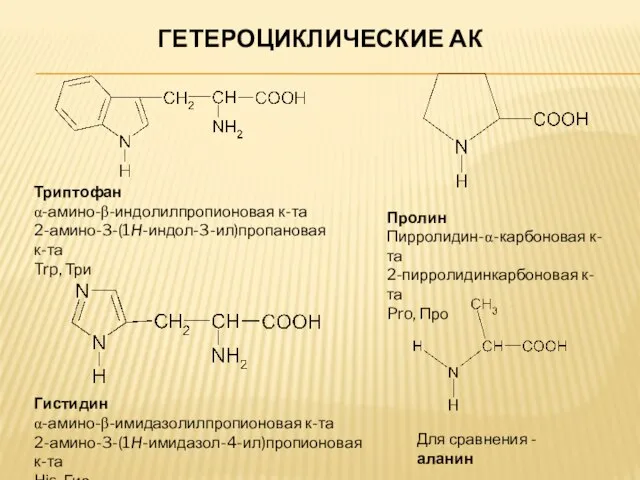
- 12. ГЕТЕРОЦИКЛИЧЕСКИЕ АК Триптофан α-амино-β-индолилпропионовая к-та 2-амино-3-(1H-индол-3-ил)пропановая к-та Trp, Три Гистидин α-амино-β-имидазолилпропионовая к-та 2-амино-3-(1H-имидазол-4-ил)пропионовая к-та His, Гис
- 13. 2. Номенклатура 2.1. Тривиальная номенклатура в основном используется для широко распространённых аминокислот. 2.2. Рациональная 2.3. IUPAC
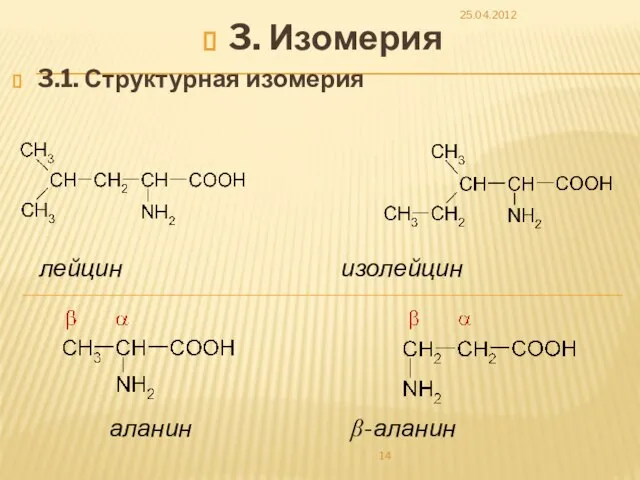
- 14. 3. Изомерия 3.1. Структурная изомерия 25.04.2012 лейцин изолейцин аланин β-аланин
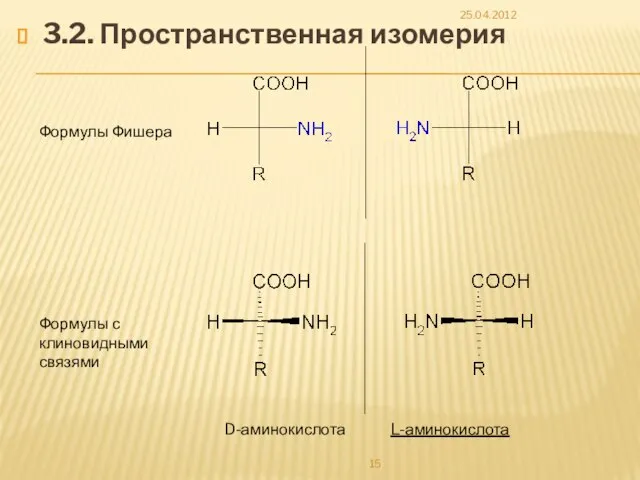
- 15. 3.2. Пространственная изомерия 25.04.2012 D-аминокислота L-аминокислота Формулы Фишера Формулы с клиновидными связями
- 16. 4. Физические свойства Аминокислоты, как правило, являются бесцветными кристаллическими соединениями. Большинство из них умеренно растворимы в
- 17. 5. Биологические свойства Из остатков аминокислот построены такие важные соединения как белки, которые участвуют практически во
- 18. うま味 Умами - “мясной вкус” 25.04.2012 Глутаминовая кислота (E620) и её соли (глутамат натрия Е621, глутамат
- 19. Глутаминовая кислота и её соли безопасны J Nutr. 2000 Apr;130(4S Suppl):1049S-52S. The safety evaluation of monosodium
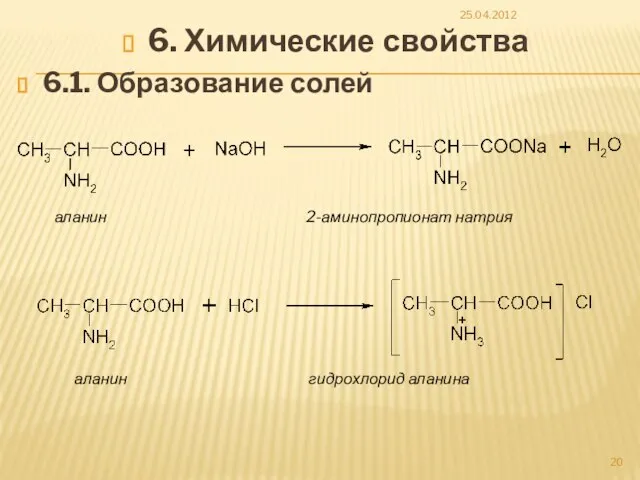
- 20. 6. Химические свойства 6.1. Образование солей 25.04.2012 аланин 2-аминопропионат натрия аланин гидрохлорид аланина
- 21. 25.04.2012 Аминогруппа нейтрализует карбоксильную группу, поэтому АК в твёрдом виде и в растворе при pH =
- 22. 25.04.2012 Сильнокислая среда Почти нейтральная Сильнощелочная среда Для моноаминомонокарбоновых кислот pI ≈ 5-6 pI моноаминодикарбоновых кислот
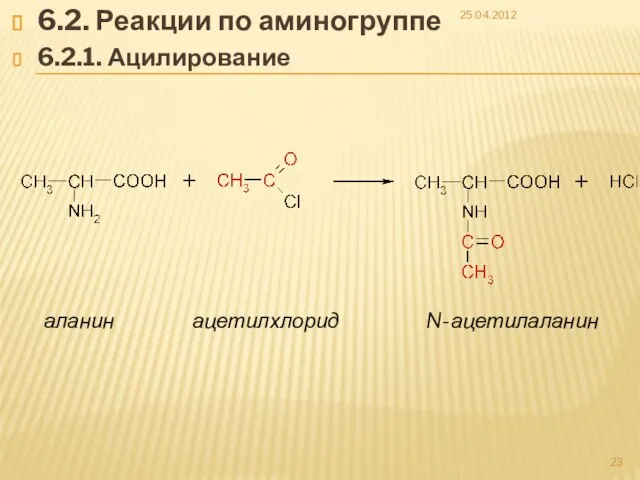
- 23. 6.2. Реакции по аминогруппе 6.2.1. Ацилирование 25.04.2012 аланин ацетилхлорид N-ацетилаланин
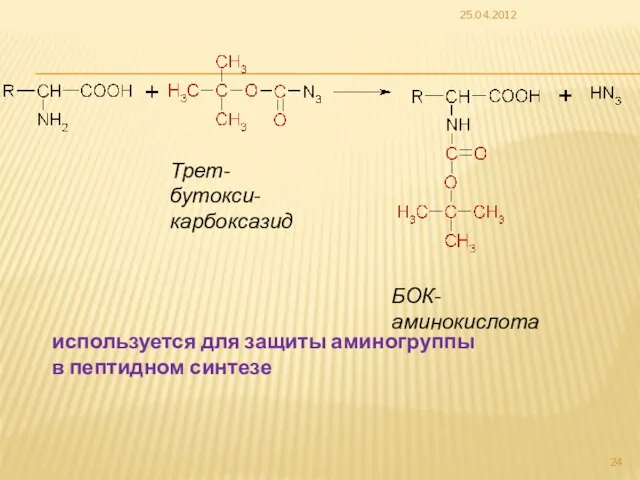
- 24. 25.04.2012 БОК-аминокислота Трет-бутокси-карбоксазид используется для защиты аминогруппы в пептидном синтезе
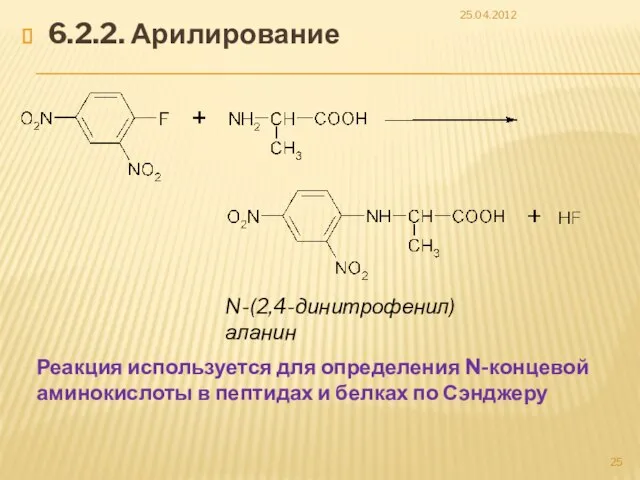
- 25. 6.2.2. Арилирование 25.04.2012 N-(2,4-динитрофенил)аланин Реакция используется для определения N-концевой аминокислоты в пептидах и белках по Сэнджеру
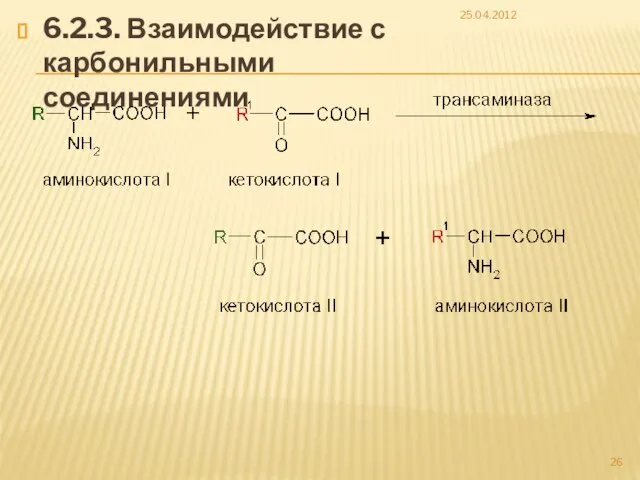
- 26. 6.2.3. Взаимодействие с карбонильными соединениями 25.04.2012
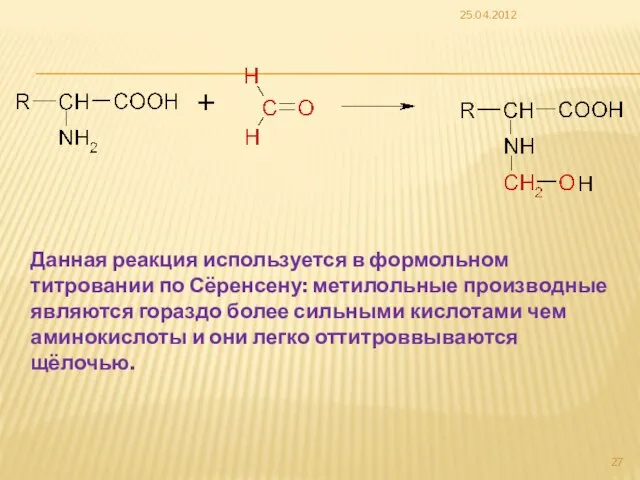
- 27. 25.04.2012 Данная реакция используется в формольном титровании по Сёренсену: метилольные производные являются гораздо более сильными кислотами
- 28. 6.2.4. Взаимодействие с азотистой кислотой 25.04.2012 α -аминокислота α-гидроксикислота Реакция с азотистой кислотой используется определения аминокислот
- 29. 6.2. Реакции по карбоксильной группе 25.04.2012 Реакция используется для защиты карбоксильной группы в синтезе пептидов
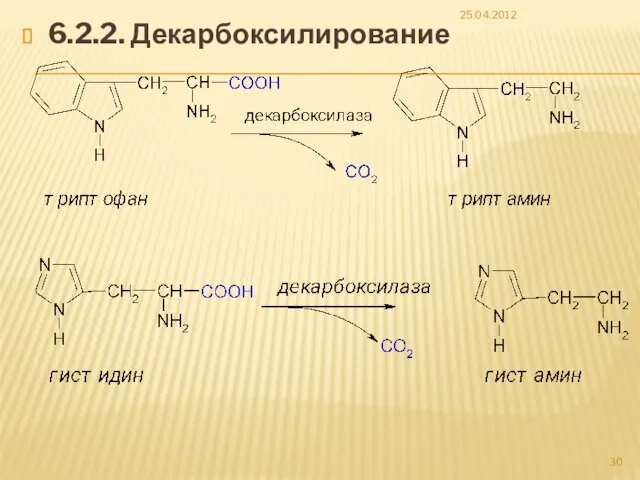
- 30. 6.2.2. Декарбоксилирование 25.04.2012
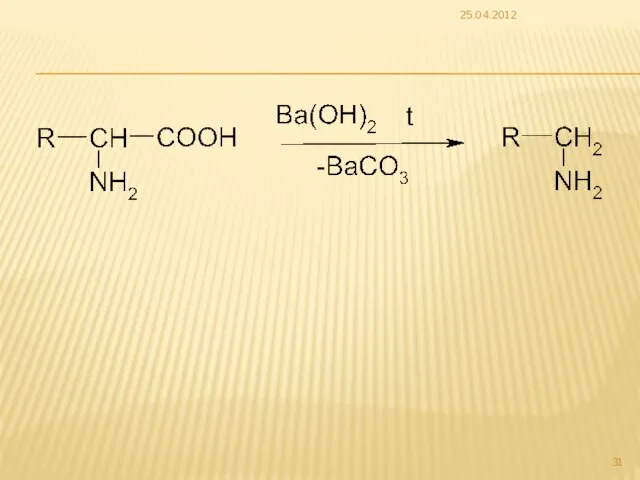
- 31. 25.04.2012
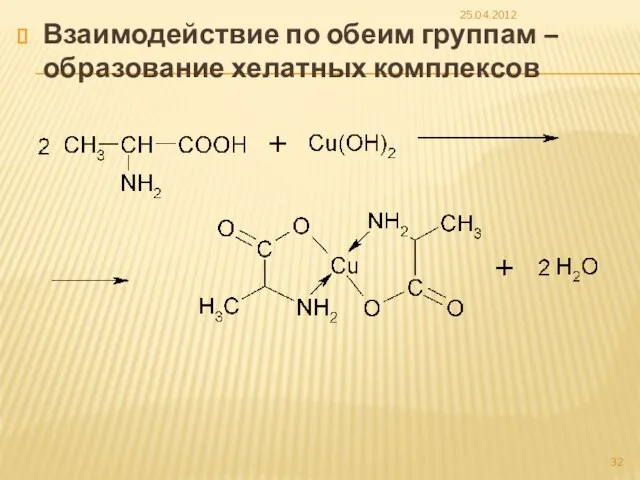
- 32. Взаимодействие по обеим группам – образование хелатных комплексов 25.04.2012
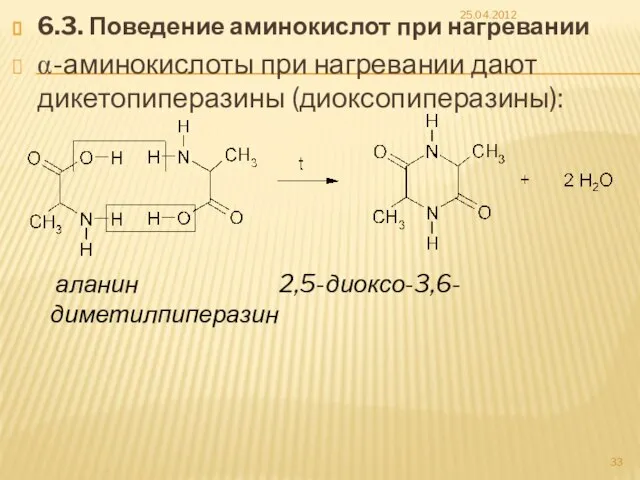
- 33. 6.3. Поведение аминокислот при нагревании α-аминокислоты при нагревании дают дикетопиперазины (диоксопиперазины): 25.04.2012 аланин 2,5-диоксо-3,6-диметилпиперазин
- 34. β-аминокислоты при нагревании отщепляют воду (реакция элиминирования), образуя ненасыщенные кислоты: 25.04.2012 β-аминопропионовая пропеновая (акриловая) кислота кислота
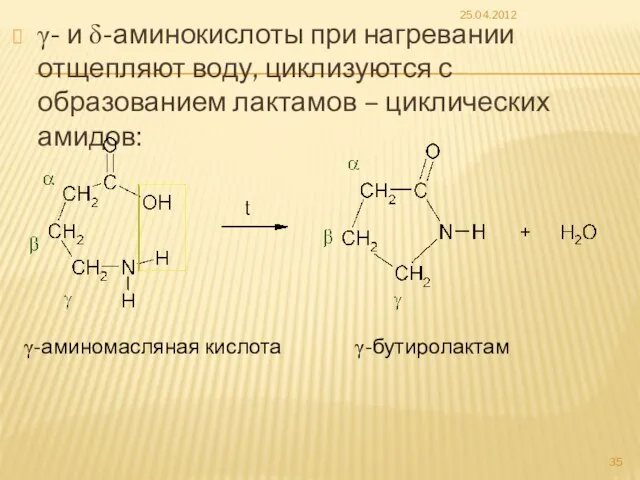
- 35. γ- и δ-аминокислоты при нагревании отщепляют воду, циклизуются с образованием лактамов – циклических амидов: 25.04.2012 γ-аминомасляная
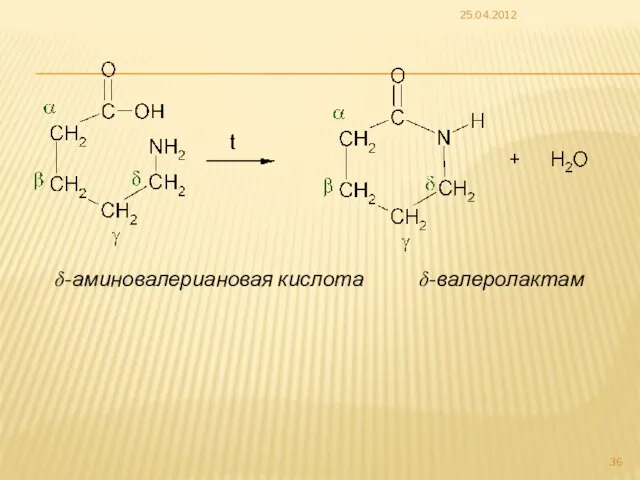
- 36. 25.04.2012 δ-аминовалериановая кислота δ-валеролактам
- 37. 7. Получение аминокислот 7.1. Выделение из белков и пептидов Белки гидролизуют в присутствии кислот (6 М
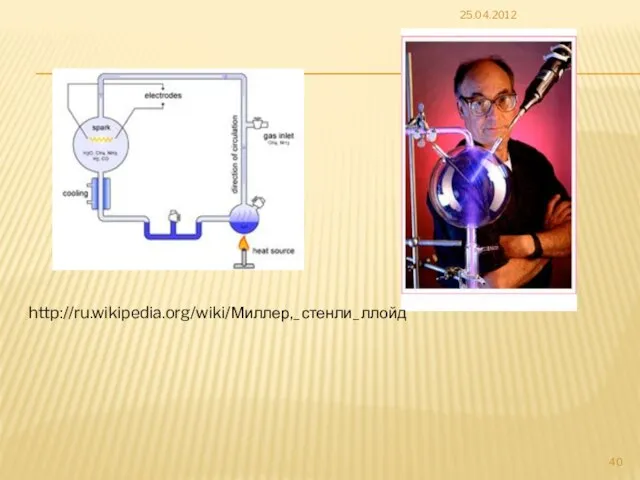
- 38. 7.3. Пребиотический (абиогенный) синтез аминокислот CH4, NH3, H2, H2O, HCN, H2S, CH2O УФ-излучение, электрический разряд, радиация
- 39. Proc Natl Acad Sci U S A. 2011 Apr 5;108(14):5526-31. Epub 2011 Mar 21. Primordial synthesis
- 40. 25.04.2012 http://ru.wikipedia.org/wiki/Миллер,_стенли_ллойд
- 41. Orig Life Evol Biosph. 2011 Apr 12. [Epub ahead of print] Catalytic effects of Murchison Material:
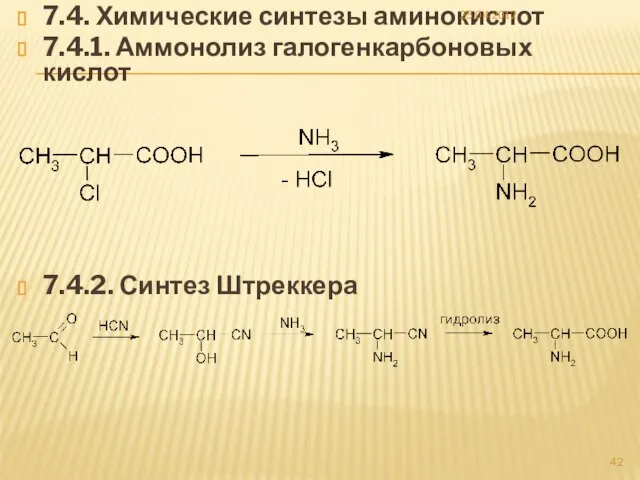
- 42. 7.4. Химические синтезы аминокислот 7.4.1. Аммонолиз галогенкарбоновых кислот 7.4.2. Синтез Штреккера 25.04.2012
- 43. ПЕПТИДЫ И БЕЛКИ Пептиды и белки - продукты поликонденсации аминокислот. Мr пептидов меньше 10000, у белков
- 44. ПЕПТИДЫ И БЕЛКИ Пептиды (πεπτος - сваренный) – первоначально - продукты неполного гидролиза белков Белки –
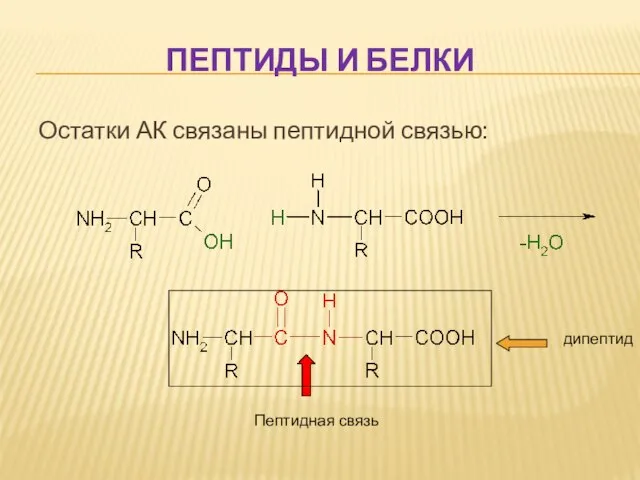
- 45. ПЕПТИДЫ И БЕЛКИ Остатки АК связаны пептидной связью: Пептидная связь дипептид
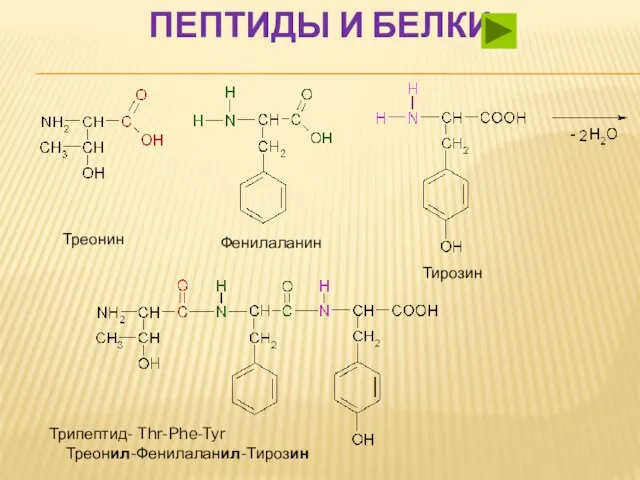
- 46. ПЕПТИДЫ И БЕЛКИ Треонин Фенилаланин Тирозин Трипептид- Thr-Phe-Tyr Треонил-Фенилаланил-Тирозин
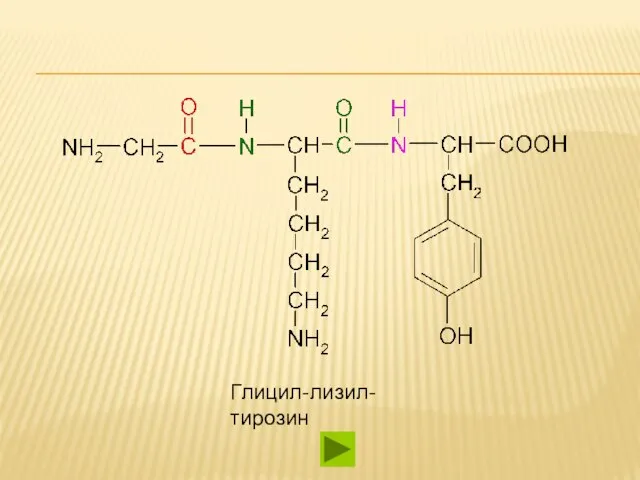
- 47. Глицил-лизил-тирозин
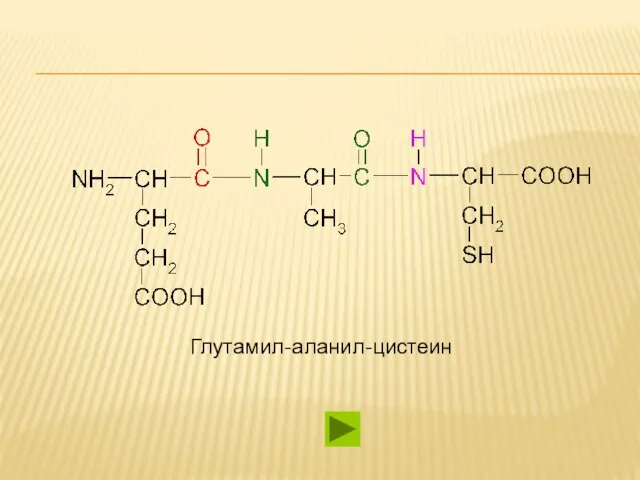
- 48. Глутамил-аланил-цистеин
- 49. ПЕПТИДНАЯ СВЯЗЬ Пространственное строение 1. Все атомы находятся в одной плоскости 2. Почти всегда атомы водорода
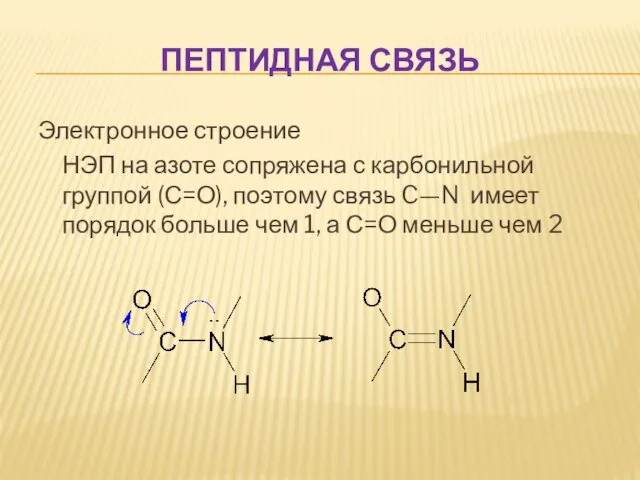
- 50. ПЕПТИДНАЯ СВЯЗЬ Электронное строение НЭП на азоте сопряжена с карбонильной группой (С=О), поэтому связь C—N имеет
- 51. ПЕПТИДЫ И БЕЛКИ Как и аминокислоты, пептиды и белки являются амфотерными соединениями, содержащими и кислотные группы
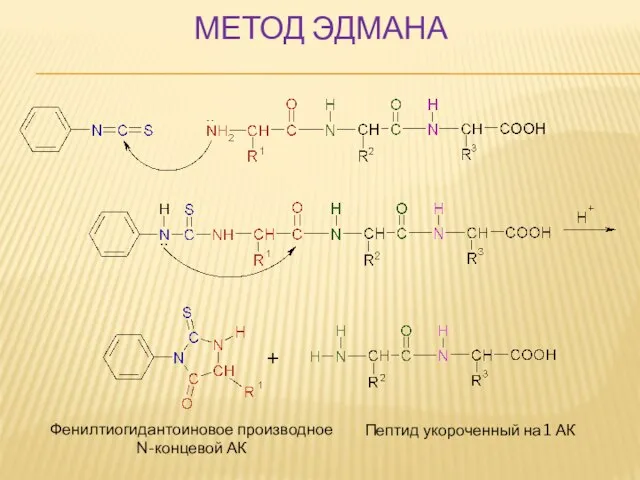
- 52. АНАЛИЗ ПЕРВИЧНОЙ СТРУКТУРЫ ПЕПТИДОВ МЕТОД ЭДМАНА Используя фенилизотиоцианат (Ph-NCS) последовательно отщепляют АК с N-конца и определяют
- 53. МЕТОД ЭДМАНА Фенилтиогидантоиновое производное N-концевой АК Пептид укороченный на 1 АК
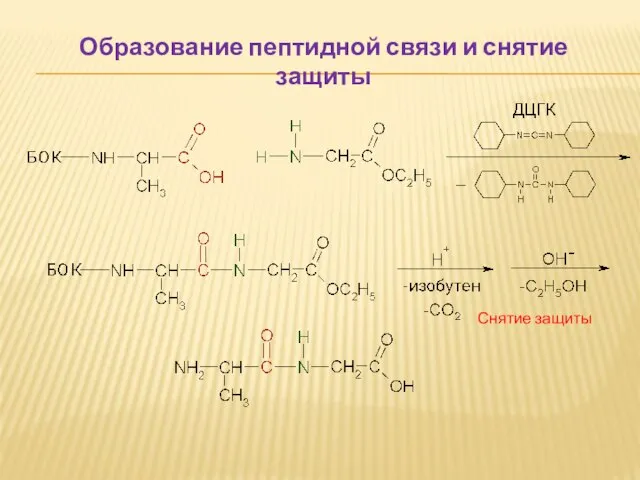
- 54. СИНТЕЗ ПЕПТИДОВ И БЕЛКОВ Защита аминогруппы (БОК-защита) Защита карбоксильной группы (образование сложных эфиров) Образование пептидной связи
- 55. Снятие защиты Образование пептидной связи и снятие защиты
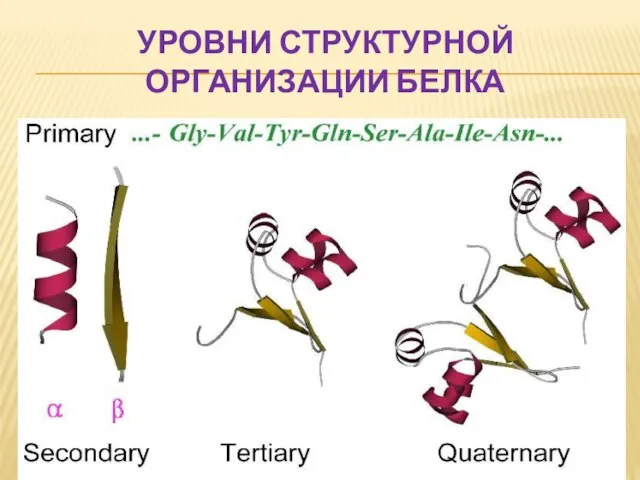
- 56. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА первичная структура – аминокислотная последовательность вторичная структура – локальные высокоупорядоченные конформации белковой
- 57. УРОВНИ СТРУКТУРНОЙ ОРГАНИЗАЦИИ БЕЛКА
- 58. ПЕРВИЧНАЯ СТРУКТУРА первичная структура –последовательность аминокислотных остатков в молекуле белка или пептида. NH2-Tyr-Pro-Lys-Gly-Phe-Tyr-Lys-COOH Первичная структура определяет
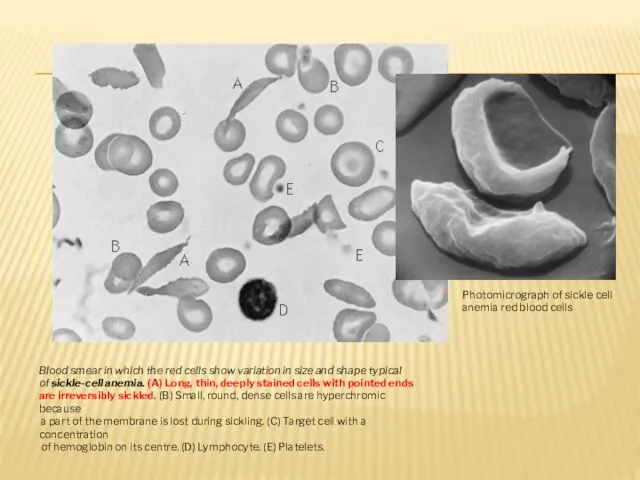
- 59. Blood smear in which the red cells show variation in size and shape typical of sickle-cell
- 60. Количество возможных первичных структур ОГРОМНО! 20 аминокислот могут дать примерно 100000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000000 белков, состоящих из 150 остатков
- 61. ВТОРИЧНАЯ СТРУКТУРА Вторичная структура- локальные высокоупорядоченные конформации белковой цепи – спирали и складчатые слои.
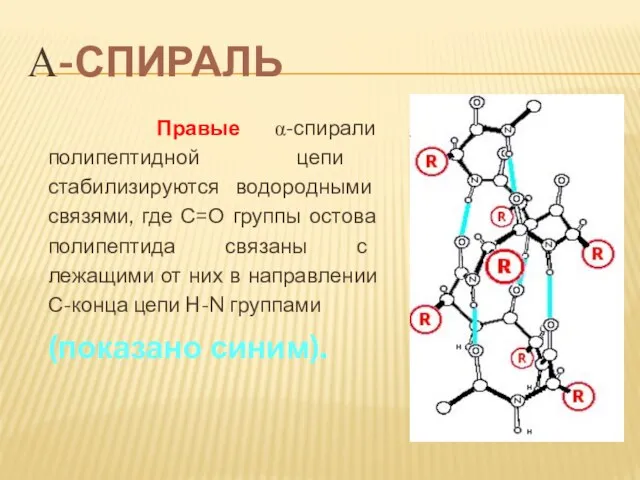
- 62. Α-СПИРАЛЬ Правые α-спирали полипептидной цепи стабилизируются водородными связями, где С=О группы остова полипептида связаны с лежащими
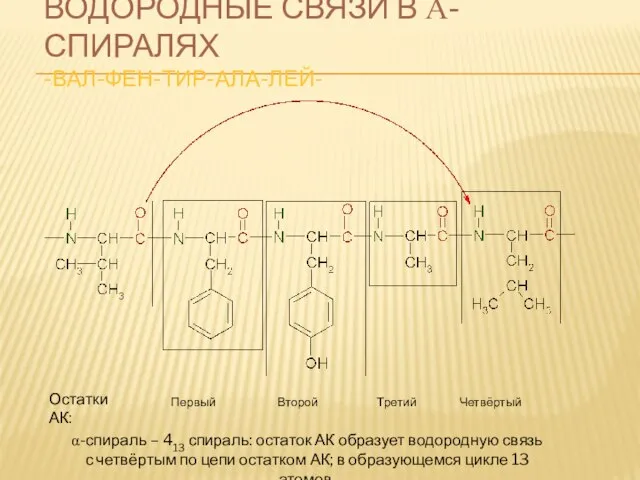
- 63. ВОДОРОДНЫЕ СВЯЗИ В Α-СПИРАЛЯХ -ВАЛ-ФЕН-ТИР-АЛА-ЛЕЙ- Первый Второй Третий Четвёртый Остатки АК: α-спираль – 413 спираль: остаток
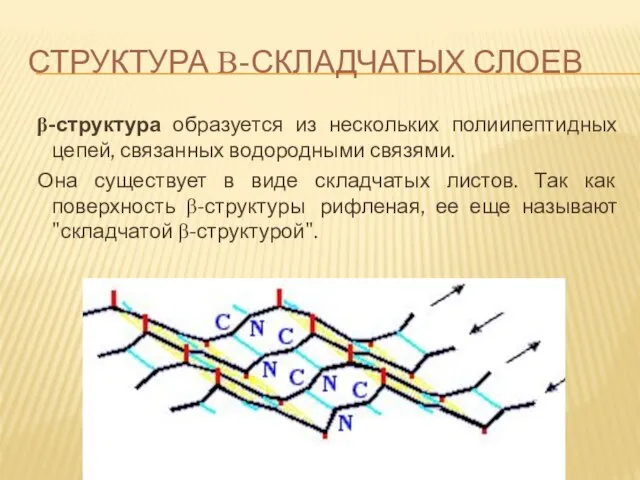
- 64. СТРУКТУРА Β-СКЛАДЧАТЫХ СЛОЕВ β-структура образуется из нескольких полиипептидных цепей, связанных водородными связями. Она существует в виде
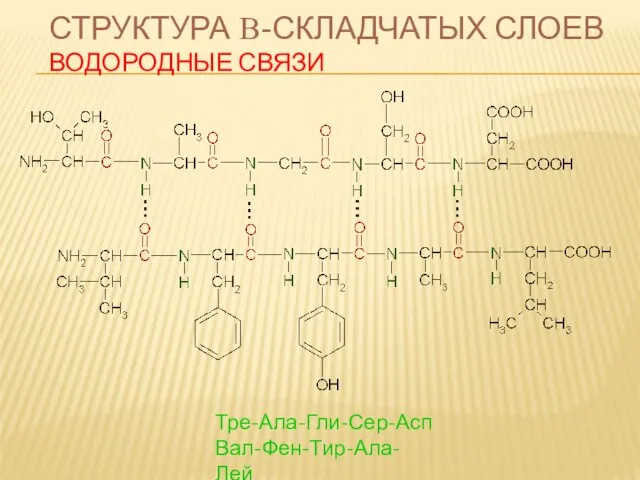
- 65. СТРУКТУРА Β-СКЛАДЧАТЫХ СЛОЕВ ВОДОРОДНЫЕ СВЯЗИ Тре-Ала-Гли-Сер-Асп Вал-Фен-Тир-Ала-Лей
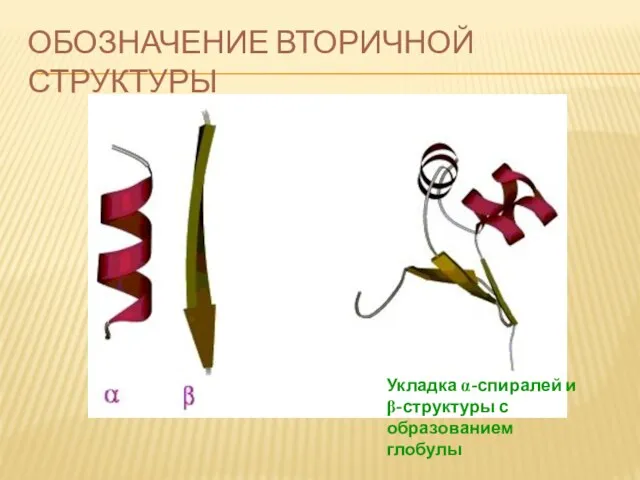
- 66. ОБОЗНАЧЕНИЕ ВТОРИЧНОЙ СТРУКТУРЫ Укладка α-спиралей и β-структуры с образованием глобулы
- 67. ТРЕТИЧНАЯ СТРУКТУРА третичная структура – форма белковой молекулы; трёхмерная структура белка. Укладка нерегулярных областей и α
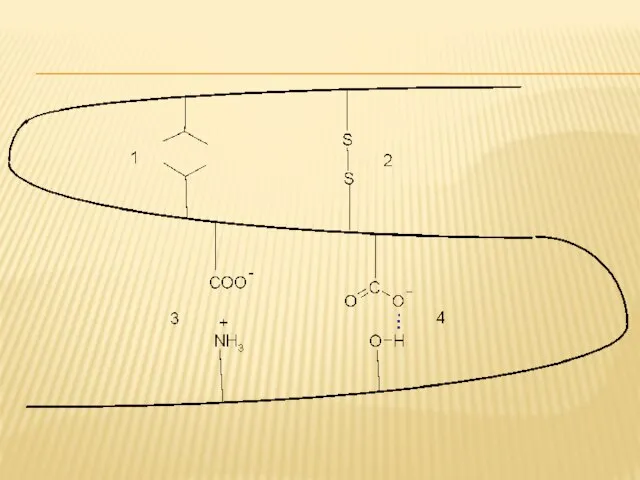
- 68. ВЗАИМОДЕЙСТВИЯ ОСТАТКОВ АК В ТРЕТИЧНОЙ СТРУКТУРЕ Остатки АК в белковой глобуле взаимодействуют за счёт: Гидрофобных взаимодействий
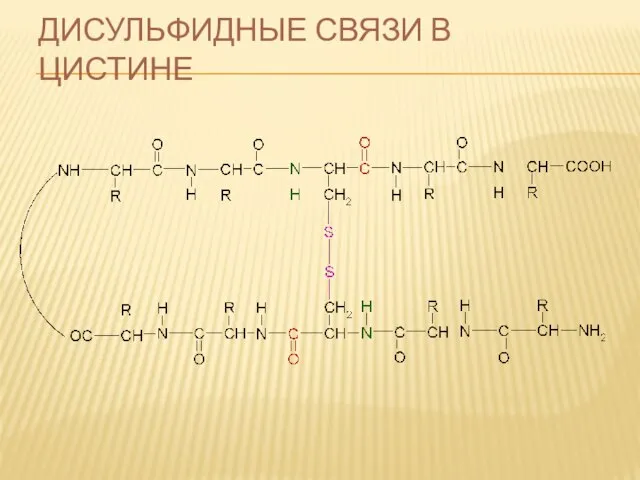
- 70. ДИСУЛЬФИДНЫЕ СВЯЗИ В ЦИСТИНЕ
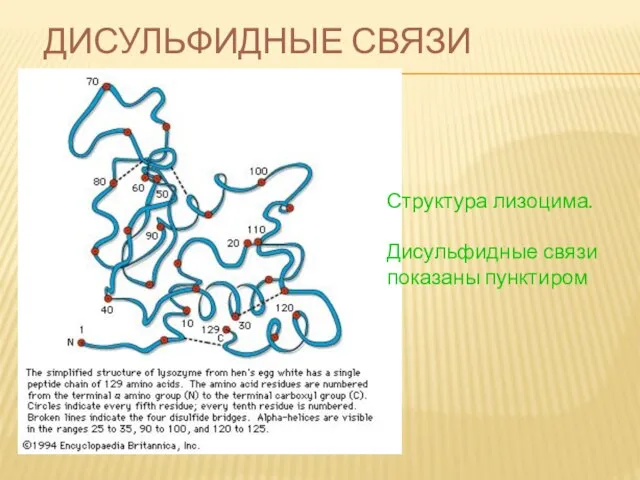
- 71. ДИСУЛЬФИДНЫЕ СВЯЗИ Структура лизоцима. Дисульфидные связи показаны пунктиром
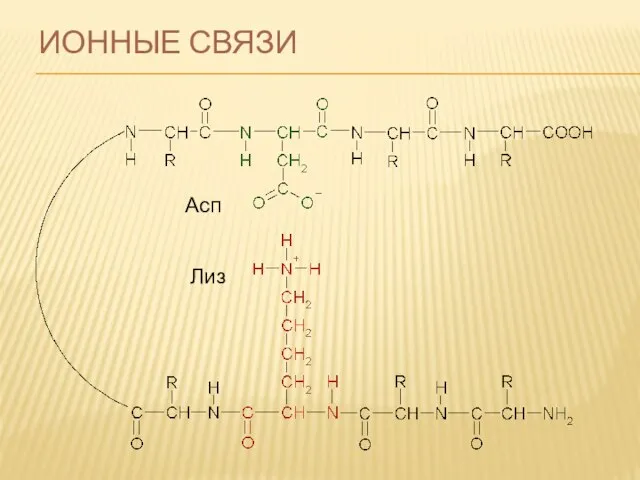
- 72. ИОННЫЕ СВЯЗИ Асп Лиз
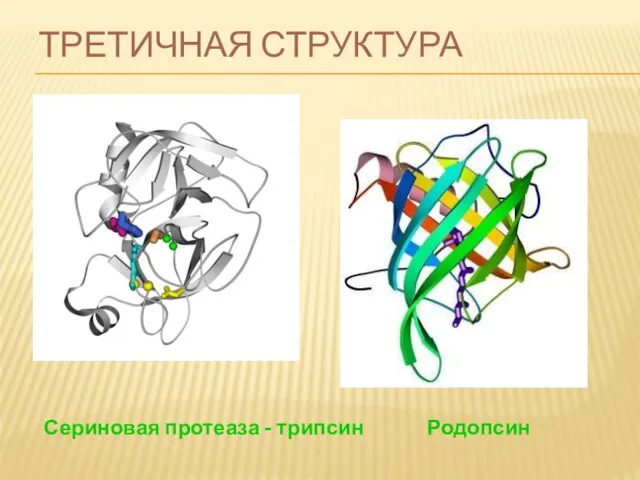
- 73. ТРЕТИЧНАЯ СТРУКТУРА Сериновая протеаза - трипсин Родопсин
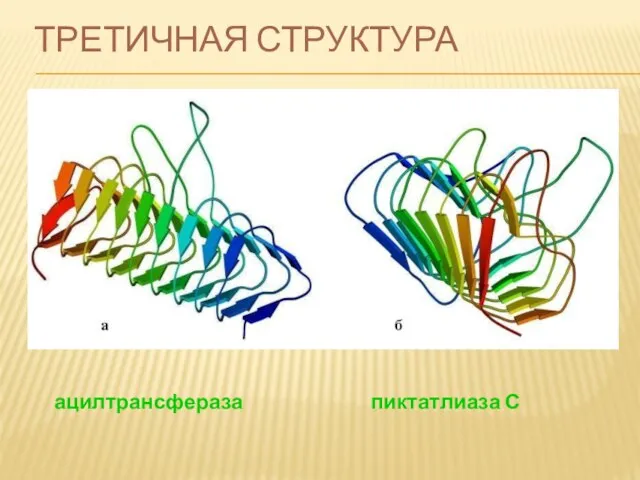
- 74. ТРЕТИЧНАЯ СТРУКТУРА ацилтрансфераза пиктатлиаза С
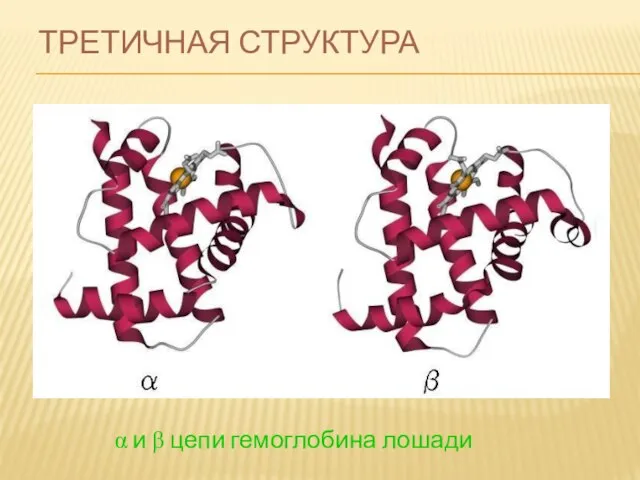
- 75. ТРЕТИЧНАЯ СТРУКТУРА α и β цепи гемоглобина лошади
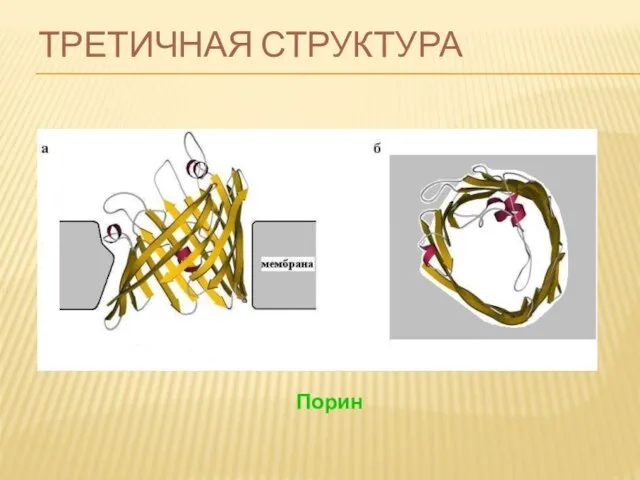
- 76. ТРЕТИЧНАЯ СТРУКТУРА Порин
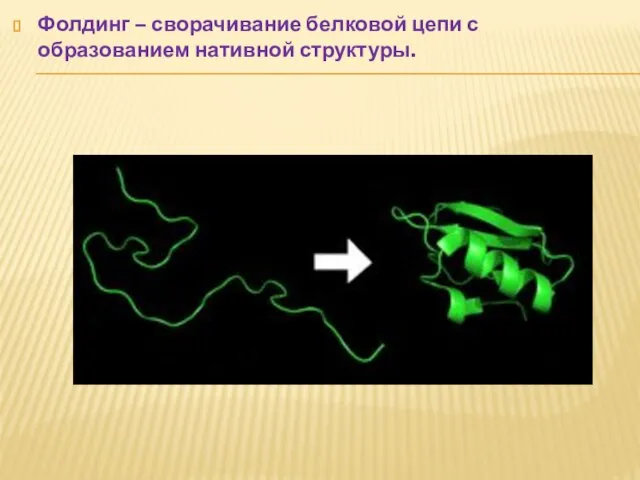
- 77. Фолдинг – сворачивание белковой цепи с образованием нативной структуры.
- 78. Неправильный фолдинг может привести к различным болезням, например к губчатым энцефалопатиям: Синдром Крейцфельда-Якоба Новый вариант Крейцфельда-Якоба
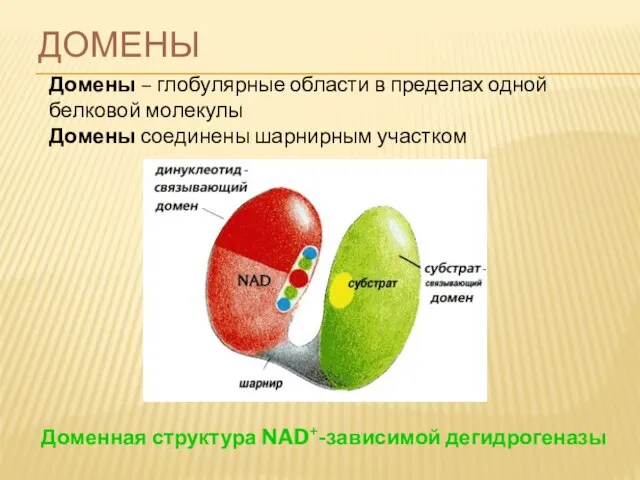
- 79. ДОМЕНЫ Домены – глобулярные области в пределах одной белковой молекулы Домены соединены шарнирным участком Доменная структура
- 80. ЧЕТВЕРТИЧНАЯ СТРУКТУРА Четвертичная структура- агрегат нескольких белковых молекул образующих одну структуру Взаимодействия: ионные, водородные, гидрофобные, ковалентные
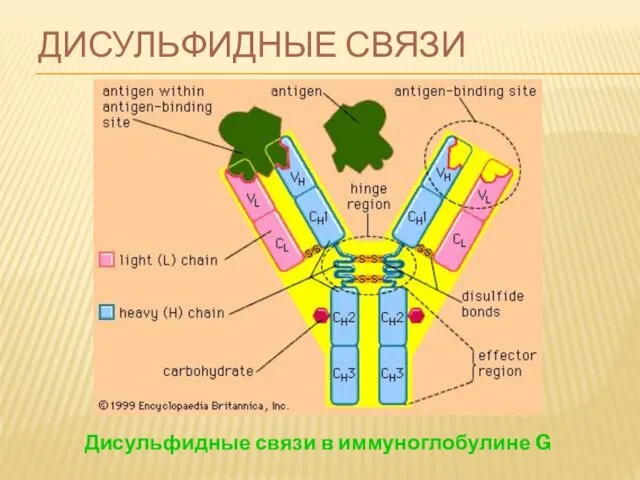
- 81. ДИСУЛЬФИДНЫЕ СВЯЗИ Дисульфидные связи в иммуноглобулине G
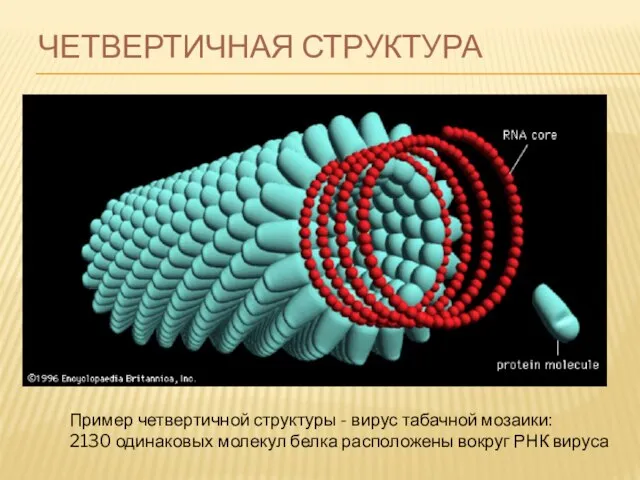
- 82. ЧЕТВЕРТИЧНАЯ СТРУКТУРА Пример четвертичной структуры - вирус табачной мозаики: 2130 одинаковых молекул белка расположены вокруг РНК
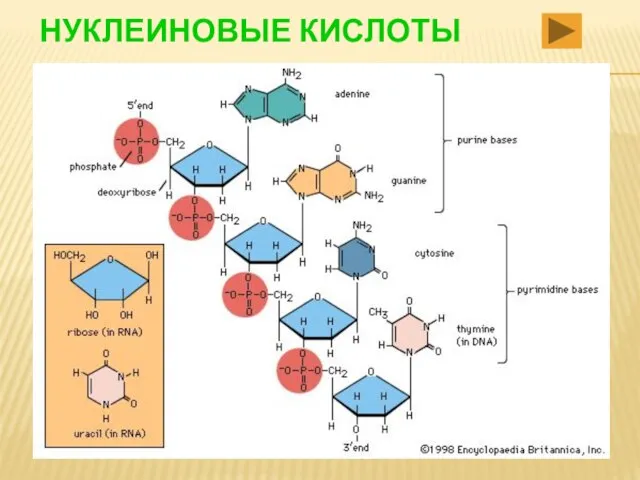
- 83. НУКЛЕИНОВЫЕ КИСЛОТЫ НК- это полинуклеотиды, т.е. биополимеры, мономерами которых являются нуклеотиды. Нуклеотиды-фосфорные эфиры нуклеозидов Нуклеозиды –
- 84. НУКЛЕИНОВЫЕ КИСЛОТЫ
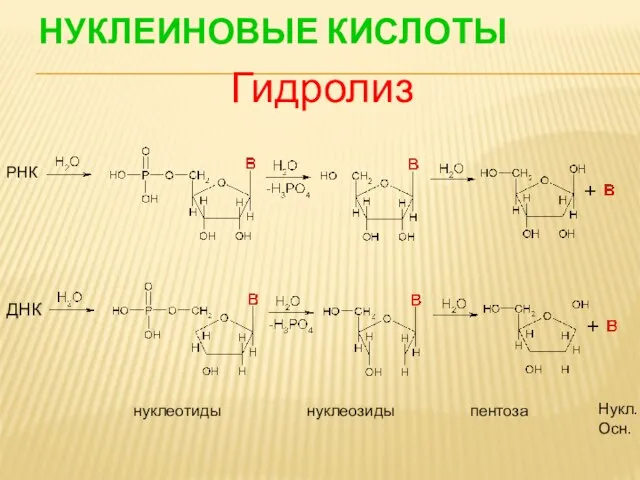
- 85. НУКЛЕИНОВЫЕ КИСЛОТЫ РНК ДНК нуклеотиды нуклеозиды пентоза Нукл. Осн. Гидролиз
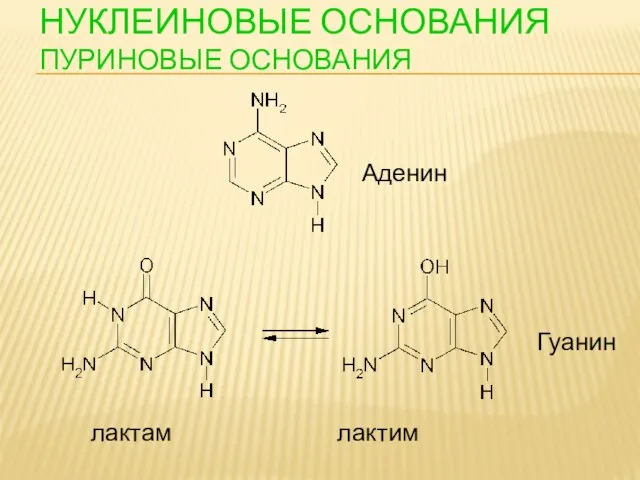
- 86. НУКЛЕИНОВЫЕ ОСНОВАНИЯ ПУРИНОВЫЕ ОСНОВАНИЯ Аденин Гуанин лактам лактим
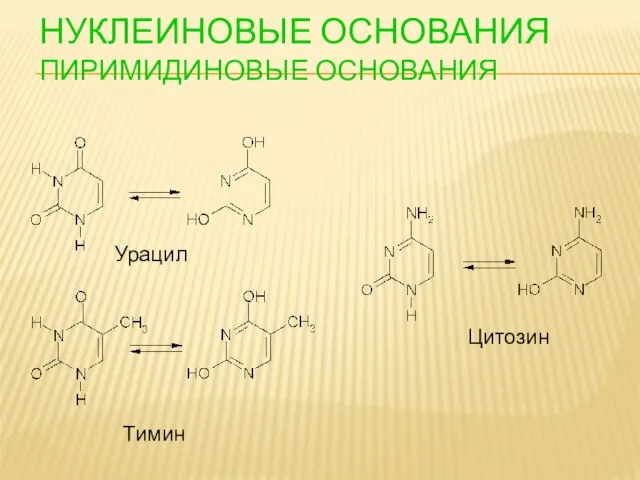
- 87. НУКЛЕИНОВЫЕ ОСНОВАНИЯ ПИРИМИДИНОВЫЕ ОСНОВАНИЯ Урацил Тимин Цитозин
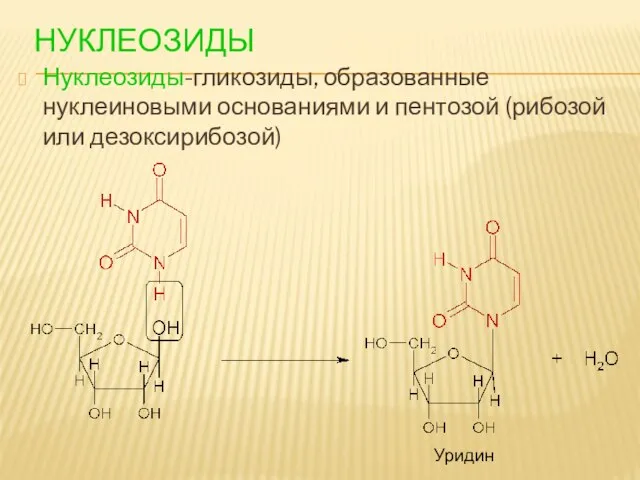
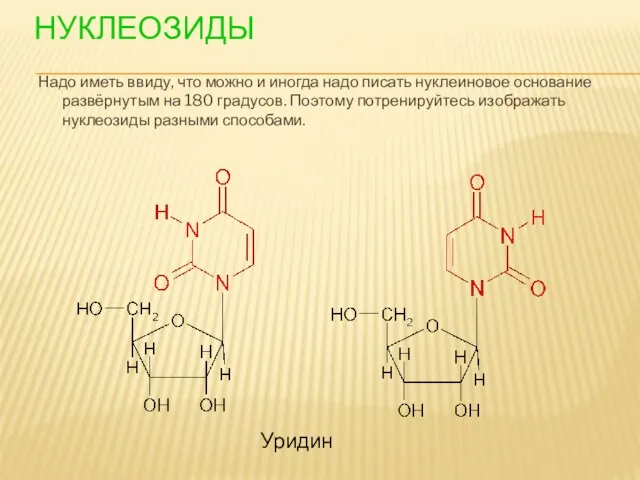
- 88. НУКЛЕОЗИДЫ Нуклеозиды-гликозиды, образованные нуклеиновыми основаниями и пентозой (рибозой или дезоксирибозой) Уридин
- 89. НУКЛЕОЗИДЫ Надо иметь ввиду, что можно и иногда надо писать нуклеиновое основание развёрнутым на 180 градусов.
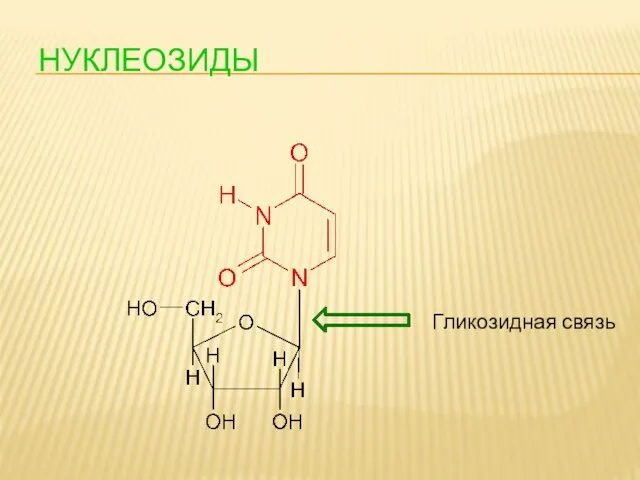
- 90. НУКЛЕОЗИДЫ Гликозидная связь
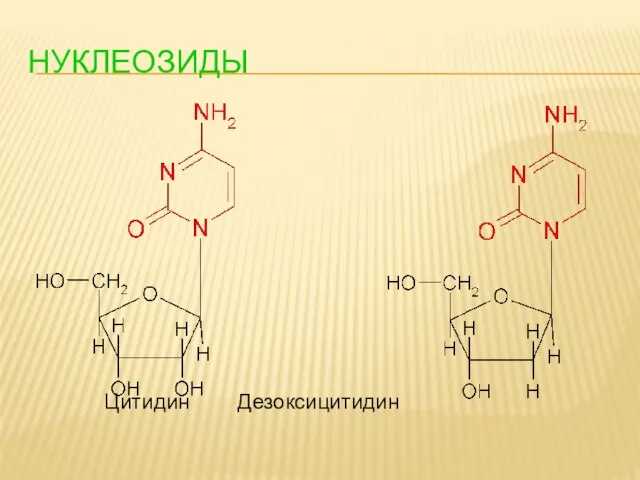
- 91. НУКЛЕОЗИДЫ Цитидин Дезоксицитидин
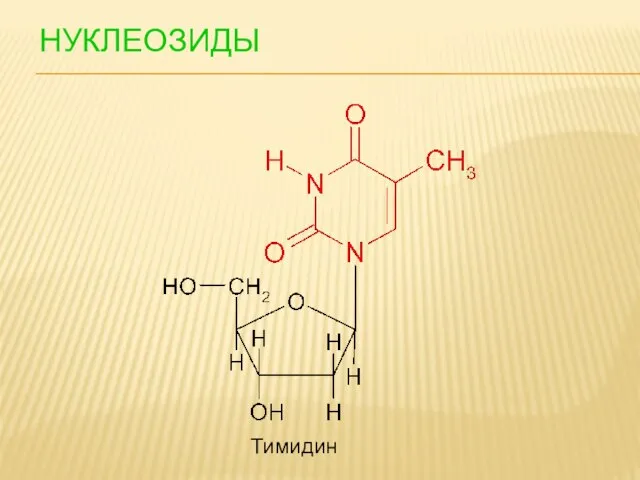
- 92. НУКЛЕОЗИДЫ Тимидин
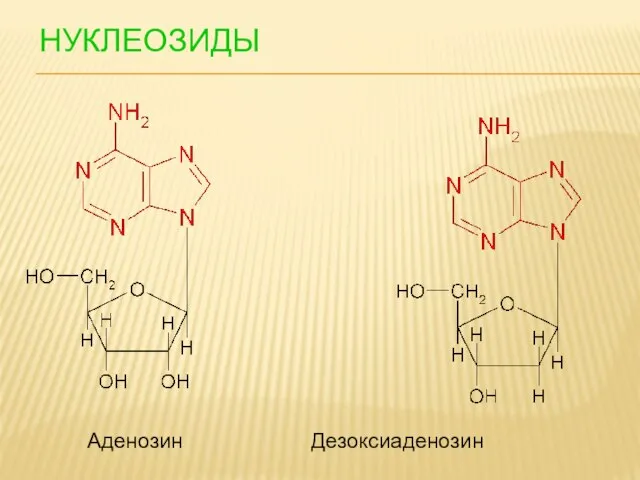
- 93. НУКЛЕОЗИДЫ Аденозин Дезоксиаденозин
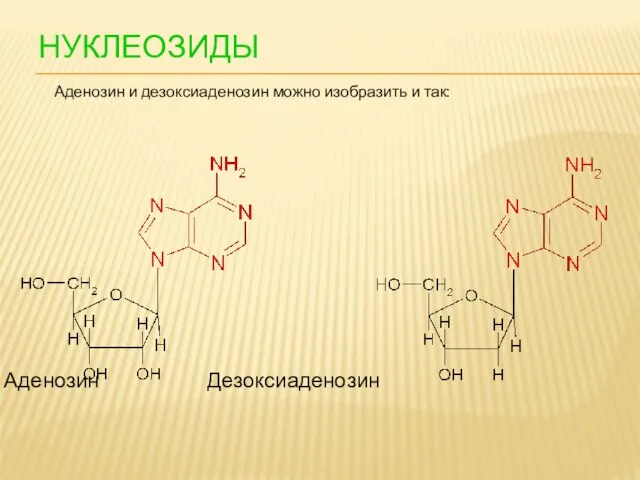
- 94. НУКЛЕОЗИДЫ Аденозин Дезоксиаденозин Аденозин и дезоксиаденозин можно изобразить и так:
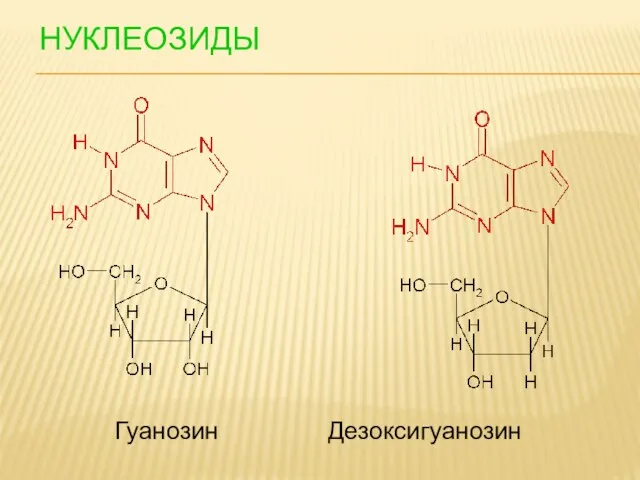
- 95. НУКЛЕОЗИДЫ Гуанозин Дезоксигуанозин
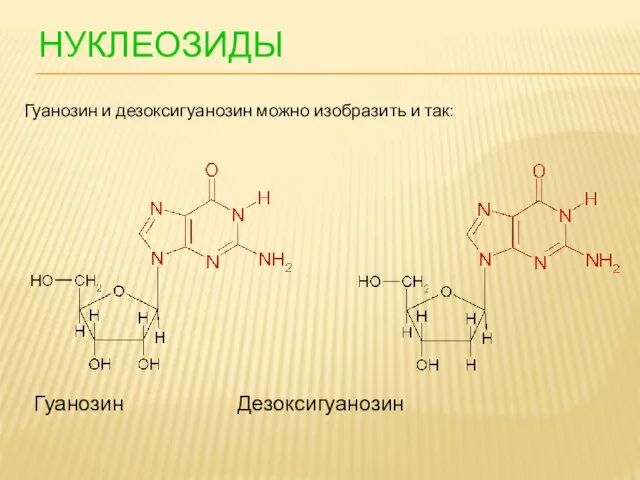
- 96. НУКЛЕОЗИДЫ Гуанозин Дезоксигуанозин Гуанозин и дезоксигуанозин можно изобразить и так:
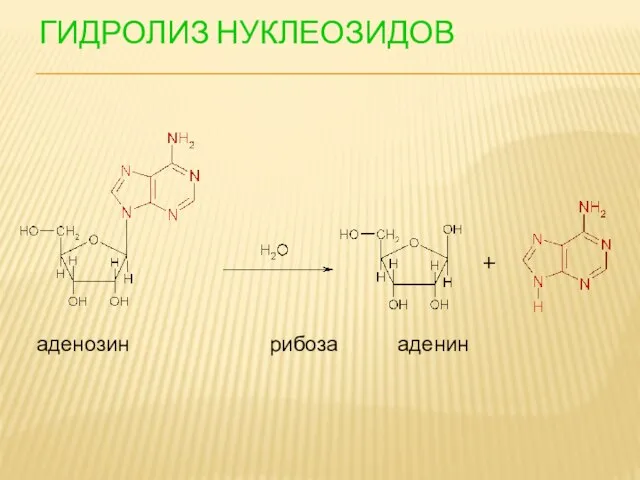
- 97. ГИДРОЛИЗ НУКЛЕОЗИДОВ аденозин рибоза аденин
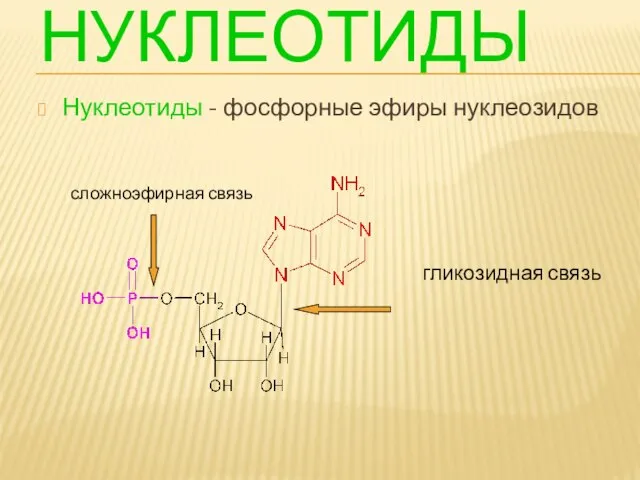
- 98. НУКЛЕОТИДЫ Нуклеотиды - фосфорные эфиры нуклеозидов гликозидная связь сложноэфирная связь
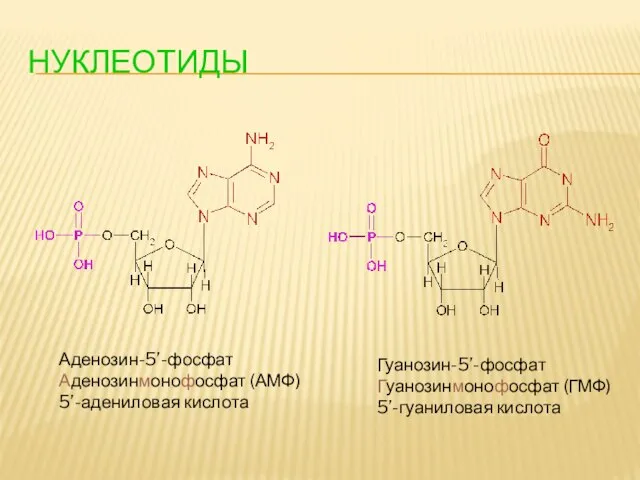
- 99. НУКЛЕОТИДЫ Аденозин-5’-фосфат Аденозинмонофосфат (АМФ) 5’-адениловая кислота Гуанозин-5’-фосфат Гуанозинмонофосфат (ГМФ) 5’-гуаниловая кислота
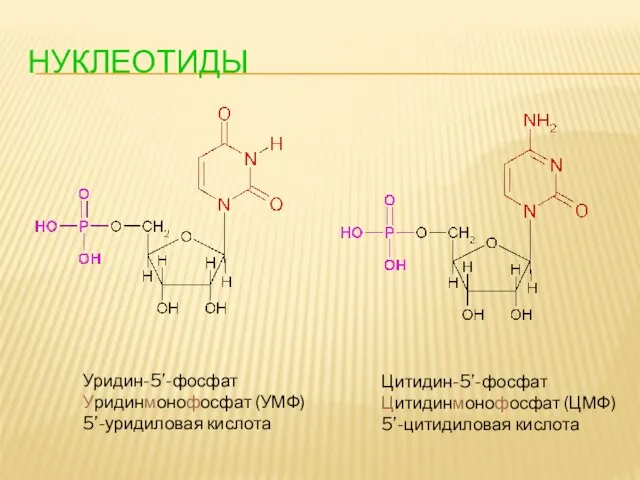
- 100. НУКЛЕОТИДЫ Уридин-5’-фосфат Уридинмонофосфат (УМФ) 5’-уридиловая кислота Цитидин-5’-фосфат Цитидинмонофосфат (ЦМФ) 5’-цитидиловая кислота
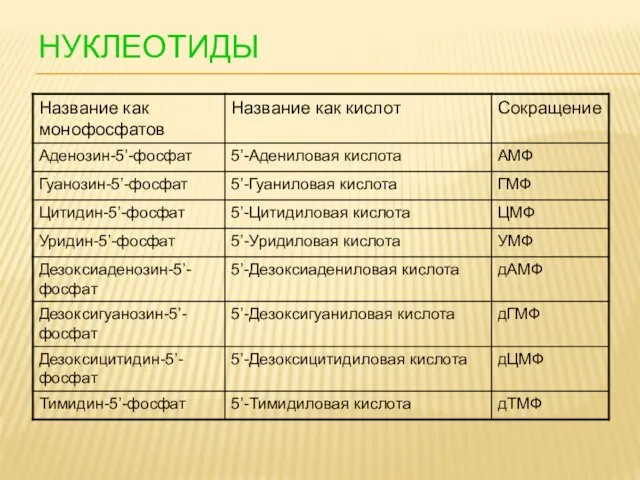
- 101. НУКЛЕОТИДЫ
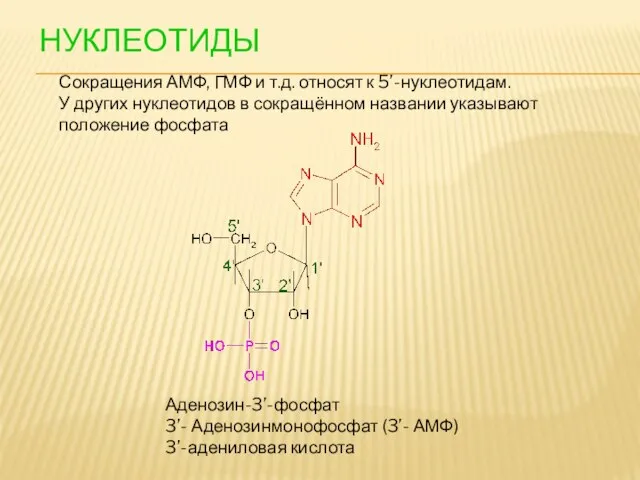
- 102. НУКЛЕОТИДЫ Сокращения АМФ, ГМФ и т.д. относят к 5’-нуклеотидам. У других нуклеотидов в сокращённом названии указывают
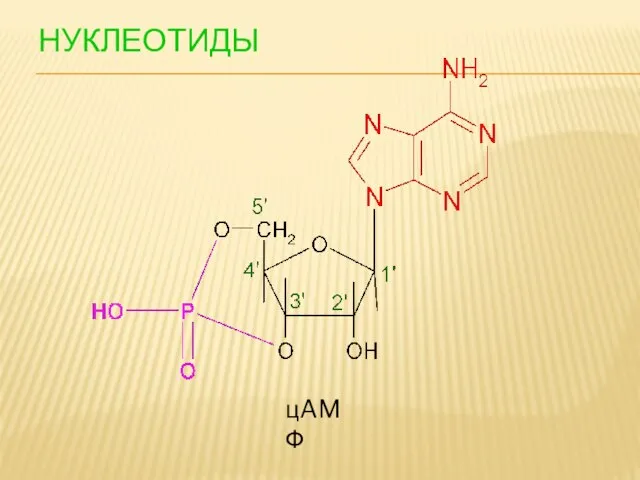
- 103. НУКЛЕОТИДЫ цAMФ
- 104. Циклический аденозинмонофосфат (циклический AMФ, цAMФ, cAMP) — Циклический нуклеотид, играющий роль вторичного посредника некоторых гормонов (глюкагона
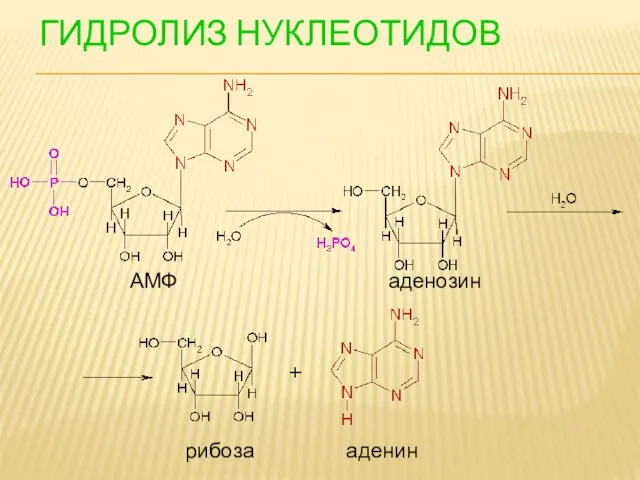
- 105. ГИДРОЛИЗ НУКЛЕОТИДОВ АМФ аденозин рибоза аденин
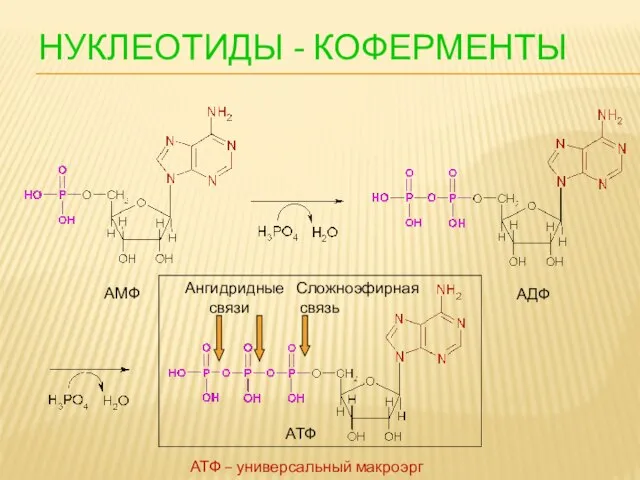
- 106. НУКЛЕОТИДЫ - КОФЕРМЕНТЫ АМФ АДФ АТФ Ангидридные связи Сложноэфирная связь АТФ – универсальный макроэрг
- 107. Образование АТФ происходит 1. В результате субстратного фосфорилирования (гликолиз, одна реакция ЦТК) 2. Окислительное фосфорилирование (в
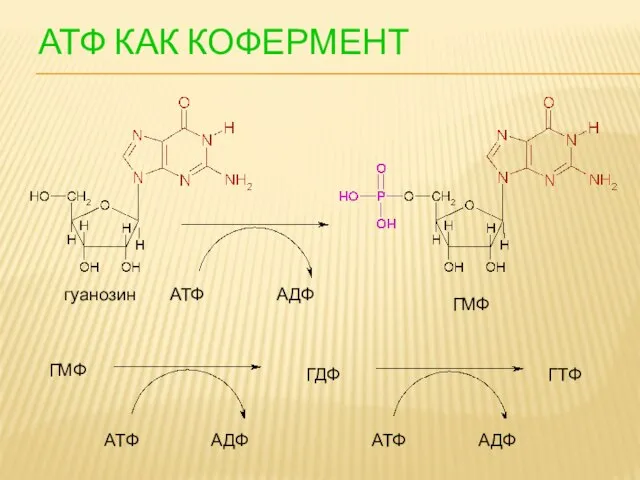
- 108. АТФ КАК КОФЕРМЕНТ АТФ АДФ АТФ АДФ АТФ АДФ ГМФ ГДФ ГТФ ГМФ гуанозин
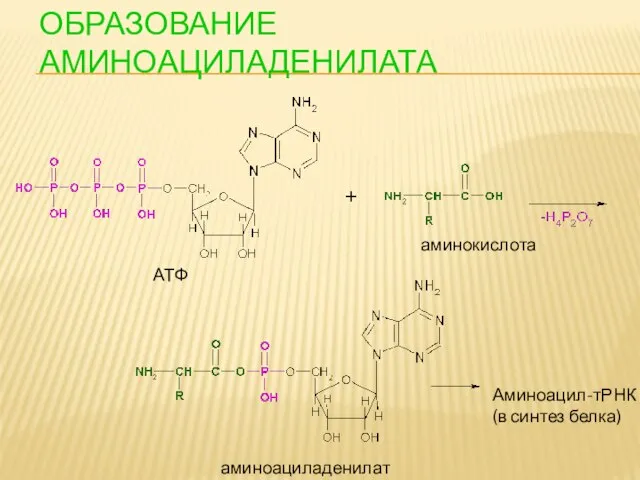
- 109. ОБРАЗОВАНИЕ АМИНОАЦИЛАДЕНИЛАТА АТФ аминокислота аминоациладенилат Аминоацил-тРНК (в синтез белка)
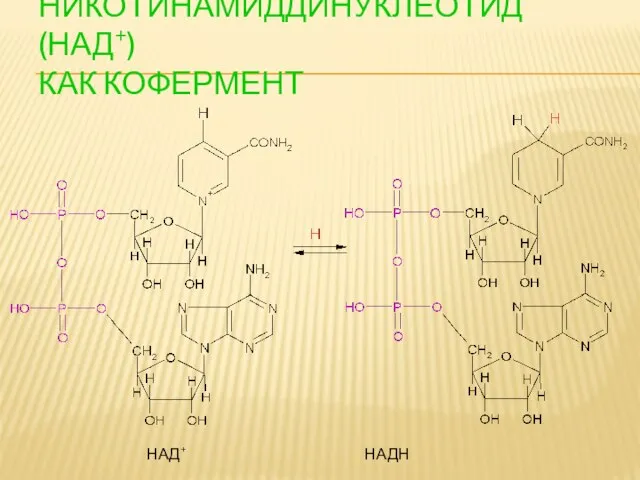
- 110. НИКОТИНАМИДДИНУКЛЕОТИД (НАД+) КАК КОФЕРМЕНТ НАД+ НАДН
- 111. ПЕРВИЧНАЯ СТРУКТУРА НК Первичная структура НК - последовательность нуклеотидов 5’- конец ТГАЦТААГТАЦЦ 3’-конец (ф-конец) (OH-конец)
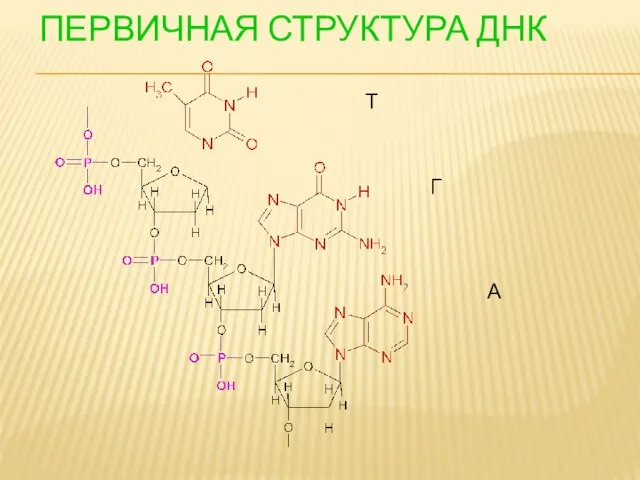
- 112. ПЕРВИЧНАЯ СТРУКТУРА ДНК Т Г А
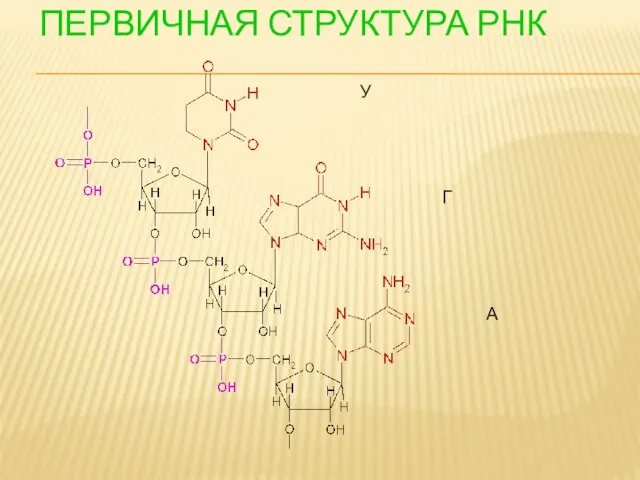
- 113. ПЕРВИЧНАЯ СТРУКТУРА РНК У Г А
- 114. ВТОРИЧНАЯ СТРУКТУРА Вторичная структура ДНК – двойная правая спираль (Уотсон, Крик, 1953) Две цепи антипараллельны друг
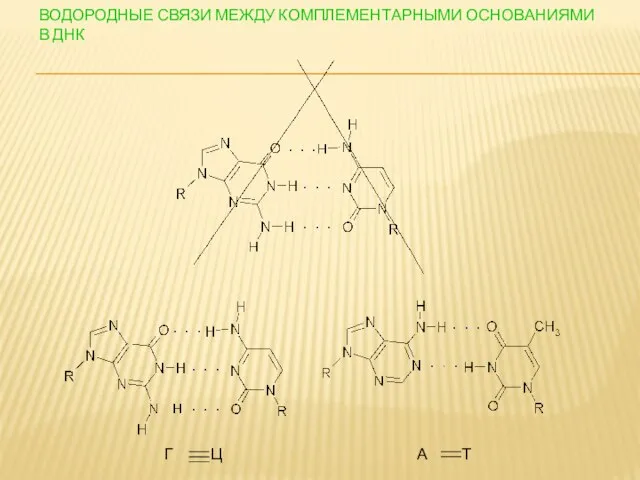
- 115. ВОДОРОДНЫЕ СВЯЗИ МЕЖДУ КОМПЛЕМЕНТАРНЫМИ ОСНОВАНИЯМИ В ДНК Г Ц А Т
- 117. Скачать презентацию





![СОДЕРЖАЩИЕ АМИНОГРУППУ Лизин α,ε-диаминокапроновая кислота 2,6-диаминогексановая кислота Lys, Лиз Аргинин α-амино-δ-гуанидилвалериановая кислота 2-амино-5-[амино(имино)метил]аминопентановая к-та Arg, Арг](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/426661/slide-9.jpg)













![Orig Life Evol Biosph. 2011 Apr 12. [Epub ahead of print] Catalytic](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/426661/slide-40.jpg)



















 [email protected]_2022-08-30_14-56-25
[email protected]_2022-08-30_14-56-25 Заповеди любви
Заповеди любви Коэффициент
Коэффициент Длина окружности и площадь круга математика 6 класс
Длина окружности и площадь круга математика 6 класс Дом Теплова
Дом Теплова Белоруссия 1941-1944гг
Белоруссия 1941-1944гг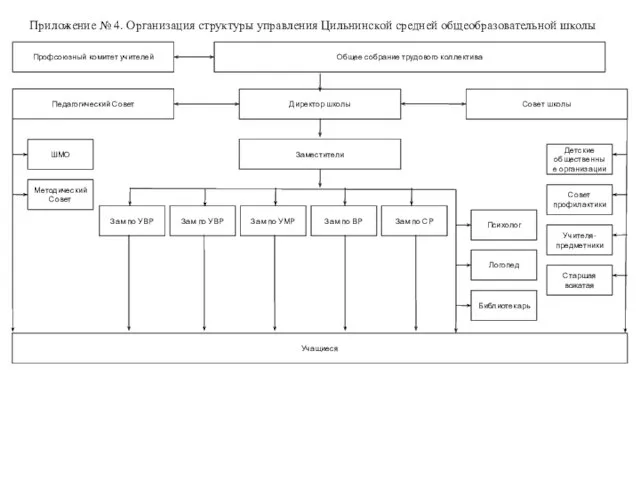 Приложение № 4. Организация структуры управления Цильнинской средней общеобразовательной школы
Приложение № 4. Организация структуры управления Цильнинской средней общеобразовательной школы Презентация на тему Мамонты
Презентация на тему Мамонты  Счастливая жизнь - международный образовательный проект
Счастливая жизнь - международный образовательный проект Перспективы теплофикации в современных условиях
Перспективы теплофикации в современных условиях Подготовила: Кальчик Лариса Александровна педагог Мбдоу №26 «солнышко» г. Старый оскол
Подготовила: Кальчик Лариса Александровна педагог Мбдоу №26 «солнышко» г. Старый оскол перфект
перфект Как выбрать шубу?
Как выбрать шубу? Представители наших секторов помогут тебе в решении проблем
Представители наших секторов помогут тебе в решении проблем Привычки
Привычки Цвет в одежде и интерьере, и его влияние на окружающую среду
Цвет в одежде и интерьере, и его влияние на окружающую среду Английский язык в мини - группах
Английский язык в мини - группах Право и организация социального обеспечения
Право и организация социального обеспечения Легка промисловість України
Легка промисловість України Николай Андреевич Римский-Корсаков
Николай Андреевич Римский-Корсаков Подключение типовых узлов ввода/вывода для однокристальных микроконтроллеров
Подключение типовых узлов ввода/вывода для однокристальных микроконтроллеров Лущение почвы
Лущение почвы Mechanism of action of supatret 0.04% gel - ogm
Mechanism of action of supatret 0.04% gel - ogm Опорный прыжок. 1 часть
Опорный прыжок. 1 часть Содержание теории трудовой стоимости и предельной полезности
Содержание теории трудовой стоимости и предельной полезности Русская классика на экране
Русская классика на экране Отчет по практике: ознакомительная с профессиональной деятельностью. Учебная практика
Отчет по практике: ознакомительная с профессиональной деятельностью. Учебная практика Презентация на тему Особая экономическая зона
Презентация на тему Особая экономическая зона