Содержание
- 2. Биохимия находится на стыке нескольких наук, прежде всего - биологии - биологии и химии. Возникнув как
- 3. Что такое жизнь? С точки зрения философии жизнь нужно рассматривать как особую форму движения материи, отличающуюся
- 4. Чем представлены информационно-генетические программы живых организмов? Они представлены нуклеиновыми кислотами, но, чтобы поддерживать и тем более
- 5. За счет чего существуют живые системы (организмы)? За счет обмена веществ и энергии с окружающей средой,
- 6. Поэтому биохимия охватывает многие области клеточной биологииПоэтому биохимия охватывает многие области клеточной биологии и включает в
- 7. Место биохимии в медицине Провести четкие границы между биохимией и смежными науками, такими, как биология клетки,
- 8. История становления биохимии Как самостоятельная наука биохимия сформировалась примерно 100 лет назад, однако биохимические процессы люди
- 9. Биохимия в средневековье ТалантливыйТалантливый арабскийТалантливый арабский учёныйТалантливый арабский учёный и врачТалантливый арабский учёный и врач X
- 10. Биохимия в посленьютоновское время XVIII векXVIII век ознаменовался гениальными трудами М. В. ЛомоносоваXVIII век ознаменовался гениальными
- 11. Становление биохимии как науки из достижений органической химии В 1828 году В 1828 году немецкий химик
- 12. Зарождение энзимологии и химии белка Новый толчок развитию биологической химии дали работы по изучению брожения, инициированные
- 13. Биохимия начала ХХ века Биохимия стала первой биологической дисциплиной с развитым математическим аппаратом благодаря работам ХолдейнаБиохимия
- 14. Открытие биоинформационных молекул В 1928 г. Фредерик ГриффитВ 1928 г. Фредерик Гриффит впервые показал, что экстракт
- 15. Развитие биохимической методологии В основе биохимической методологии лежит фракционирование, анализ, изучение структуры и свойств отдельных компонентов
- 16. Биохимия и молекулярная генетика С конца ХХ в. в биохимии все шире применяются методы молекулярнойС конца
- 17. Биохимия сегодня В настоящее время основные проблемы, разрешаемые биохимией – это связь между строением и биологической
- 18. Перспективы развития биохимии Основная масса ферментов была открыта биохимиками в середине XX века, и к концу
- 19. Основные разделы биохимии Статическая биохимия – изучение химической природы и свойств компонентов клеток. Динамическая биохимия –
- 20. С чего начать? Начнём с химического состава организма. Элементы, обычно входящие в состав организма называют биогенными
- 21. Биогенные элементы - биоэлементы Поскольку многие биомолекулы помимо Н, О, С и N содержат также атомы
- 22. БИОМОЛЕКУЛЫ Подавляющее большинство биомолекул является производными более простых соединений биоэлементов-органогенов: Н, О, С, N, S, P.
- 23. Макромолекулы - биополимеры К макромолекулам-биополимерам относятся белки, нуклеиновые кислоты, высшие изопреноиды (каучуки), полисахариды, характеризующиеся достигаемой в
- 24. Белки как биополимеры Белки это биополимеры, образованные из альфа-аминокислот, соединенных пептидной (амидной) связью. В живых организмах
- 25. Биологические функции аминокислот
- 26. Стереохимия аминокислот
- 27. Буферные свойства аминокислот
- 28. Протеиногенные (канонические) аминокислоты Протеиногенными (каноническими) называются 20 α-аминокислот, которые кодируются генетическим кодом и включение которых в
- 29. Алифатические и серосодержащие аминокислоты
- 30. Аминокислоты ароматические, нейтральные и иминокислоты
- 31. Нейтральные, кислые и основные аминокислоты
- 32. Пептидная связь
- 33. Конформация полипептидной цепи
- 34. Сравнение первичных структур гистонов Н4 методом выравнивания
- 35. Многообразие белков
- 36. Классификация белков Белки делятся на простые и сложные. Простые белки при гидролизе распадаются только до аминокислот,
- 37. Первичная и вторичная структура инсулина
- 38. Основные типы спиралей полипептидной цепи
- 39. Складчатые – β-структуры
- 40. Повороты полипептидной цепи
- 41. Фолдинг и рефолдинг протеинов
- 42. Третичные структуры
- 43. Инсулин третичная и четвертичная структура
- 44. Структурные белки: коллаген и кератин
- 45. Особенности структуры гемоглобина
- 47. Скачать презентацию
Слайд 2Биохимия находится на стыке нескольких наук, прежде всего - биологии - биологии
Биохимия находится на стыке нескольких наук, прежде всего - биологии - биологии

Возникнув как наука о химии жизни в конце XIX век, чему предшествовало бурное развитие органической химии, биохимия отличается от органической химии тем, что исследует только те вещества и химические реакции, которые имеют место в живых организмах, прежде всего в живой клетке. Попробуем определиться в понятиях: живой, жизнь.
Слайд 3Что такое жизнь?
С точки зрения философии жизнь нужно рассматривать как особую форму
Что такое жизнь?
С точки зрения философии жизнь нужно рассматривать как особую форму

Слайд 4Чем представлены информационно-генетические программы живых организмов?
Они представлены нуклеиновыми кислотами, но, чтобы поддерживать
Чем представлены информационно-генетические программы живых организмов?
Они представлены нуклеиновыми кислотами, но, чтобы поддерживать

Слайд 5За счет чего существуют живые системы (организмы)?
За счет обмена веществ и энергии
За счет чего существуют живые системы (организмы)?
За счет обмена веществ и энергии

для извлечения энергии при распаде органических веществ, затрачивая которую живые организмы синтезируют необходимые для своего существования сложные органические соединения, в том числе и биоинформационные молекулы
Слайд 6Поэтому биохимия охватывает многие области клеточной биологииПоэтому биохимия охватывает многие области клеточной
Поэтому биохимия охватывает многие области клеточной биологииПоэтому биохимия охватывает многие области клеточной

После выделения последней в особую дисциплину, размежевание между биохимией и молекулярной биологией в основном сформировалось как методологическое и по предмету исследования. Молекулярные биологи преимущественно работают с нуклеиновыми кислотамиПосле выделения последней в особую дисциплину, размежевание между биохимией и молекулярной биологией в основном сформировалось как методологическое и по предмету исследования. Молекулярные биологи преимущественно работают с нуклеиновыми кислотами, изучая их структуру и функции, в то время как биохимики сосредоточились на белкахПосле выделения последней в особую дисциплину, размежевание между биохимией и молекулярной биологией в основном сформировалось как методологическое и по предмету исследования. Молекулярные биологи преимущественно работают с нуклеиновыми кислотами, изучая их структуру и функции, в то время как биохимики сосредоточились на белках, в особенности на ферментах, катализирующих биохимические реакции.
Слайд 7Место биохимии в медицине
Провести четкие границы между биохимией и смежными науками, такими,
Место биохимии в медицине
Провести четкие границы между биохимией и смежными науками, такими,

Слайд 8История становления биохимии
Как самостоятельная наука биохимия сформировалась примерно 100 лет назад, однако
История становления биохимии
Как самостоятельная наука биохимия сформировалась примерно 100 лет назад, однако

Слайд 9Биохимия в средневековье
ТалантливыйТалантливый арабскийТалантливый арабский учёныйТалантливый арабский учёный и врачТалантливый арабский учёный
Биохимия в средневековье
ТалантливыйТалантливый арабскийТалантливый арабский учёныйТалантливый арабский учёный и врачТалантливый арабский учёный

Зародилось направление иатрохимия. Иатрохимия — направление в науке 16-17 вв., представители которого стремились поставить химию на службу медицине, исследуя различные вещества как возможные лекарства и изучая составы живого.
Великий итальянский учёный и художникВеликий итальянский учёный и художник Леонардо да ВинчиВеликий итальянский учёный и художник Леонардо да Винчи на основании интереснейших опытов сделал важный вывод о том, что живой организм способен существовать только в такой атмосфереВеликий итальянский учёный и художник Леонардо да Винчи на основании интереснейших опытов сделал важный вывод о том, что живой организм способен существовать только в такой атмосфере, в которой может горетьВеликий итальянский учёный и художник Леонардо да Винчи на основании интереснейших опытов сделал важный вывод о том, что живой организм способен существовать только в такой атмосфере, в которой может гореть пламя.
Слайд 10Биохимия в посленьютоновское время
XVIII векXVIII век ознаменовался гениальными трудами М. В. ЛомоносоваXVIII
Биохимия в посленьютоновское время
XVIII векXVIII век ознаменовался гениальными трудами М. В. ЛомоносоваXVIII

Изучение химии жизни уже в 1827 г. привело к принятому до сих пор разделению биологических молекул на белкиИзучение химии жизни уже в 1827 г. привело к принятому до сих пор разделению биологических молекул на белки, жирыИзучение химии жизни уже в 1827 г. привело к принятому до сих пор разделению биологических молекул на белки, жиры и углеводыИзучение химии жизни уже в 1827 г. привело к принятому до сих пор разделению биологических молекул на белки, жиры и углеводы. Автором этой классификации был известный английский химик и врач Уильям Праут.
Слайд 11Становление биохимии как науки из достижений органической химии
В 1828 году В
Становление биохимии как науки из достижений органической химии
В 1828 году В

Слайд 12Зарождение энзимологии и химии белка
Новый толчок развитию биологической химии дали работы по
Зарождение энзимологии и химии белка
Новый толчок развитию биологической химии дали работы по

Слайд 13Биохимия начала ХХ века
Биохимия стала первой биологической дисциплиной с развитым математическим аппаратом
Биохимия начала ХХ века
Биохимия стала первой биологической дисциплиной с развитым математическим аппаратом

Открытие ферментов позволило начать грандиозную работу по полному описанию всех процессов метаболизмаОткрытие ферментов позволило начать грандиозную работу по полному описанию всех процессов метаболизма, не завершенную до сих пор. Одними из первых значительных находок в этой области стали открытия витаминовОткрытие ферментов позволило начать грандиозную работу по полному описанию всех процессов метаболизма, не завершенную до сих пор. Одними из первых значительных находок в этой области стали открытия витаминов, гликолизаОткрытие ферментов позволило начать грандиозную работу по полному описанию всех процессов метаболизма, не завершенную до сих пор. Одними из первых значительных находок в этой области стали открытия витаминов, гликолиза и цикла трикарбоновых кислот.
Слайд 14Открытие биоинформационных молекул
В 1928 г. Фредерик ГриффитВ 1928 г. Фредерик Гриффит впервые
Открытие биоинформационных молекул
В 1928 г. Фредерик ГриффитВ 1928 г. Фредерик Гриффит впервые

В 1953 году В 1953 году американский биолог Дж. Уотсон В 1953 году американский биолог Дж. Уотсон и английский физик Ф. Крик В 1953 году американский биолог Дж. Уотсон и английский физик Ф. Крик описали структуру ДНК В 1953 году американский биолог Дж. Уотсон и английский физик Ф. Крик описали структуру ДНК — ключ к пониманию принципов передачи наследственной информации В 1953 году американский биолог Дж. Уотсон и английский физик Ф. Крик описали структуру ДНК — ключ к пониманию принципов передачи наследственной информации. Это открытие означало рождение нового направления науки — молекулярной биологии.
Слайд 15Развитие биохимической методологии
В основе биохимической методологии лежит фракционирование, анализ, изучение структуры и
Развитие биохимической методологии
В основе биохимической методологии лежит фракционирование, анализ, изучение структуры и

Слайд 16Биохимия и молекулярная генетика
С конца ХХ в. в биохимии все шире применяются
Биохимия и молекулярная генетика
С конца ХХ в. в биохимии все шире применяются

Слайд 17Биохимия сегодня
В настоящее время основные проблемы, разрешаемые биохимией – это связь между
Биохимия сегодня
В настоящее время основные проблемы, разрешаемые биохимией – это связь между

Слайд 18Перспективы развития биохимии
Основная масса ферментов была открыта биохимиками в середине XX века,
Перспективы развития биохимии
Основная масса ферментов была открыта биохимиками в середине XX века,

Кроме того, чрезвычайно перспективны исследования молекулярных механизмов регуляции метаболизма и биоинженерное конструирование новых белков
Слайд 19Основные разделы биохимии
Статическая биохимия – изучение химической природы и свойств компонентов клеток.
Динамическая
Основные разделы биохимии
Статическая биохимия – изучение химической природы и свойств компонентов клеток.
Динамическая

Частная (функциональная) биохимия – изучение функционирования отдельных органов и тканей методами биохимии.
Слайд 20С чего начать? Начнём
с химического состава организма.
Элементы, обычно входящие в
С чего начать? Начнём
с химического состава организма.
Элементы, обычно входящие в

Н – главный в биохимии восстановитель, а протон (p) - закислитель среды; О – главный в живых системах окислитель;
С – не только основной структурный элемент, но и главный для живых организмов донатор энергии через окислительно-восстановительные реакции, реализуемые в кругообороте углерода;
N – необходимый составной компонент белков и биоинформационных молекул, придающий важное информационное разнообразие биополимерам.
Н и О – составные элементы воды, на которую приходится до 70% массы живых организмов, в том числе и наших с вами.
Слайд 21Биогенные элементы - биоэлементы
Поскольку многие биомолекулы помимо Н, О, С и N
Биогенные элементы - биоэлементы
Поскольку многие биомолекулы помимо Н, О, С и N

К макроэлементам относят также Na, К, Mg, Са, Cl, а также Fe, содержание которого достигает в живых организмах 0,05%.
Те биоэлементы, содержание которых составляет сотые доли процента и меньше называют микроэлементами, к которым относят Cu, Zn, I, Co, F, Br, Se, Mn, Mo.
К ультрамикроэлементам относят Li, B, Al, Si, V, Cr, Ni, содержание которых ниже тысячных долей процента.
Выделяют также следовые элементы – As, Au, Hg, Cd и другие. Значение многих ультрамикроэлементов и следовых элементов в настоящее время неизвестно.
Слайд 22БИОМОЛЕКУЛЫ
Подавляющее большинство биомолекул является производными более простых соединений биоэлементов-органогенов: Н, О, С,
БИОМОЛЕКУЛЫ
Подавляющее большинство биомолекул является производными более простых соединений биоэлементов-органогенов: Н, О, С,

На основе этих простых соединений путем замены атомов водорода на углеводородную группировку-R, и дальнейшего частичного окисления, дегидратации, поликонденсации и полимеризации образуется все многообразие органических молекул: амины, спирты, тиоспирты, дисульфиды, альдегиды, карбоновые кислоты, полуацетали, сложные эфиры, амиды карбоновых кислот, моно- и дизамещенные эфиры фосфорной кислоты, ангидриды, аминокислоты и т.д., с дальнейшим образованием макромолекул.
Слайд 23Макромолекулы - биополимеры
К макромолекулам-биополимерам относятся белки, нуклеиновые кислоты, высшие изопреноиды (каучуки), полисахариды,
Макромолекулы - биополимеры
К макромолекулам-биополимерам относятся белки, нуклеиновые кислоты, высшие изопреноиды (каучуки), полисахариды,

В последнее время к биополимерам стали относить также фосфолипидные комплексы, лежащие в основе структуры биомембран, также характеризующиеся высокой степенью регулярности и организации.
Слайд 24Белки как биополимеры
Белки это биополимеры, образованные из альфа-аминокислот, соединенных пептидной (амидной) связью.
Белки как биополимеры
Белки это биополимеры, образованные из альфа-аминокислот, соединенных пептидной (амидной) связью.

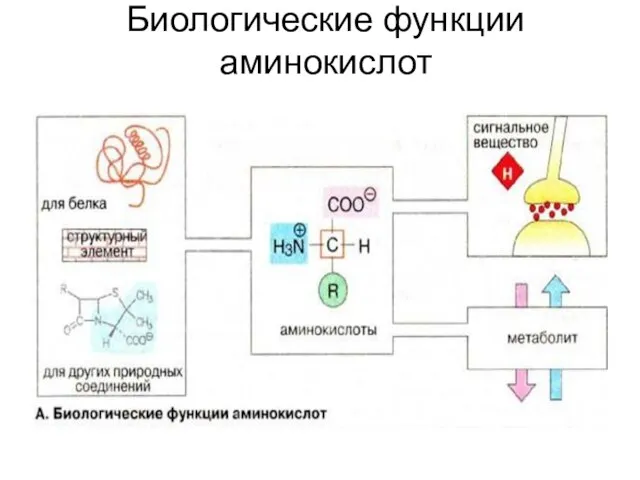
Аминокислоты в организме выполняют различные функции:
Аминокислоты структурные компоненты пептидов и белков и некоторых других соединений (коферментов, желчных кислот, фосфолипидов, антибиотиков).
Аминокислоты – переносчики сигналов (нейромедиаторы, предшественники гормонов, медиаторов и нейромедиаторов.
Аминокислоты – метаболиты, важнейшие компоненты питания, доноры азота.
Аминокислоты из которых синтезируются белки называются протеиногенными
Существуют также изопротеиногенные аминокислоты – это химически модифицированные протеиногенные аминок-ты, содержащиеся в в белках.
Слайд 25Биологические функции аминокислот
Биологические функции аминокислот
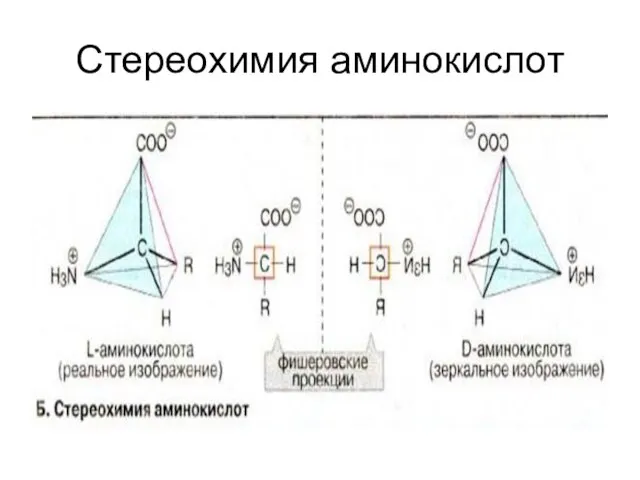
Слайд 26Стереохимия аминокислот
Стереохимия аминокислот
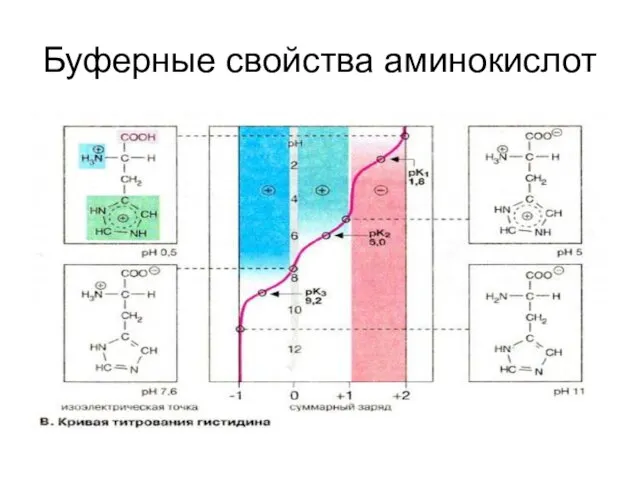
Слайд 27Буферные свойства аминокислот
Буферные свойства аминокислот
Слайд 28Протеиногенные (канонические) аминокислоты
Протеиногенными (каноническими) называются 20 α-аминокислот, которые кодируются генетическим кодом и
Протеиногенные (канонические) аминокислоты
Протеиногенными (каноническими) называются 20 α-аминокислот, которые кодируются генетическим кодом и

В настоящее время известна также минорная протеиногенная α-аминокислота селеноцистеин, входящая в состав некоторых ферментов-оксидоредуктаз.
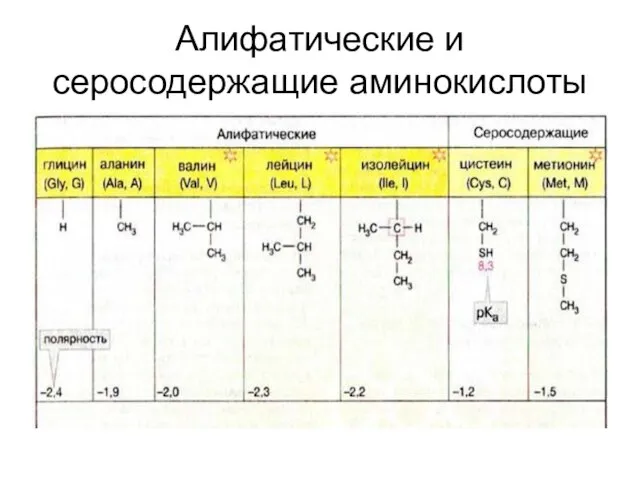
Слайд 29Алифатические и серосодержащие аминокислоты
Алифатические и серосодержащие аминокислоты
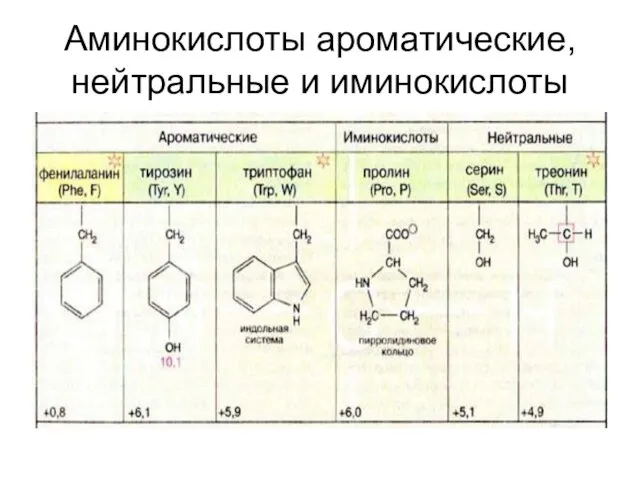
Слайд 30Аминокислоты ароматические, нейтральные и иминокислоты
Аминокислоты ароматические, нейтральные и иминокислоты
Слайд 31Нейтральные, кислые и основные аминокислоты
Нейтральные, кислые и основные аминокислоты

Слайд 32Пептидная связь
Пептидная связь
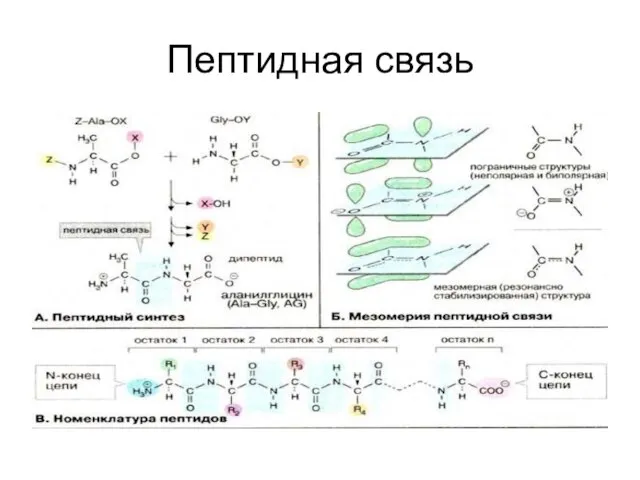
Слайд 33Конформация полипептидной цепи
Конформация полипептидной цепи
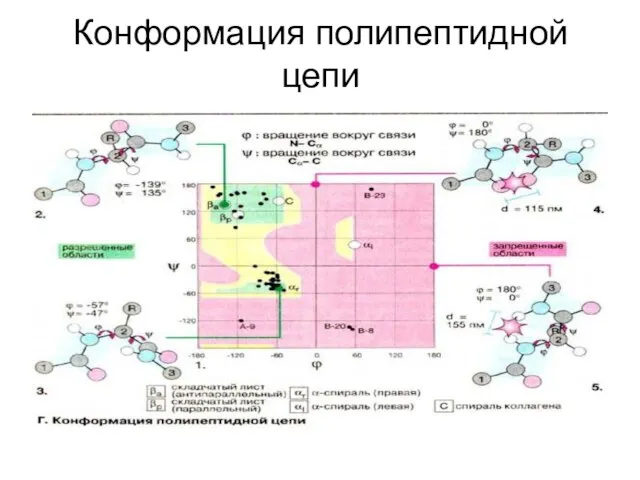
Слайд 34Сравнение первичных структур гистонов Н4 методом выравнивания
Сравнение первичных структур гистонов Н4 методом выравнивания
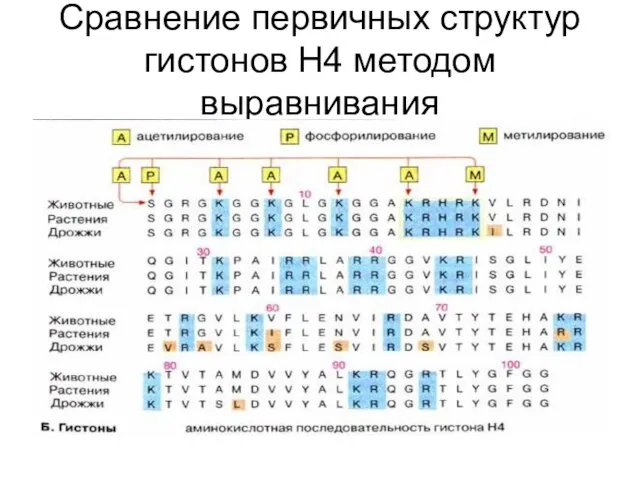
Слайд 35Многообразие белков
Многообразие белков
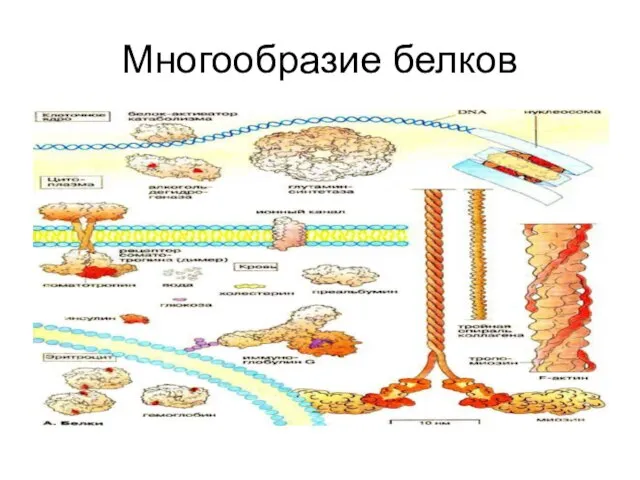
Слайд 36Классификация белков
Белки делятся на простые и сложные.
Простые белки при гидролизе распадаются только
Классификация белков
Белки делятся на простые и сложные.
Простые белки при гидролизе распадаются только

Особое положение занимают фосфопротеины и металлопротеины, при гидролизе которых наряду с аминокислотами освобождаются фосфорная кислота или ионы металлов, хотя их часто относят к сложным белкам
Простые белки делят на глобулярные и фибриллярные
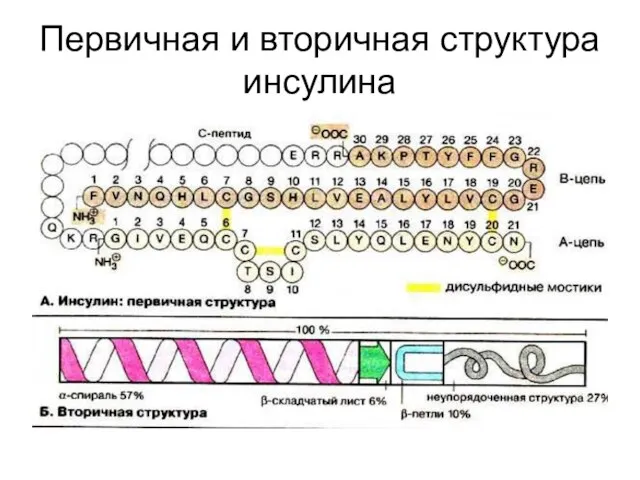
Слайд 37Первичная и вторичная структура инсулина
Первичная и вторичная структура инсулина
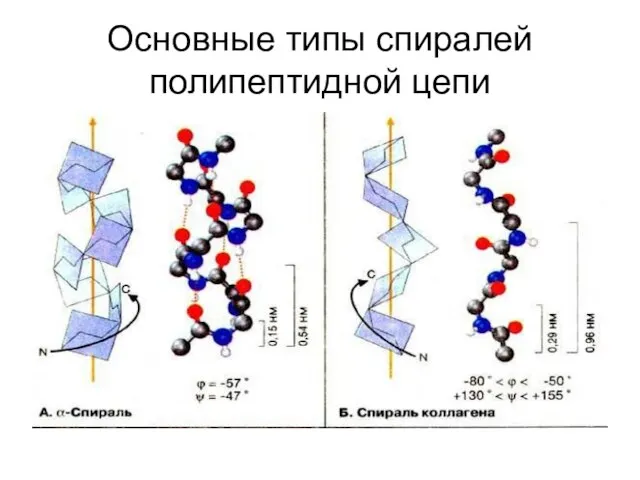
Слайд 38Основные типы спиралей полипептидной цепи
Основные типы спиралей полипептидной цепи
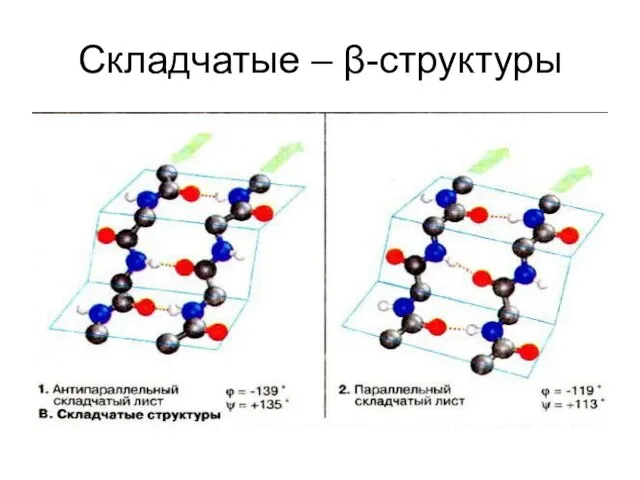
Слайд 39Складчатые – β-структуры
Складчатые – β-структуры
Слайд 40Повороты полипептидной цепи
Повороты полипептидной цепи
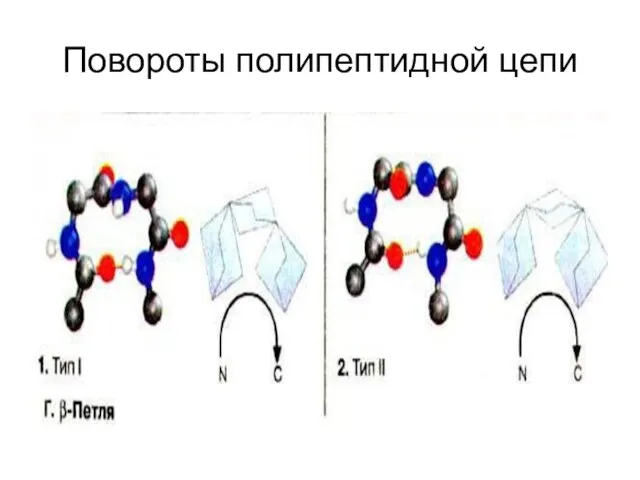
Слайд 41Фолдинг и рефолдинг протеинов
Фолдинг и рефолдинг протеинов
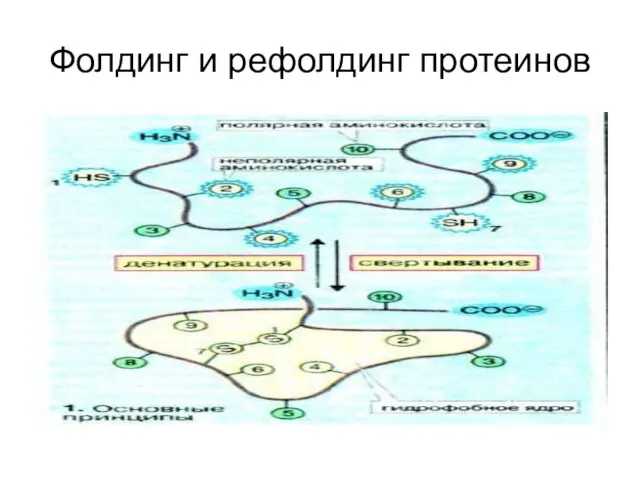
Слайд 42Третичные структуры
Третичные структуры
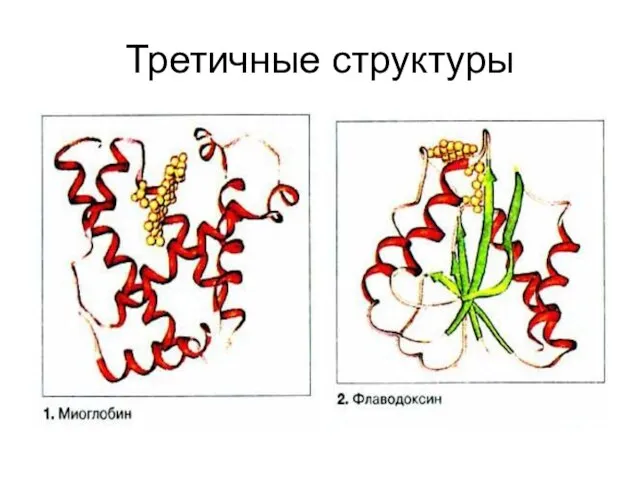
Слайд 43Инсулин третичная и четвертичная структура
Инсулин третичная и четвертичная структура
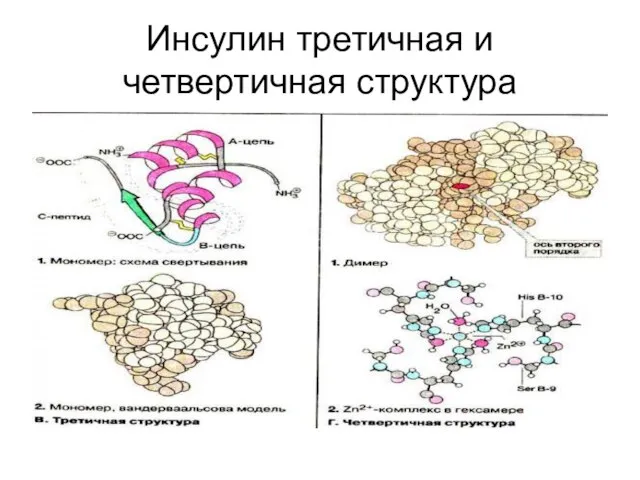
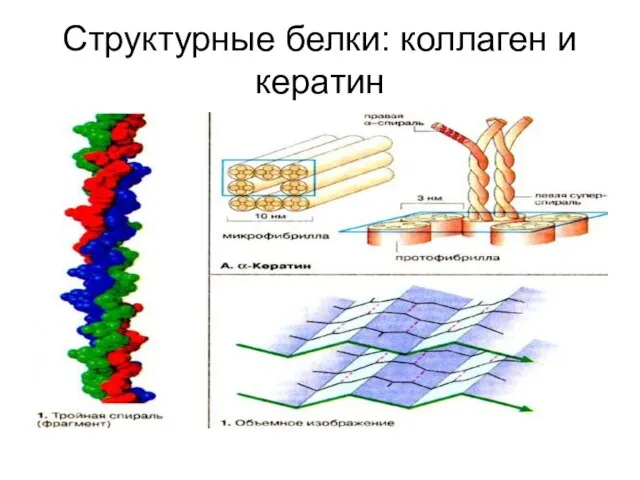
Слайд 44Структурные белки: коллаген и кератин
Структурные белки: коллаген и кератин
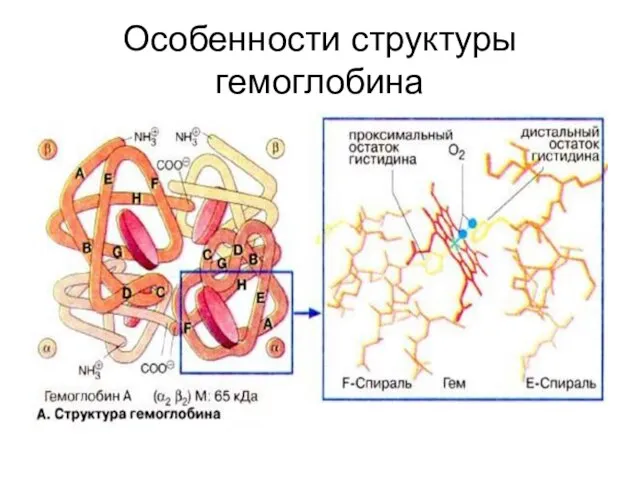
Слайд 45Особенности структуры гемоглобина
Особенности структуры гемоглобина
 Презентация на тему Контрреформы Александра ΙΙΙ
Презентация на тему Контрреформы Александра ΙΙΙ  Лекция № 12 Механические колебания
Лекция № 12 Механические колебания Gif-анимация в PhotoShop CS5
Gif-анимация в PhotoShop CS5 Восприятие
Восприятие Деловые встречи.Переговоры
Деловые встречи.Переговоры Интерьер бального зала
Интерьер бального зала Автомобиль будущего
Автомобиль будущего Античный мир Зевс
Античный мир Зевс Компьютер – враг, друг, помощник?
Компьютер – враг, друг, помощник? Ефаклар. Гель-мікропілінг для очищення проблемної шкіри
Ефаклар. Гель-мікропілінг для очищення проблемної шкіри Весенний праздник – женский день
Весенний праздник – женский день Робототехника для будущего (Умный дом Кировская область)
Робототехника для будущего (Умный дом Кировская область) Удмуртское национальное блюдо пельнянь
Удмуртское национальное блюдо пельнянь Моя будущая профессия
Моя будущая профессия Состав риэлторской услуги
Состав риэлторской услуги Твоя семья 2 класс
Твоя семья 2 класс Презентация на тему Какая бывает роса на траве
Презентация на тему Какая бывает роса на траве Планирование в менеджменте
Планирование в менеджменте ВОЗ о национальной лекаpственной политике и о развитии фармпроизводства
ВОЗ о национальной лекаpственной политике и о развитии фармпроизводства Серия представлена тремя продуктами: Лидер 21 века Тайм-менеджмент. Наука успевать НЛП. Стратегия успеха
Серия представлена тремя продуктами: Лидер 21 века Тайм-менеджмент. Наука успевать НЛП. Стратегия успеха Тренажер лексики на тему: It
Тренажер лексики на тему: It О стратегических оценках последствий изменения климата
О стратегических оценках последствий изменения климата Презентация на тему Загрязнение реки Дон
Презентация на тему Загрязнение реки Дон Презентация на тему Движущие силы эволюции Борьба за существование
Презентация на тему Движущие силы эволюции Борьба за существование «Двойники»
«Двойники» Утвердительно-отрицательный вопрос
Утвердительно-отрицательный вопрос Болмыс. Болмысқа анықтама беруші ғалымдар пікірі
Болмыс. Болмысқа анықтама беруші ғалымдар пікірі Это программа для семей города Луганска, которые добровольно, без материального вознаграждения, берут на себя роль новых мам, пап,
Это программа для семей города Луганска, которые добровольно, без материального вознаграждения, берут на себя роль новых мам, пап,