Содержание
- 2. Учебная цель: закрепить практические навыки ординаторов детских кардиологов по разделу “Генетические основы диагностики сердечно-сосудистых заболеваний”
- 3. Задачи Знать основные типы генных мутаций и полимофизмов, обуславливающих риски развития и неблагоприятного течения кардиоваскулярных заболеваний
- 4. Генетическая диагностика. В настоящее время описано около 2,5 тысяч моногенных наследственных синдромов, при которых наблюдается вовлечение
- 5. Генетическая диагностика. Известно около сотни наследственных заболеваний, при которых поражение сердца и сосудов являются ведущими в
- 6. Генетическая диагностика. Из общей структуры даже таких классических мультифакториальных заболеваний, как ишемическая болезнь сердца и артериальная
- 7. По сравнению с применяемыми функциональными методами диагностики сердечно-сосудистых заболеваний, данный метод позволяет более точно спрогнозировать вероятность
- 8. С учетом результатов генотипирования возможно проводить эффективную целевую профилактику заболевания сердечно-сосудистой системы.
- 9. направлена на регистрацию непосредственной причины заболевания в виде изменения нуклеотидной последовательности ДНК. ДНК-диагностика
- 10. Выявление мутации в конкретном гене напрямую свидетельствует о наличии заболевания, независимо от степени выраженности клинических симптомов,
- 11. Пресимптоматическая диагностика позволяет сформировать оптимальную тактику наблюдения для каждого пациента, с учетом генетических, анамнестических и электрокардиографических
- 12. В зависимости от пораженного гена, по-разному оценивается влияние пола и возраста на риск кардио-васкулярной смерти .
- 13. Описаны мутации, ассоциированные как с относительно благоприятным течением заболевания, так и с очень тяжелым прогнозом. Данные
- 14. Современные подходы к оценке риска внезапной смерти у таких пациентов и выбору тактики лечения в значительной
- 16. Ген ангиотензин I-превращающего фермента (ACE). Полиморфизм Alu Ins/Del. Активность фермента в крови связана с наличием варианта
- 17. Ген ангиотензин I-превращающего фермента (ACE). Полиморфизм Alu Ins/Del. Показания к анализу. Коронарная болезнь сердца, ишемическая болезнь
- 18. AGTR1 (рецептор типа I ангиотензина-II) Полиморфизм -1166 A>C Рецептор типа I ангиотензина-II (AGTR1) обуславливает основные кардиоваскулярные
- 19. AGTR1 (рецептор типа I ангиотензина-II) Полиморфизм -1166 A>C Показания к анализу: гипертония, диабетическая нефропатия, ишемическая болезнь
- 20. AGT (ангиотензиноген) Полиморфизмы T174M (C>T) и M235T (T>C) Ангиотензиноген (AGT) производится печенью и служит предшественником ангиотензина-II,
- 21. AGT (ангиотензиноген) Полиморфизмы T174M (C>T) и M235T (T>C) Показания к анализу: гипертония, старшая возрастная группа (>45
- 22. NOS3 (синтаза окиси азота) Полиморфизм E298D (G->T) Синтаза окиси азота (NOS3) синтезирует окись азота, принимающую участие
- 23. NOS3 (синтаза окиси азота) Полиморфизм E298D (G->T) Показания к анализу: инфаркт миокарда, сердечно-сосудистые заболевания, нарушение артериальной
- 24. ApoE (аполипопротеин Е) Полиморфизмы L28P (3100 T->C), ApoE*2 (Arg158Cys) и ApoE*4 (Cys112Arg) Физиология и генетика. Аполипопротеин
- 25. ApoE (аполипопротеин Е) Полиморфизмы L28P (3100 T->C), ApoE*2 (Arg158Cys) и ApoE*4 (Cys112Arg) Физиология и генетика. Участвует
- 26. ApoE (аполипопротеин Е) Полиморфизмы L28P (3100 T->C), ApoE*2 (Arg158Cys) и ApoE*4 (Cys112Arg) Показания к анализу: инфаркт
- 28. Ген метилентетрагидрофолатредуктазы (MTHFR). Метилентетрагидрофолатредуктаза (MTHFR) играет ключевую роль в метаболизме фолиевой кислоты. Фермент катализирует восстановление 5,10-метилентетрагидрофолята
- 29. Ген метилентетрагидрофолатредуктазы (MTHFR). Метилентетрагидрофолатредуктаза (MTHFR) играет ключевую роль в метаболизме фолиевой кислоты. Фермент катализирует восстановление 5,10-метилентетрагидрофолята
- 30. Ген MTHFR локализован на хромосоме 1р36.3. Известно около двух десятков мутаций этого гена, нарушающих функцию фермента.
- 31. Ген MTHFR полиморфизм MTHFR обозначается как мутация C677T. У лиц, гомозиготных по данной мутации (генотип Т/Т),
- 32. Ген MTHFR Показания к анализу: ИБС, инфаркт миокарда, атеросклероз, атеротромбоз.
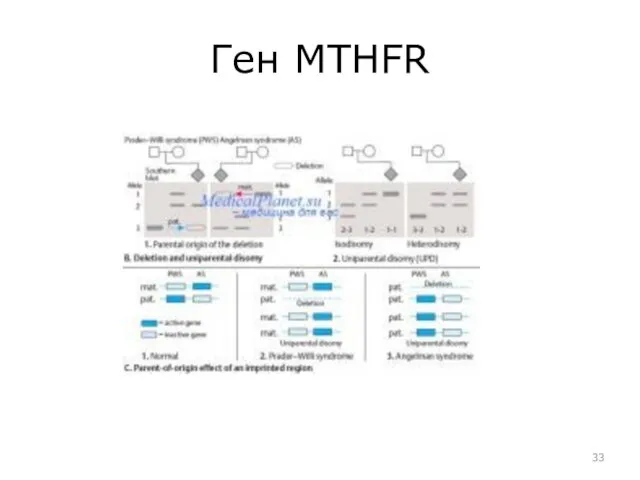
- 33. Ген MTHFR
- 34. PPARD (рецептор активатора пролиферации пероксисом) Полиморфизм T(–87)C (T294C) PPARs - это группа ядерных рецепторов, которые выступают
- 35. PPARD (рецептор активатора пролиферации пероксисом) Полиморфизм T(–87)C (T294C) Показано, что PPARD играет роль в β-окислении жирных
- 36. PPARD (рецептор активатора пролиферации пероксисом) Полиморфизм T(–87)C (T294C) Показания к анализу: Сердечно-сосудистые заболевания в семейном анамнезе,
- 37. ITGA2 (Интегрин альфа-2) Аббревиатуры GPIa (гликобелок Ia), CD49B, VLA-2 (англ. «very late activation antigen 2») относятся
- 38. Ген хемокинового рецептора (CCR2). Полиморфизм Ile64Val Ген CCR2 кодирует 2 изоформы рецептора для моноцитов. Данный рецептор
- 39. Но у некоторых ВИЧ – инфицированных больных число лимфоцитов CD4+ не снижается и СПИД не развивается
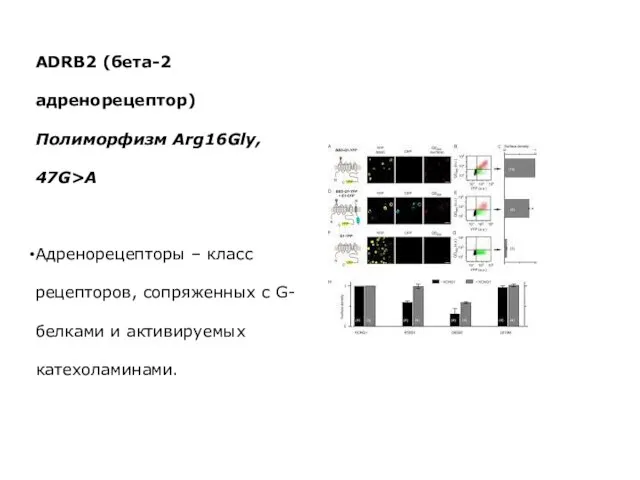
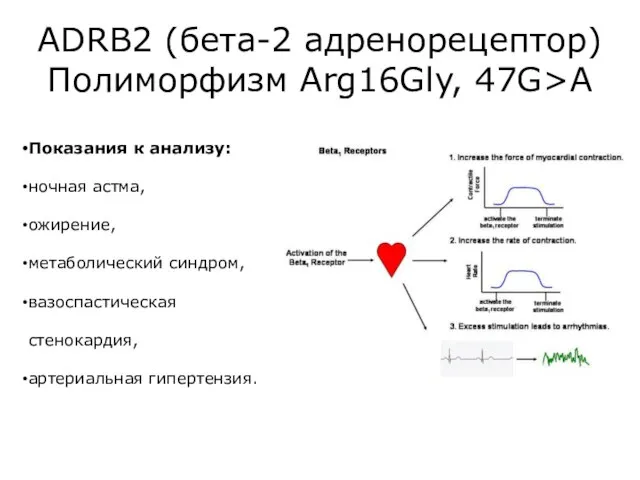
- 40. ADRB2 (бета-2 адренорецептор) Полиморфизм Arg16Gly, 47G>A Адренорецепторы – класс рецепторов, сопряженных с G-белками и активируемых катехоламинами.
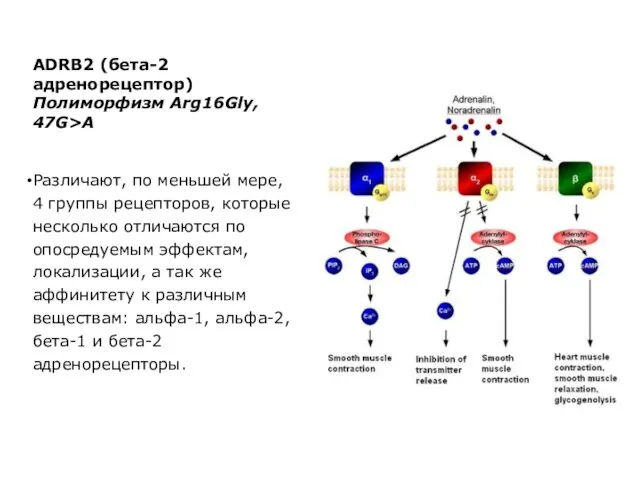
- 41. ADRB2 (бета-2 адренорецептор) Полиморфизм Arg16Gly, 47G>A Различают, по меньшей мере, 4 группы рецепторов, которые несколько отличаются
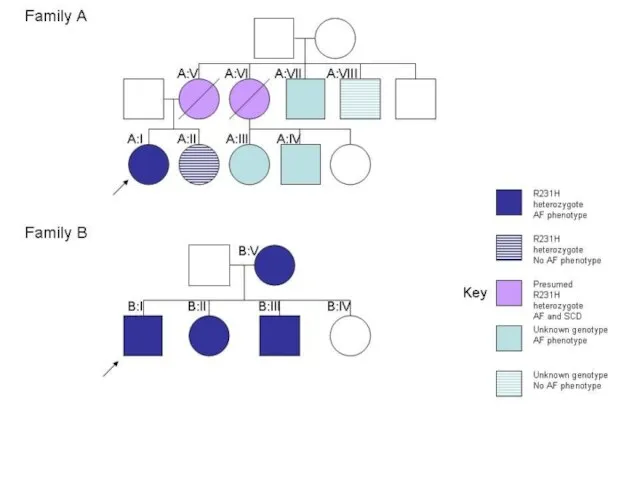
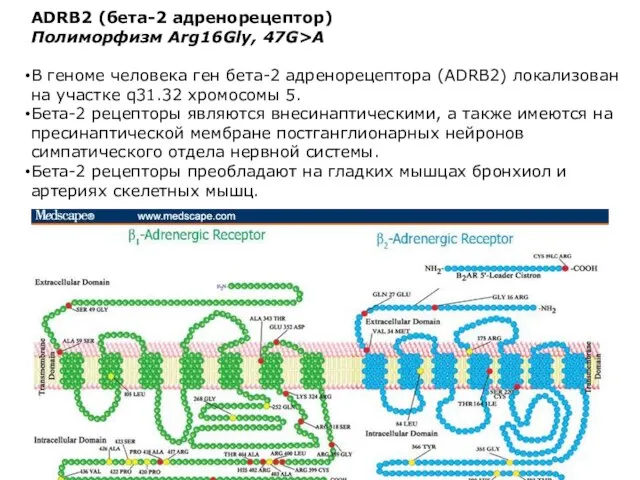
- 43. ADRB2 (бета-2 адренорецептор) Полиморфизм Arg16Gly, 47G>A В геноме человека ген бета-2 адренорецептора (ADRB2) локализован на участке
- 44. При их возбуждении обеспечивается тормозной эффект: расширение сосудов (коронарных, скелетных мышц), расслабление гладких мышц, дыхательных путей,
- 45. Показания к анализу: ночная астма, ожирение, метаболический синдром, вазоспастическая стенокардия, артериальная гипертензия. ADRB2 (бета-2 адренорецептор) Полиморфизм
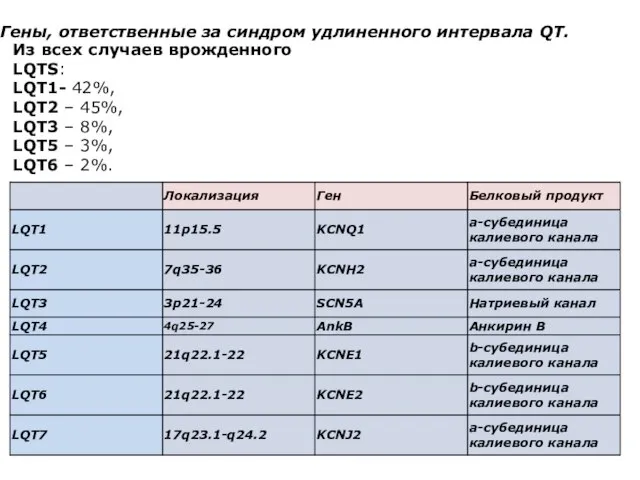
- 47. Гены, ответственные за синдром удлиненного интервала QT. Из всех случаев врожденного LQTS: LQT1- 42%, LQT2 –
- 49. Скачать презентацию




































 Каталитическая активность ферментов в живых тканях
Каталитическая активность ферментов в живых тканях ИКТ как средство повышения качества и доступности учебников
ИКТ как средство повышения качества и доступности учебников Ландшафтный свет
Ландшафтный свет Политика, блок 3:Политические процессы.
Политика, блок 3:Политические процессы. Дипломная работа по курсу Инста-Профи 7.0
Дипломная работа по курсу Инста-Профи 7.0 Рождество в Англии и США
Рождество в Англии и США МБОУ Еланская СОШ
МБОУ Еланская СОШ МАФ из современных материалов для детских площадок
МАФ из современных материалов для детских площадок Конституционно правовые нормы Великобритании
Конституционно правовые нормы Великобритании Становление самодержавияРомановых
Становление самодержавияРомановых Enhanced External Counterpulsation
Enhanced External Counterpulsation Тема урока: «Классификация профессий по целям труда, по орудиям и условиям труда»
Тема урока: «Классификация профессий по целям труда, по орудиям и условиям труда» Расчет массы и объема тела по его плотности
Расчет массы и объема тела по его плотности Формирование УУД в учебной деятельности
Формирование УУД в учебной деятельности Проектирование транспортно-грузовых комплексов
Проектирование транспортно-грузовых комплексов Бегающие стулья
Бегающие стулья Строгально-протяжные станки
Строгально-протяжные станки Вначале было слово…. День славянской письменности и культуры
Вначале было слово…. День славянской письменности и культуры Притяжение звездного неба
Притяжение звездного неба Животные Саратовской области и своей местности. Их охрана
Животные Саратовской области и своей местности. Их охрана Здоровье как человеческая ценность
Здоровье как человеческая ценность Проверка знаний по ИЗО (2 класс)
Проверка знаний по ИЗО (2 класс) Строение и многообразие водорослей
Строение и многообразие водорослей Возможности и перспективы аутсорсинга в бюджетных учреждениях
Возможности и перспективы аутсорсинга в бюджетных учреждениях Убранство русской избы
Убранство русской избы Уроки нравственности Толстого
Уроки нравственности Толстого Натюрморт
Натюрморт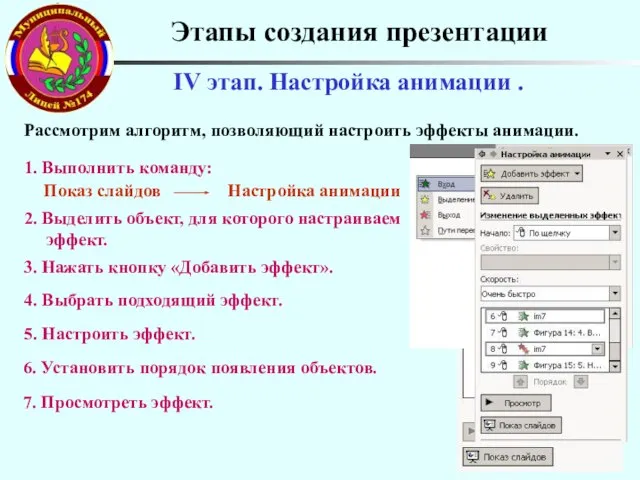 Этапы создания презентации
Этапы создания презентации