Содержание
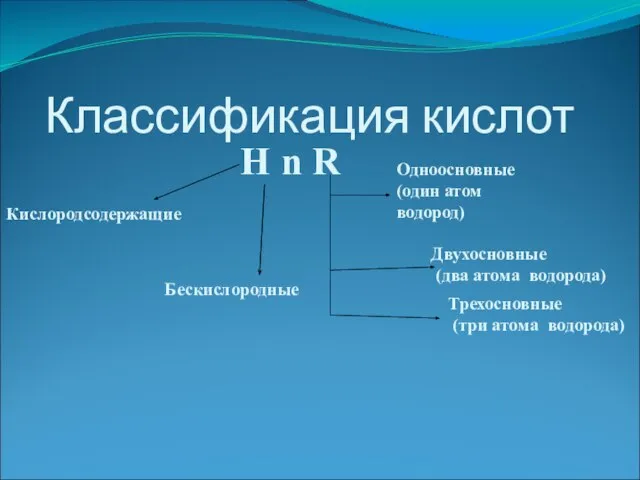
- 2. Классификация кислот H n R Кислородсодержащие Бескислородные Одноосновные (один атом водород) Двухосновные (два атома водорода) Трехосновные
- 3. Сильные кислоты HCl – HI – HNO3 – H2SO4 – HBr – соляная кислота иодоводородная кислота
- 4. Слабые кислоты -H2S -HNO2 -H2SO 3 SO2 H2O -H2CO3 CO2 H2O -H2SiO3 Сероводородная кислота Азотистая кислота
- 5. HCl H2S HNO2 H2SiO3 H2CO3 H3PO4
- 6. H2S H2SiO3 H3PO4 H2CO3 HCl HNO2
- 7. Кислотные оксиды -> Кислоты N 2O 5 -> HNO3 +5 +5 Оксид азота (V)-> Азотная кислота
- 8. Индикаторы – вещества, которые в растворах кислот изменяют свой цвет. ЛАКМУС в р-ре кислоты – красный
- 9. Химические свойства кислот 1. Взаимодействие с металлами ( стоящими до Н ) 2. Взаимодействие с основными
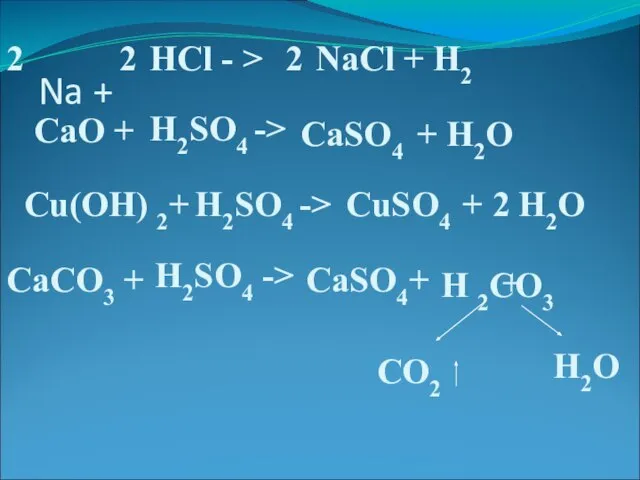
- 10. Na + NaCl + H2 HCl - > 2 2 2 CaO + H2SO4 -> CaSO4
- 11. Закончите уравнения реакций. Са + HNO2 -> Са (NO2) 2+ H2 2 FeO + HNO2 ->
- 13. Скачать презентацию








 Сложение и вычитание смешанных чисел
Сложение и вычитание смешанных чисел Агентам по продаже услуг ООО «АТОН»
Агентам по продаже услуг ООО «АТОН» Трудовые права молодежи
Трудовые права молодежи Цветок ветренницы - праобраз колеса
Цветок ветренницы - праобраз колеса Как читать книгу
Как читать книгу Правописание НЕ
Правописание НЕ Презентация на тему Биологические особенности раннецветущих растений
Презентация на тему Биологические особенности раннецветущих растений  Презентация на тему С огнем не играй - пожар не затевай!
Презентация на тему С огнем не играй - пожар не затевай! Планирование расходов в период подготовки и проведения выборов в единый день голосования
Планирование расходов в период подготовки и проведения выборов в единый день голосования Номинация Рукоделие
Номинация Рукоделие Казахский университет международных отношений и мировых языков имени Абылай хана
Казахский университет международных отношений и мировых языков имени Абылай хана Оптический принцип записи и считывания информации
Оптический принцип записи и считывания информации Presentation Title
Presentation Title  Психолого-педагогическая характеристика и развивающие занятия для детей раннего возраста
Психолого-педагогическая характеристика и развивающие занятия для детей раннего возраста ИСПОЛНЕНИЕ БЮДЖЕТА МО ТЮМЕНСКИЙ МУНИЦИПАЛЬНЫЙ РАЙОН за 1 полугодие 2011 года
ИСПОЛНЕНИЕ БЮДЖЕТА МО ТЮМЕНСКИЙ МУНИЦИПАЛЬНЫЙ РАЙОН за 1 полугодие 2011 года Практикум по проектной деятельности в социальных организациях (в рамках стажёрской практики студентов)
Практикум по проектной деятельности в социальных организациях (в рамках стажёрской практики студентов) Совет по профориентации УГНТУ
Совет по профориентации УГНТУ Организация технического обслуживания и ремонта высоковольтных выключателей
Организация технического обслуживания и ремонта высоковольтных выключателей Стипендиальные программы
Стипендиальные программы 5 причин, почему для Вашего бренда будет полезно выиграть 500 000 грн на медиа-размещение в соцсетиОдноклассники
5 причин, почему для Вашего бренда будет полезно выиграть 500 000 грн на медиа-размещение в соцсетиОдноклассники Повторение
Повторение Монтаж соединения проводов с помощью сварки
Монтаж соединения проводов с помощью сварки Распространение ППО в системе образования Варгашинского района как ресурс развития учительского потенциала
Распространение ППО в системе образования Варгашинского района как ресурс развития учительского потенциала Создание цветочного салона
Создание цветочного салона Поход за грибами
Поход за грибами Развитие познавательной активности на уроках «Человек и мир»
Развитие познавательной активности на уроках «Человек и мир» Олеиновая кислота
Олеиновая кислота SMM, SEO, Баннеры – в чем отличие?
SMM, SEO, Баннеры – в чем отличие?