Содержание
- 2. Аммиак может быть обязан своим названием оазису бога Аммона в Северной Африке, находящемуся на перекрестке караванных
- 3. По некоторым другим сведениям, аммиак мог получить современное название от древнеегипетского слова «амониан». Так называли всех
- 4. Сокращенное название «аммиак» которым мы всегда пользуемся, ввел в обиход в 1801 году русский ученый -
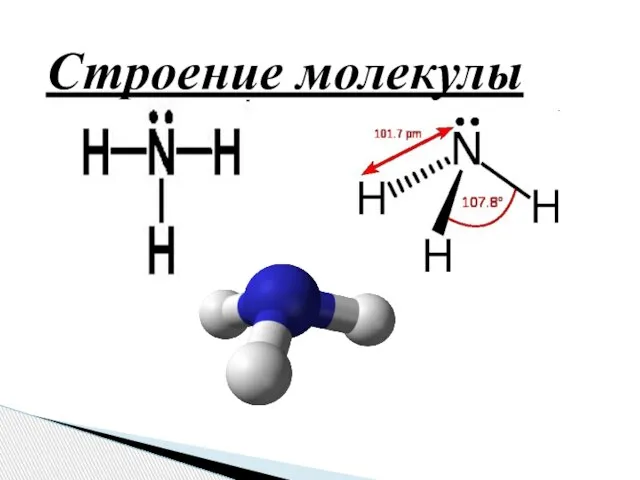
- 5. Строение молекулы
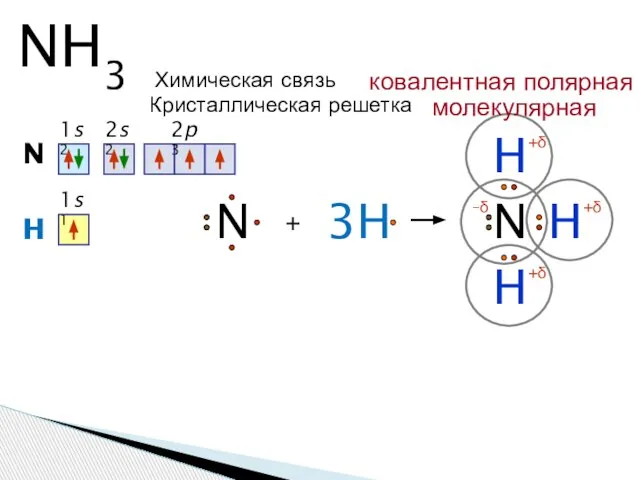
- 6. NH3 N 1s2 2s2 2p3 + H N H H 3H H N 1s1 +δ +δ
- 7. Молекула аммиака имеет форму тригональной пирамиды с атомом азота в вершине. Три неспаренных p-электрона атома азота
- 8. Физические свойства (при н.у. ) бесцветный газ с резким характерным запахом (запах нашатырного спирта) легче воздуха
- 9. По физиологическому действию на организм относится к группе веществ удушающего и нейротропного действия, способных вызвать токсический
- 10. Получение аммиака Для получения аммиака в лаборатории используют действие сильных щелочей на соли аммония: 2NH4Cl +
- 11. Промышленный способ получения аммиака основан на прямом взаимодействии водорода и азота: N2(г) + 3H2(г) ↔ 2NH3(г)
- 12. Химические свойства аммиака Для аммиака характерны реакции: 1) с изменением степени окисления атома азота (реакции окисления);
- 13. Реакции с изменением степени окисления атома азота (реакции окисления) N-3 → N0→ N+2 NH3-сильный восстановитель
- 14. с кислородом Горение аммиака (при нагревании) 4NH3 + 3O2 → 2N2 + 6H20 Каталитическое окисление амииака
- 15. с оксидами металлов 2NH3 +3CuO =3Cu + N2 +3H2O
- 16. с сильными окислителями 2NH3 + 3Cl2 = N2 + 6HCl (при нагревании)
- 17. Реакции без изменения степени окисления атома азота (присоединение - образование иона аммония NH4+ по донорно-акцепторному механизму
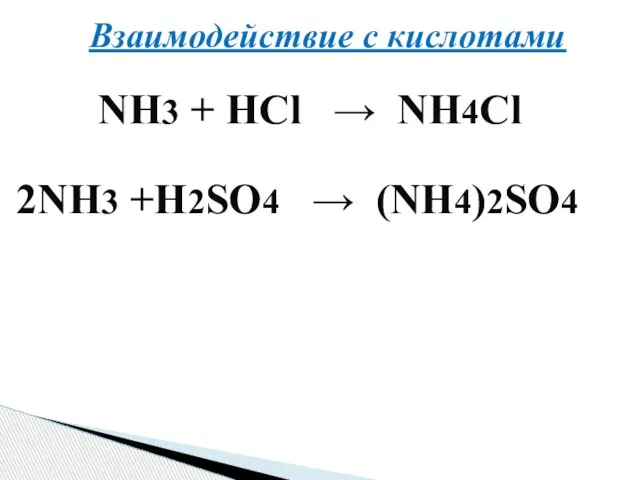
- 18. Взаимодействие с кислотами NH3 + HCl → NH4Cl 2NH3 +H2SO4 → (NH4)2SO4
- 19. Взаимодействие с водой NH3 + H2O = NH4OH При добавлении фенолфталеина‑ раствор становится малиновым, так как
- 20. Применение аммиака Производство пластмасс и волокон 2. В составе моющих средств
- 21. 3. Производство азотных удобрений 4. В сельском хозяйстве
- 22. 5. Производство азотной кислоты 6. Получение взрывчатых веществ
- 23. 7. В медицине
- 24. По объемам производства аммиак занимает одно из первых мест; ежегодно во всем мире получают около 100
- 26. Скачать презентацию



















 АлександрСергеевич Пушкин
АлександрСергеевич Пушкин П Р Е З Е Н Т А Ц И Я
П Р Е З Е Н Т А Ц И Я Презентация на тему Значение опорно-двигательной системы человека
Презентация на тему Значение опорно-двигательной системы человека Учение Н. И. Пироговао врачебных ошибках
Учение Н. И. Пироговао врачебных ошибках Концепция развития ЭБ ГПИБ и задачи сохранности библиотечного фонда
Концепция развития ЭБ ГПИБ и задачи сохранности библиотечного фонда Борис Григорьев 1918 г. Виже-Лебре
Борис Григорьев 1918 г. Виже-Лебре  МОСКВА, Май 2011 ИНВЕСТИЦИИ В РАЗВИТИЕ: Инвесторы не хотят или ритейлеры не могут? DIY & HH DIRECTOR 2011. - презентация
МОСКВА, Май 2011 ИНВЕСТИЦИИ В РАЗВИТИЕ: Инвесторы не хотят или ритейлеры не могут? DIY & HH DIRECTOR 2011. - презентация Совет спорторгов УГНТУ
Совет спорторгов УГНТУ Константин Капитан Актер театра и кино, режиссер, шоу мен, сценарист, конферансье, ведущий, тамада.
Константин Капитан Актер театра и кино, режиссер, шоу мен, сценарист, конферансье, ведущий, тамада. Генно-модифицированные продукты растительного происхождения: проблемы биоэтики и биобезопасности
Генно-модифицированные продукты растительного происхождения: проблемы биоэтики и биобезопасности Решение линейных уравнений, с параметрами, содержащими знак модуля
Решение линейных уравнений, с параметрами, содержащими знак модуля Принадлежность к двуум мирам
Принадлежность к двуум мирам монолог_9
монолог_9 Температура и температурные шкалы.
Температура и температурные шкалы. Бизнес-план
Бизнес-план 6_klass_RYa_1_urok
6_klass_RYa_1_urok Дом без насилия
Дом без насилия Прецизионная радиовысотометрия из космоса
Прецизионная радиовысотометрия из космоса Специальные средства и средства индивидуальной бронезащиты
Специальные средства и средства индивидуальной бронезащиты Судебно-бухгалтерская экспертиза
Судебно-бухгалтерская экспертиза Презентация на тему Защита окружающей среды
Презентация на тему Защита окружающей среды Социальные права человека
Социальные права человека 14 жовтня
14 жовтня ВСЕОБЩАЯ ДЕКЛАРАЦИЯ ПРАВ ЧЕЛОВЕКА: 1948–2011ГОДЫ
ВСЕОБЩАЯ ДЕКЛАРАЦИЯ ПРАВ ЧЕЛОВЕКА: 1948–2011ГОДЫ Рыбалка. Книги о рыбаках
Рыбалка. Книги о рыбаках Воздушное питание растений. Фотосинтез
Воздушное питание растений. Фотосинтез Биологическая и психологическая подструктура личности
Биологическая и психологическая подструктура личности ПРОГРАММЫ МНТЦ
ПРОГРАММЫ МНТЦ