Содержание
- 2. Состав Кислоты - это сложные вещества, в молекулах которых содержат атомы водорода и кислотный остаток H-R,
- 3. Классификация кислот Одноосновные кислоты, например, HCl, HNO3 (отщепляют при диссоциации один атом водорода) Многоосновные кислоты, например,
- 4. Разбавление серной кислоты Относительно смешивания серной кислоты с водой с давних пор существует строгое правило: «Сначала
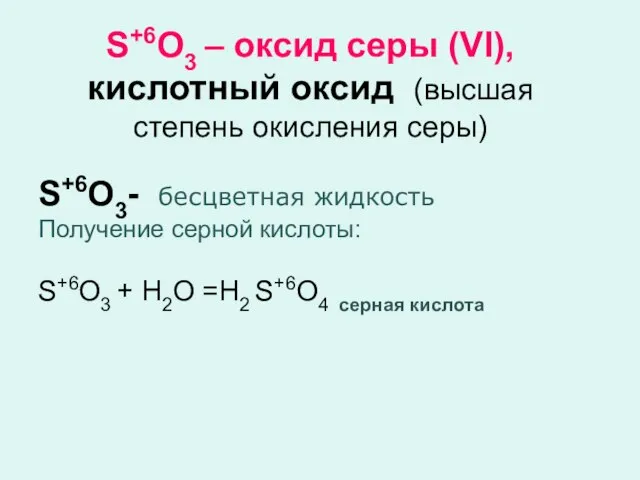
- 5. S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы) S+6O3- бесцветная жидкость Получение серной
- 6. Химические свойства серной кислоты разбавленная серная кислота проявляет все характерные свойства кислот: С оксидами металлов.(реакция обмена)
- 7. Качественная реакция на ион –SO42- Реактивом на серную кислоту и ее соли является катион бария ,
- 8. Концентрированная серная кислота Ме+Н2SO4(кoнц)→МеSO4+H2O+(Н2S,S,SO2) Серная кислота(конц) восстанавливается до (Н2S,S,SO2) в зависимости от активности металла и условий
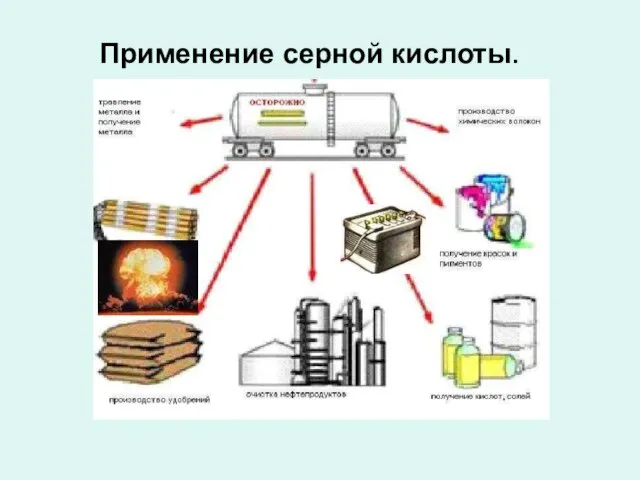
- 9. Применение серной кислоты.
- 10. Сульфат натрия.
- 11. Сульфат никеля
- 12. Сульфат меди дать классификацию химическим реакциям.
- 14. Скачать презентацию








 Операционная система персонального компьютера
Операционная система персонального компьютера Католицизм: кнут и пряник
Католицизм: кнут и пряник Презентация на тему тренажер по английскому языку
Презентация на тему тренажер по английскому языку Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО
Публичный докладдиректора школы МОУ “СОШ № 10” Н.А. Давыдовой г.Биробиджан, ЕАО Декларации пожарной безопасности
Декларации пожарной безопасности  Презентация на тему: Бородинская панорама
Презентация на тему: Бородинская панорама Заседание Совета кураторов
Заседание Совета кураторов Нутромер оборудование для измерения диаметра внутренних полостей
Нутромер оборудование для измерения диаметра внутренних полостей Music
Music Устройство увеличительных приборов. Строение клетки
Устройство увеличительных приборов. Строение клетки Реклама новых книг
Реклама новых книг Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей
Роль точечных мутаций гена RUNX1 в патогенезе миелодиспластических и миелопролиферативных заболеваний у детей FLEXWORK project materials and their use in TELESOL
FLEXWORK project materials and their use in TELESOL Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА
Презентация на тему ПРИНЦИП ГЮЙГЕНСА. ЗАКОН ОТРАЖЕНИЯ СВЕТА Выдающаяся личность
Выдающаяся личность урок
урок Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ»
Презентация услуг компании «ГЛОБАЛ КОНСАЛТИНГ» Храм Святой Софии в Константинополе
Храм Святой Софии в Константинополе Сечение ударной электронной ионизации. Оже-электроны
Сечение ударной электронной ионизации. Оже-электроны Россия на политической карте мира. Особенности развития на современном этапе
Россия на политической карте мира. Особенности развития на современном этапе Животные и растения Северной Америки
Животные и растения Северной Америки Иконки автомобильные
Иконки автомобильные The dark matter power complex
The dark matter power complex Система академика Л.Занкова
Система академика Л.Занкова “Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол”
“Практика внедрения международного стандарта ISО 14001 в ОАО “Концерн Стирол” АООП НОО для обучающихся с НОДА
АООП НОО для обучающихся с НОДА Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках
Лига Индиго. Интеллектуально-развлекательная игра. Разрыв шаблона о корпоративных праздниках Компания МИКРОБОР НАНОТЕХ
Компания МИКРОБОР НАНОТЕХ