Содержание
- 2. Цели урока - познакомиться с основными химическими производствами Казахстана; -научиться вычислять выход продукта реакции от теоретически
- 3. Критерии оценивания -называет основные производства и производственные процессы, осуществляемые в Республике Казахстан - производит расчеты выхода
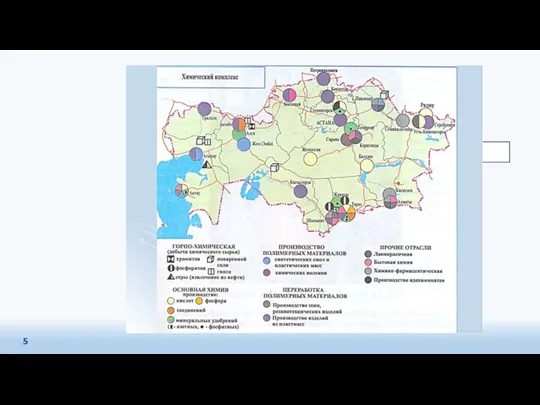
- 4. Химическая промышленность Казахстана Основными предприятиями химической промышленности РК являются: АО «Актюбинский завод хромовых соединений», АО «Ульбинский
- 7. 5
- 8. 3
- 9. Химическая промышленность Казахстана, основанная на богатейшей сырьевой базе, имеет большие перспективы для развития и представляет большой
- 10. 1) Прочитай внимательно условие задачи 2) Запиши: «Дано» и «Найти». 3) Составь уравнение реакции (не забудь
- 11. Задача 1. При взаимодействии магния массой 1,2 г с раствором серной кислоты получили соль массой 5,
- 12. Решите задачи: 1.Металлический хром получают восстановлением его оксида Cr2O3 металлическим алюминием. Вычислите массу хрома, который можно
- 14. Скачать презентацию










 Федеральный Государственный образовательный стандарт начального общего образования представляет собой совокупность требований
Федеральный Государственный образовательный стандарт начального общего образования представляет собой совокупность требований Дистанционные занятия рукопашным боем для детей возрастом 8 - 9 лет
Дистанционные занятия рукопашным боем для детей возрастом 8 - 9 лет 115035 г.Москва Болотная ул., 12, стр. 3 Тел/факс (095)234-53-76
115035 г.Москва Болотная ул., 12, стр. 3 Тел/факс (095)234-53-76 Многозначные слова и омонимы
Многозначные слова и омонимы Хәрефләрдән сүз төзегез Н, ф, е, о, а, к, т, и
Хәрефләрдән сүз төзегез Н, ф, е, о, а, к, т, и Правовое регулирование информации ограниченного доступа. Тема 3
Правовое регулирование информации ограниченного доступа. Тема 3 Студенческая жизнь факультета ККП
Студенческая жизнь факультета ККП Пилотирование УМКк учебникам Ю.А. Комаровой, И.В. Ларионовой, Ж. Перретт«Английский язык. BRILLIANT». Изд. «Русское слово. Макмиллан»в 3,
Пилотирование УМКк учебникам Ю.А. Комаровой, И.В. Ларионовой, Ж. Перретт«Английский язык. BRILLIANT». Изд. «Русское слово. Макмиллан»в 3, Состав этапов типового проекта моделирования и реорганизации бизнес-процессов организации
Состав этапов типового проекта моделирования и реорганизации бизнес-процессов организации Меню для футболистов
Меню для футболистов Новогодние открытки
Новогодние открытки Технологии преодоления карьерных кризисов
Технологии преодоления карьерных кризисов ТАҚДИМОТ СЕНТЯБР
ТАҚДИМОТ СЕНТЯБР Пропорции для срисовки
Пропорции для срисовки Вода - путешественница
Вода - путешественница Презентация урока географии в 8 классе
Презентация урока географии в 8 классе «Дозиметрические приборы для излучений радиотерапевтических установок, услуги по разработке проектов размещения клинических р
«Дозиметрические приборы для излучений радиотерапевтических установок, услуги по разработке проектов размещения клинических р 20161218_chtogde_kogda
20161218_chtogde_kogda Темы про Пететрбург и Москву
Темы про Пететрбург и Москву Приемы формирования ключевых компетентностей на уроках истории и обществознания
Приемы формирования ключевых компетентностей на уроках истории и обществознания Презентация на тему Кто лишний?
Презентация на тему Кто лишний? Искусство кино
Искусство кино Проект на тему : ПО Маяк
Проект на тему : ПО Маяк МОУ Ильменская
МОУ Ильменская Лечение астматического статуса
Лечение астматического статуса Слайды для рекламы на выставках
Слайды для рекламы на выставках Гоночный трек Долина скорости
Гоночный трек Долина скорости Презентация на тему Победы и поражения России на рубеже 19-20 веков.
Презентация на тему Победы и поражения России на рубеже 19-20 веков.