Слайд 3Что общего между этими картинками?
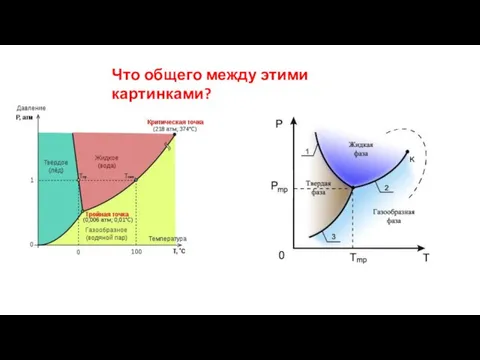
Слайд 4Фазовые диаграммы. Тройная точка.
Критическое состояние вещества.
Цель обучения:
объяснять и анализировать фазовую

диаграмму, определять тройную точку;
определять и объяснять критическую температуру;
раскрывать физическое содержание фазовой диаграммы.
Слайд 5Критерии оценивания:
Учащийся:
анализирует фазовую диаграмму;
объясняет и описывает критическую температуру вещества;
объясняет

физический смысл тройной точки;
анализирует равновесное состояние вещества.
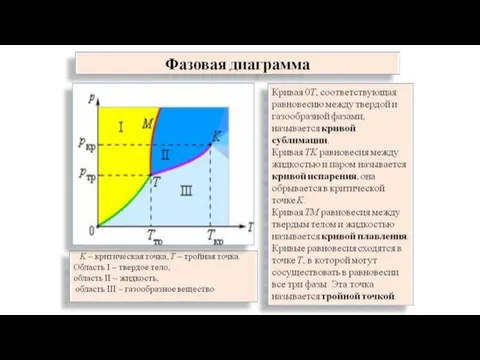
Слайд 6Как на диаграмме обозначены области агрегатных состояний?
Укажите критическую точку на диаграмме.
Укажите кривую
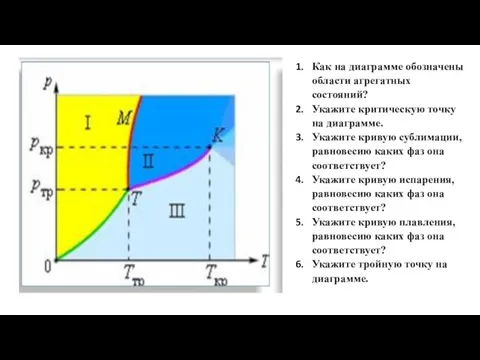
сублимации, равновесию каких фаз она соответствует?
Укажите кривую испарения, равновесию каких фаз она соответствует?
Укажите кривую плавления, равновесию каких фаз она соответствует?
Укажите тройную точку на диаграмме.
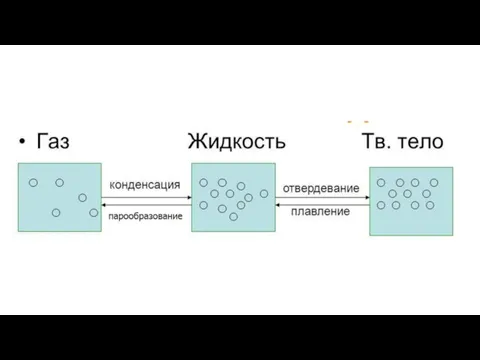
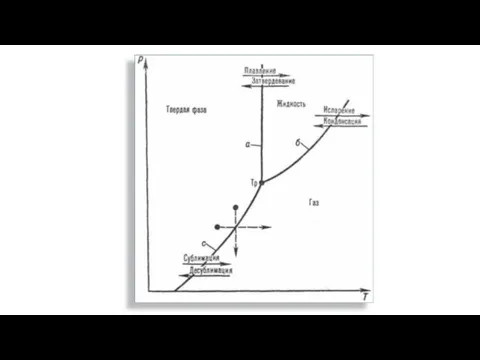
Слайд 8Укажите на данной диаграмме агрегатные состояния вещества и обозначьте какие фазовые переходы

могут произойти.
Слайд 10Критическое состояние вещества
Критическое состояние вещества - наступает тогда, когда отсутствует различие между
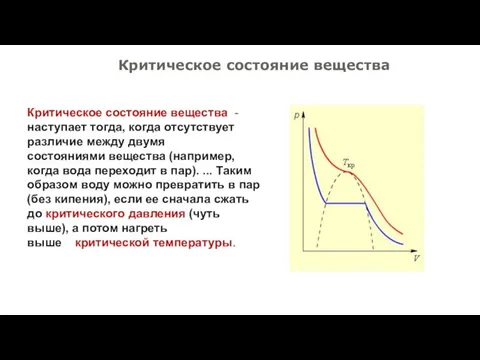
двумя состояниями вещества (например, когда вода переходит в пар). ... Таким образом воду можно превратить в пар (без кипения), если ее сначала сжать до критического давления (чуть выше), а потом нагреть выше критической температуры.
Слайд 11Существует некая критическая температура, выше которой невозможно образование насыщенного пара.
Если этот процесс

изобразить на графике зависимости плотности
от температуры, то можно увидеть, что при критической температуре
плотность жидкости сравнивается с плотностью пара, и различия между
ними пропадают.
Критическая температура – та температура
при которой плотность насыщенного пара равна плотности жидкости.








 Течь жидкости ГУР
Течь жидкости ГУР Оптимизация массогабаритных параметров маховика
Оптимизация массогабаритных параметров маховика Понятие импульса
Понятие импульса Поршневые компрессоры. Лекция №6
Поршневые компрессоры. Лекция №6 Третий закон Ньютона
Третий закон Ньютона Пространство и время
Пространство и время Современные способы и методы контроля и регулировки судовых дизельных двигателей
Современные способы и методы контроля и регулировки судовых дизельных двигателей Закон сохранения энергии в механике
Закон сохранения энергии в механике Устройство и история счетчиков электроэнергии
Устройство и история счетчиков электроэнергии Презентация на тему Плавление
Презентация на тему Плавление  Экспериментальные методы исследования элементарных частиц (68)
Экспериментальные методы исследования элементарных частиц (68) Телескоп. Рефрактор
Телескоп. Рефрактор Физические и химические явления. Признаки химических реакций
Физические и химические явления. Признаки химических реакций Основные понятия. Цепи постоянного тока
Основные понятия. Цепи постоянного тока Ресурс долота. Понятия и расчеты
Ресурс долота. Понятия и расчеты Применение метода стабилизации связей к задачам неголономной механики
Применение метода стабилизации связей к задачам неголономной механики Электростатическое поле в диэлектрике. Лекция 3-2020
Электростатическое поле в диэлектрике. Лекция 3-2020 Модельный ряд двигателей ЗМЗ
Модельный ряд двигателей ЗМЗ Сопротивление материалов
Сопротивление материалов Презентация на тему Электрический ток в различных средах
Презентация на тему Электрический ток в различных средах  Оптика. Закон отражения света
Оптика. Закон отражения света Работа. Мощность. Энергия
Работа. Мощность. Энергия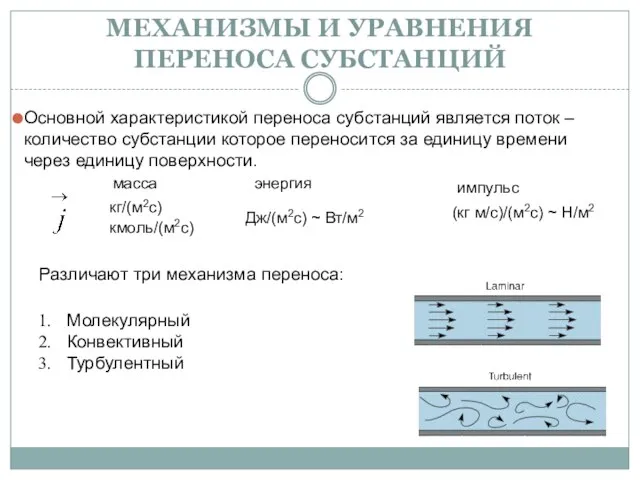 Механизмы и уравнения переноса субстанций
Механизмы и уравнения переноса субстанций Биология. Физика. Химия. Радиация. Естествознание, 10 класс
Биология. Физика. Химия. Радиация. Естествознание, 10 класс Микромир – мир атомов и элементарных частиц
Микромир – мир атомов и элементарных частиц ВКР: совершенствование сервисного обслуживания с модернизацией стенда для проверки форсунок грузовых автомобилей
ВКР: совершенствование сервисного обслуживания с модернизацией стенда для проверки форсунок грузовых автомобилей Регулирование гидромуфт
Регулирование гидромуфт Метод рефрактометрии и ИК-спектроскопии
Метод рефрактометрии и ИК-спектроскопии