Содержание
- 2. 7.1. Закономерности в атомных спектрах Изолированные атомы в виде разреженного газа или паров металлов испускают спектр,
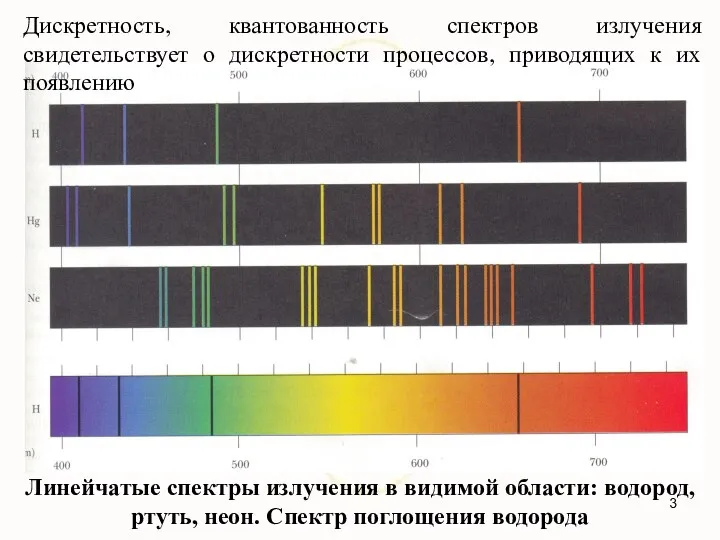
- 3. Линейчатые спектры излучения в видимой области: водород, ртуть, неон. Спектр поглощения водорода Дискретность, квантованность спектров излучения
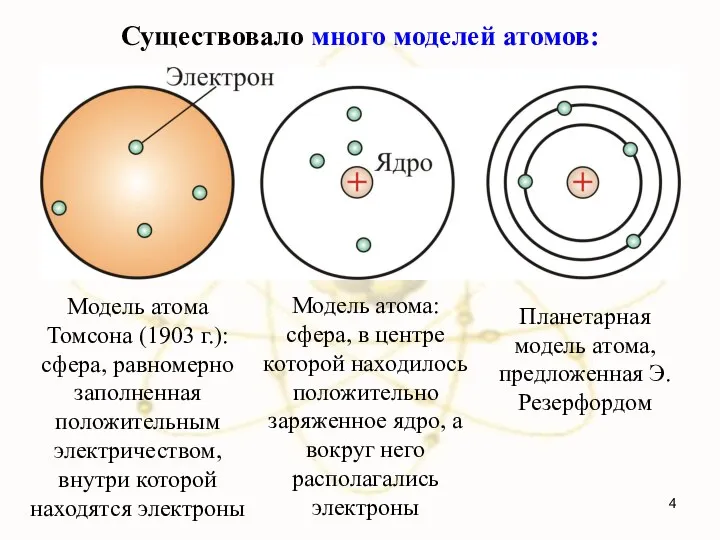
- 4. Существовало много моделей атомов: Модель атома Томсона (1903 г.): сфера, равномерно заполненная положительным электричеством, внутри которой
- 5. и теории строения атома. В 1899 г. открыл альфа - и бета-лучи. Вместе с Ф. Содди
- 6. Планетарная модель строения атома Конец ХIХ - начало ХХ века
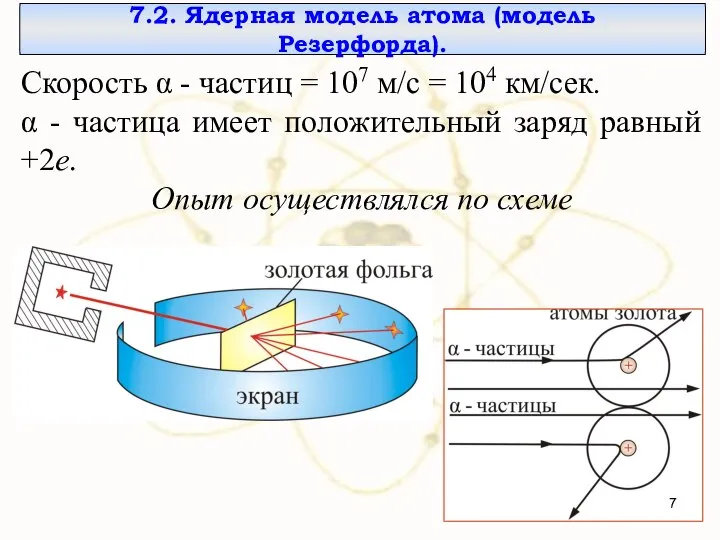
- 7. 7.2. Ядерная модель атома (модель Резерфорда). Скорость α - частиц = 107 м/с = 104 км/сек.
- 8. Узкий пучок α-частиц испускался радиоактивным веществом и попадал на фольгу. При прохождении через фольгу α-частицы отклонялись
- 9. Обнаружилось, что некоторые α-частицы отклонялись на большие углы, до 180º. Резерфорд понял, что такое отклонение возможно
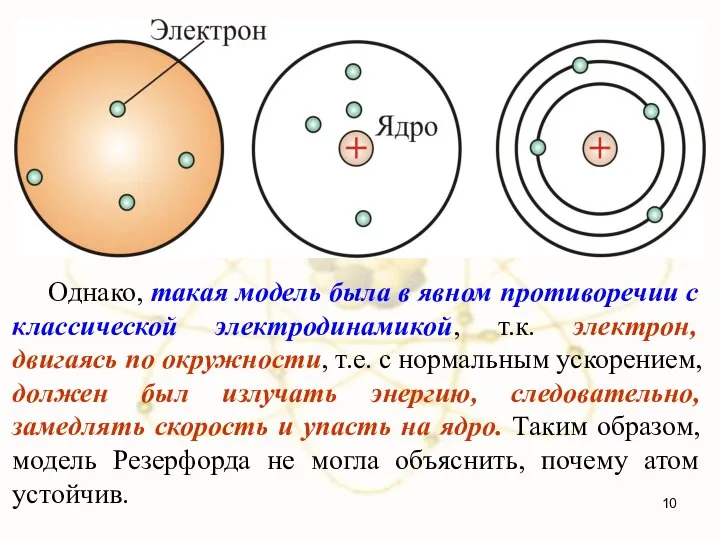
- 10. Однако, такая модель была в явном противоречии с классической электродинамикой, т.к. электрон, двигаясь по окружности, т.е.
- 11. Планетарная модель атома противоречит электродинамике Максвелла
- 12. Согласно которой, ускоренно движущийся заряд излучает электромагнитные волны.
- 13. При движении по окружности имеется центростремительное ускорение. Поэтому электрон должен терять энергию на электромагнитное излучение и
- 14. Попыткой спасения планетарной модели атома стали постулаты Н. Бора
- 15. 7.3. Элементарная теория Бора. БОР Нильс Хендрик Давид (1885–1962) – Выдающийся датский физик-теоретик, один из создателей
- 16. Атом следует описывать как «пирамиду» стационарных энергетических состояний. Пребывая в одном из стационарных состояний, атом не
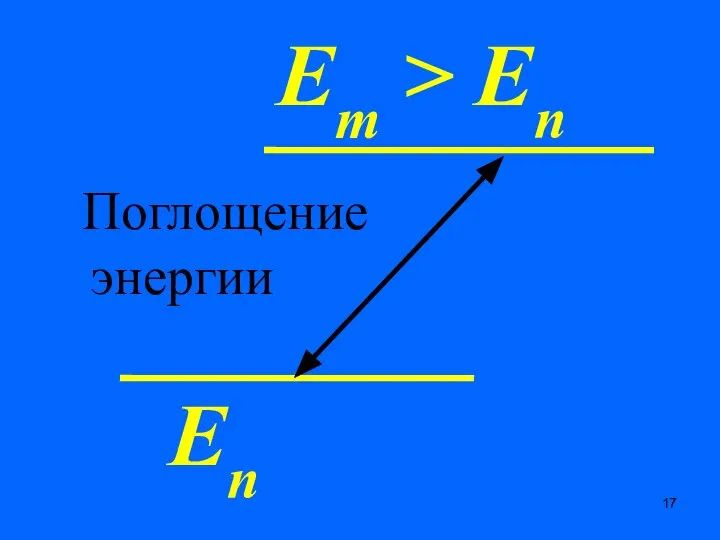
- 17. Еn Em > En Поглощение энергии
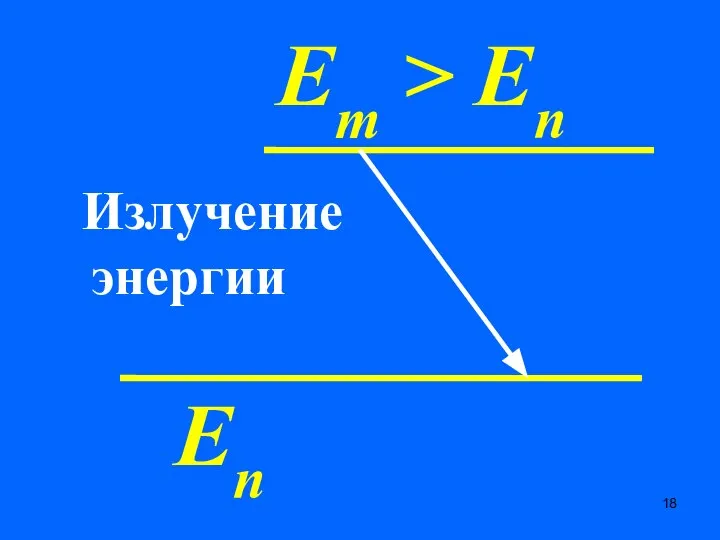
- 18. Еn Em > En Излучение энергии
- 19. Постулаты Бора Первый постулат (постулат стационарных состояний): электроны движутся только по определенным (стационарным) орбитам. При этом,
- 20. Правило частот: частота излучаемой линии, равна или
- 21. Правило квантования орбит: из всех орбит электрона возможны только те, для которых момент импульса равен целому
- 22. Радиус первой орбиты водородного атома называют Боровским радиусом. При n =1, Z = 1 для водорода
- 23. Внутренняя энергия атома слагается из кинетической энергии электрона (ядро неподвижно) и потенциальной энергией взаимодействия электрона с
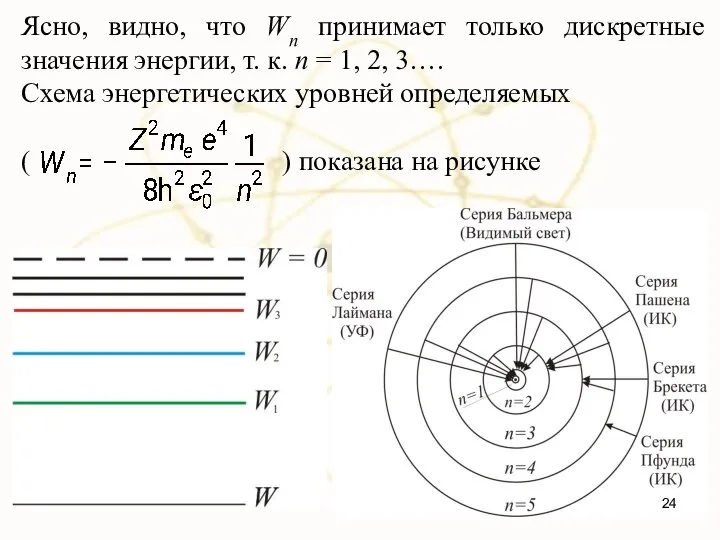
- 24. Ясно, видно, что Wn принимает только дискретные значения энергии, т. к. n = 1, 2, 3….
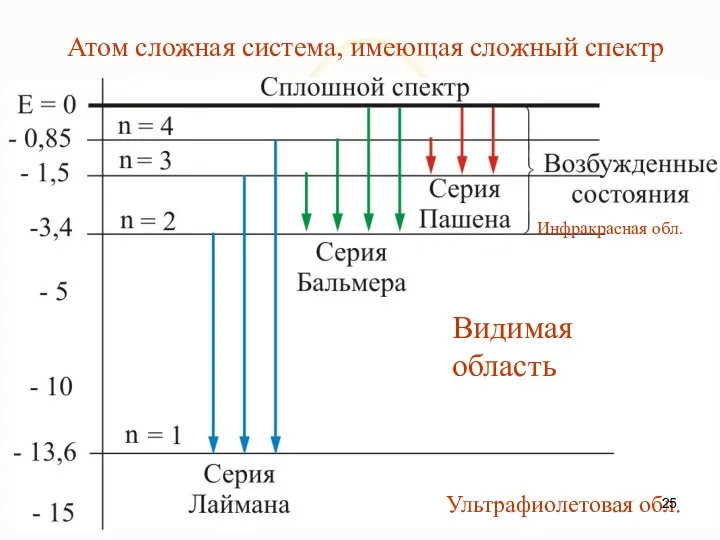
- 25. Атом сложная система, имеющая сложный спектр Видимая область Инфракрасная обл. Ультрафиолетовая обл.
- 26. При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией:
- 27. Серьезным успехом теории Бора явилось: вычисление постоянной Ридберга для водородоподобных систем и объяснение структуры их линейчатых
- 28. Бор теоретически вычислил отношение массы протона к массе электрона mp/me = 1847, это находится в соответствии
- 29. Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. Главнейшее – внутренняя
- 30. Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и правильной
- 31. Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра
- 32. 7.4. Опыт Франка и Герца. Существование дискретных энергетических уровней атома подтверждается опытом Франка и Герца. Немецкие
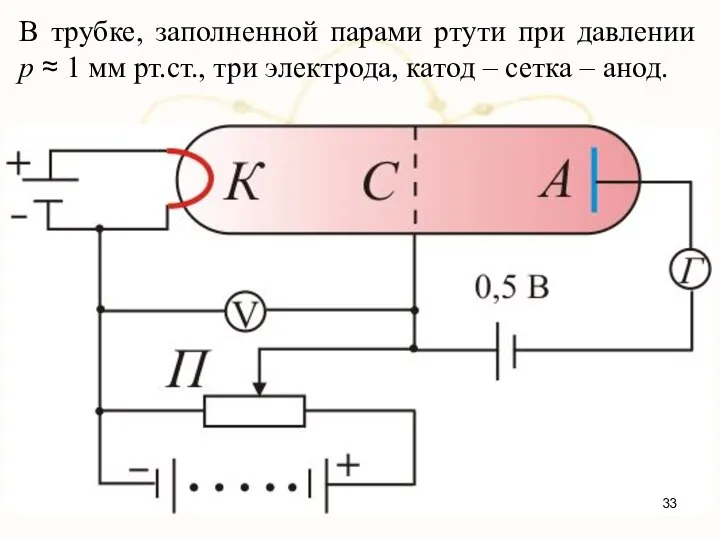
- 33. В трубке, заполненной парами ртути при давлении р ≈ 1 мм рт.ст., три электрода, катод –
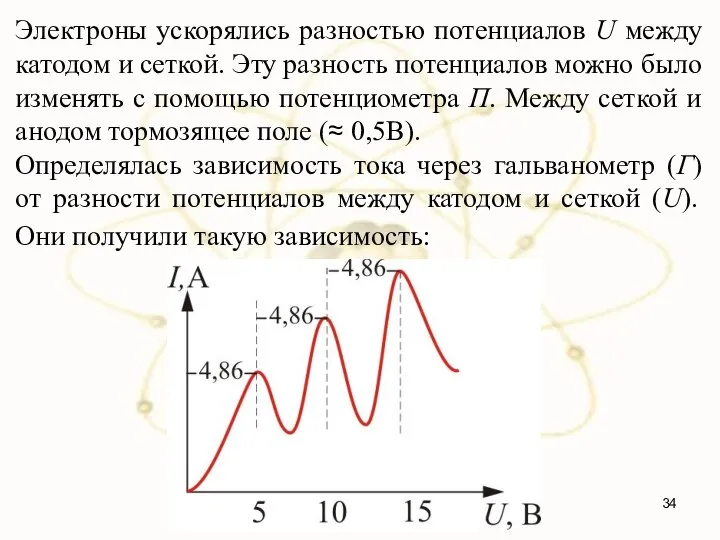
- 34. Электроны ускорялись разностью потенциалов U между катодом и сеткой. Эту разность потенциалов можно было изменять с
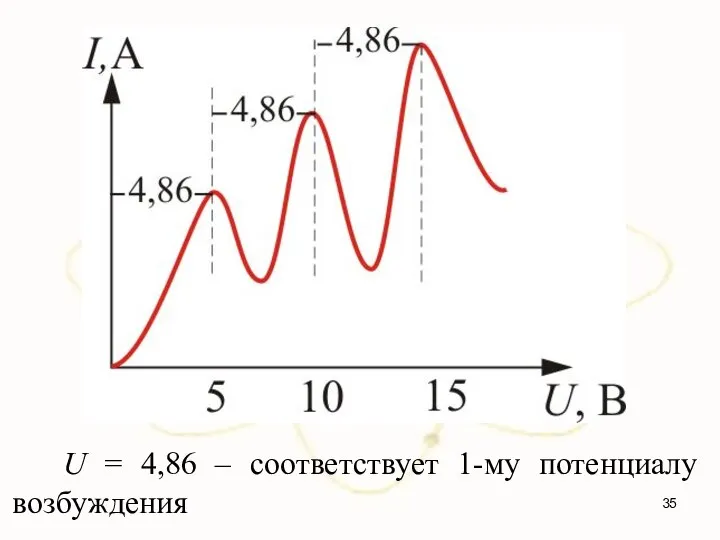
- 35. U = 4,86 – соответствует 1-му потенциалу возбуждения
- 36. Согласно Боровский теории: каждый из атомов ртути может получить лишь вполне определенную энергию, переходя в одно
- 37. Из опыта следует, что при увеличении ускоряющего потенциала вплоть до 4,86 В анодный ток возрастает монотонно,
- 38. Пока разность потенциалов между катодом и сеткой меньше 4,86 В, электроны, встречая на своем пути атомы
- 39. Электроны, потерявшие свою кинетическую энергию уже не смогут преодолеть тормозящий потенциал и достигнуть анода. Этим и
- 40. Таким образом, опыт показал, что электроны передают свою энергию атомам ртути порциями, причем 4,86 эВ –
- 41. Атомы ртути, получившие при соударении с электронами энергию , переходят в возбужденное состояние и должны вернуться
- 43. Скачать презентацию





























 Презентация на тему Импульс Закон сохранения импульса
Презентация на тему Импульс Закон сохранения импульса  Ферромагнитные динамические амортизаторы
Ферромагнитные динамические амортизаторы Последовательное и параллельное соединения проводников
Последовательное и параллельное соединения проводников Электромагнитная индукция
Электромагнитная индукция Решение задач по физике. Задания В-1 - В-14
Решение задач по физике. Задания В-1 - В-14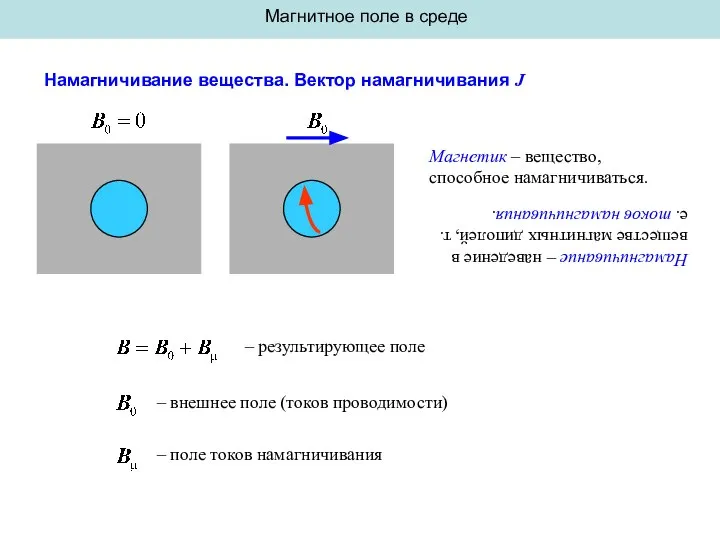 Намагничивание вещества. Вектор намагничивания J
Намагничивание вещества. Вектор намагничивания J ВСР №10. Полупроводниковые приборы
ВСР №10. Полупроводниковые приборы Автопогрузчик H14-80 Evo серия 39X
Автопогрузчик H14-80 Evo серия 39X Движение и его относительность
Движение и его относительность Швейная машина. История создания швейной машины
Швейная машина. История создания швейной машины Презентация на тему Постоянные магниты
Презентация на тему Постоянные магниты  Презентация "Электрические явления" - скачать
Презентация "Электрические явления" - скачать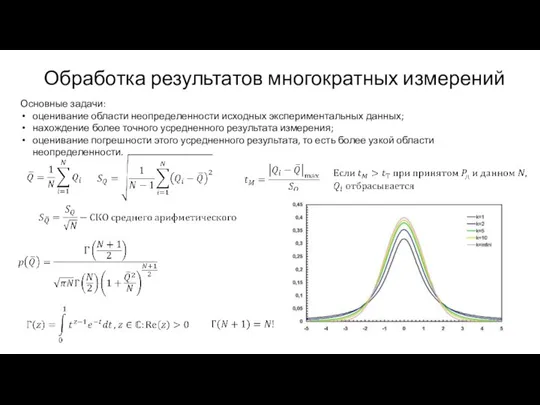 Обработка результатов многократных измерений
Обработка результатов многократных измерений Молниезащита зданий и сооружений
Молниезащита зданий и сооружений Оптимизация корпусов ГТД по массе с обеспечением требований удержания оборвавшейся лопатки
Оптимизация корпусов ГТД по массе с обеспечением требований удержания оборвавшейся лопатки Кипение. Удельная теплота парообразования и конденсации
Кипение. Удельная теплота парообразования и конденсации 2_Волны
2_Волны Prüfen und Einstellen
Prüfen und Einstellen Конструкция самолета и безколлекторный двигатель
Конструкция самолета и безколлекторный двигатель Трение в природе, технике, быту
Трение в природе, технике, быту konspekt (1)
konspekt (1) Свет и цвет. Естествознание, 10 класс
Свет и цвет. Естествознание, 10 класс Механическая работа и мощность
Механическая работа и мощность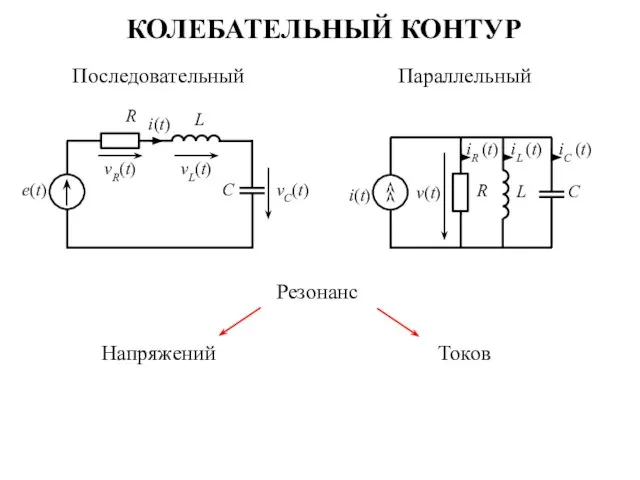 Колебательный контур
Колебательный контур Электродинамика. Электрическая емкость. Конденсаторы. Энергия электрического поля
Электродинамика. Электрическая емкость. Конденсаторы. Энергия электрического поля Домашнее задание по физике
Домашнее задание по физике Парообразование
Парообразование Хроматофокусирование: новые подходы в концентрировании и разделении
Хроматофокусирование: новые подходы в концентрировании и разделении