Содержание
- 2. ЧТОБ ТЕМУ УРОКА УЗНАТЬ , ВАМ НУЖНО ЗАГАДКИ ОТГАДАТЬ. 1. Какой элемент не имеет постоянной прописки
- 3. ОТВЕТЫ ВОДОРОД РадОн НикЕль СеРебро
- 4. ПРОВЕРИМ ЗНАНИЯ В каком году был открыт периодический закон? Дайте современную формулировку периодического закона. Чем отличается
- 5. ВОПРОСЫ 1. В каком году был открыт периодический закон? (1 марта 1869г.) 2. Дайте современную формулировку
- 6. ТЕСТЫ 1. Сколько химических элементов было известно к моменту открытия Периодического закона? а) 18 б)32 в)
- 7. ТЕСТЫ 10. Что означает слово «атом» в переводе с греческого? а) неделимый б) единственный в) нейтральный
- 9. Скачать презентацию
Слайд 2ЧТОБ ТЕМУ УРОКА УЗНАТЬ , ВАМ НУЖНО ЗАГАДКИ ОТГАДАТЬ.
1. Какой элемент не
ЧТОБ ТЕМУ УРОКА УЗНАТЬ , ВАМ НУЖНО ЗАГАДКИ ОТГАДАТЬ.
1. Какой элемент не

имеет постоянной прописки в ПС?
2. Какой элемент всегда рад?
В состав названия, какого металла входит дерево?
Название какого металла имеет кость скелета животного или человека?
2. Какой элемент всегда рад?
В состав названия, какого металла входит дерево?
Название какого металла имеет кость скелета животного или человека?
Слайд 3ОТВЕТЫ
ВОДОРОД
РадОн
НикЕль
СеРебро
ОТВЕТЫ
ВОДОРОД
РадОн
НикЕль
СеРебро

Слайд 4ПРОВЕРИМ ЗНАНИЯ
В каком году был открыт периодический закон?
Дайте современную формулировку
ПРОВЕРИМ ЗНАНИЯ
В каком году был открыт периодический закон?
Дайте современную формулировку

периодического закона.
Чем отличается современная формулировка периодического закона от данной Менделеевым?
Чем отличается современная формулировка периодического закона от данной Менделеевым?
Слайд 5ВОПРОСЫ
1. В каком году был открыт периодический закон? (1 марта 1869г.)
2. Дайте
ВОПРОСЫ
1. В каком году был открыт периодический закон? (1 марта 1869г.)
2. Дайте

современную формулировку периодического закона. (Свойства химических элементов, а также их соединений находятся в периодической зависимости от зарядов ядер атомов.)
3. Чем отличается современная формулировка периодического закона от данной Менделеевым? (За основу Менделеев брал атомный вес элемента.)
3. Чем отличается современная формулировка периодического закона от данной Менделеевым? (За основу Менделеев брал атомный вес элемента.)
Слайд 6ТЕСТЫ
1. Сколько химических элементов было известно к моменту открытия Периодического закона?
а) 18
ТЕСТЫ
1. Сколько химических элементов было известно к моменту открытия Периодического закона?
а) 18

б)32 в) 63 г)98
2. Кто впервые разделил все элементы на металлы и неметаллы?
а) Менделеев б) Берцелиус в) Аристотель г) Томсон
3. На чем основана классификация элементов в Периодической системе?
а) относительные атомные массы элементов б) количество электронов в)название элемента
г) количество нейтронов
3. У каких элементов наиболее ярко выражены металлические свойства?
а) галогены б) металлы побочных подгрупп в) щелочные металлы г) инертные газы
4. Кислотные свойства в периоде увеличиваются
а) не увеличиваются б) изменяются периодически в) справа налево г) слева направо
5. Как изменяются основные свойства в группе сверху вниз?
а) увеличиваются б) уменьшаются в) не изменяются г) изменяются периодически
6. В каком ряду элементов усиляются неметаллические свойства?
а) F, S, As б) Li, Na, K в) Na, Al, Mg г) Br, Cl, F
7. Чем отличаются друг от друга изотопы одного и того же элемента?
а) массовым числом б) зарядом ядра в) номером в таблице г) числом электронов
8. Порядковый номер химического элемента не показывает
а) заряд ядра атома б) количество нейтронов в) количество протонов г) количество электронов
9. Радиус атома увеличивается
а) в группе снизу вверх б) в периоде слева направо в) диагонально г) в периоде справа налево
Слайд 7ТЕСТЫ
10. Что означает слово «атом» в переводе с греческого?
а) неделимый б) единственный
ТЕСТЫ
10. Что означает слово «атом» в переводе с греческого? а) неделимый б) единственный

в) нейтральный г) маленький
11. Какая структура атома была предложена Томсоном?
а) планетарная б) «сливовый пуддинг» в) «шоколадный кекс» г) системная
12. Кто предложил планетарную модель атома?
а) Эйнштейн б) Томсон в) Резерфорд г) Бор
13. В каком году Бор внес квантовые представления в строение атома?
а) 1913 б) 1911 в) 1915 г) 1905
14. Какая орбиталь имеет сферическую форму?
а) s б) p в) d г) f
15. Какую форму имеет р-обиталь?
а) сферическую б) объемного цветка в) шара г) гантели
16. Какое максимальное число электронов может находиться на 3-м энергетическом уровне?
а) 9 б) 32 в) 8 г) 18
17. Чему равно значение главного квантового числа?
а) числу орбиталей б) числу подуровней в) числу электронов г) типу орбитали
18. Какое квантовое число может принимать отрицательные целые значения?
а) магнитное б) орбитальное в) спиновое г) главное
19. Какое квантовое число может принимать только 2 значения?
а) побочное б) главное в) орбитальное г) спиновое
20. В каком атоме полностью завершен второй электронный слой?
а) O б) P в) F г) C
- Предыдущая
Present Simple & Present Continuous (1)Следующая -
Практична робота №1 (1) Пробоотбор и пробоподготовка
Пробоотбор и пробоподготовка Побочная подгруппа VIII группы
Побочная подгруппа VIII группы Periodická tabuľka prvkov PTP
Periodická tabuľka prvkov PTP Практическая работа №5. Качественные реакции на анионы 1-3 групп
Практическая работа №5. Качественные реакции на анионы 1-3 групп Разработка системы подготовки лаборанта химического анализа
Разработка системы подготовки лаборанта химического анализа Презентация на тему Углеродные нанотрубки
Презентация на тему Углеродные нанотрубки  Развитие энергетики и проблемы изменения структуры использования углеводородного сырья
Развитие энергетики и проблемы изменения структуры использования углеводородного сырья Алканы. Зачетная работа
Алканы. Зачетная работа Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Серная кислота
Серная кислота Нейропротекторные функции низкомолекулярных активаторов АМФК
Нейропротекторные функции низкомолекулярных активаторов АМФК Явление хемилюменисценции
Явление хемилюменисценции Щелочные металлы
Щелочные металлы Химические реакции. по фазовому составу
Химические реакции. по фазовому составу Презентация на тему Обобщение сведений об основных классах неорганических веществ
Презентация на тему Обобщение сведений об основных классах неорганических веществ  Свойства солёной воды. Море у меня в стакане
Свойства солёной воды. Море у меня в стакане Раздел 1
Раздел 1 Янтарь
Янтарь Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Лекция № 1
Лекция № 1 Классификация неорганических соединений
Классификация неорганических соединений Термопласты: основные представители, сравнение свойств и область их применения
Термопласты: основные представители, сравнение свойств и область их применения Презентация на тему Химический "Звездный час"
Презентация на тему Химический "Звездный час"  Алкины
Алкины Строение вещества
Строение вещества Относительная атомная масса. Массы атомов
Относительная атомная масса. Массы атомов Материальные и энергетические балансы. Тема 2
Материальные и энергетические балансы. Тема 2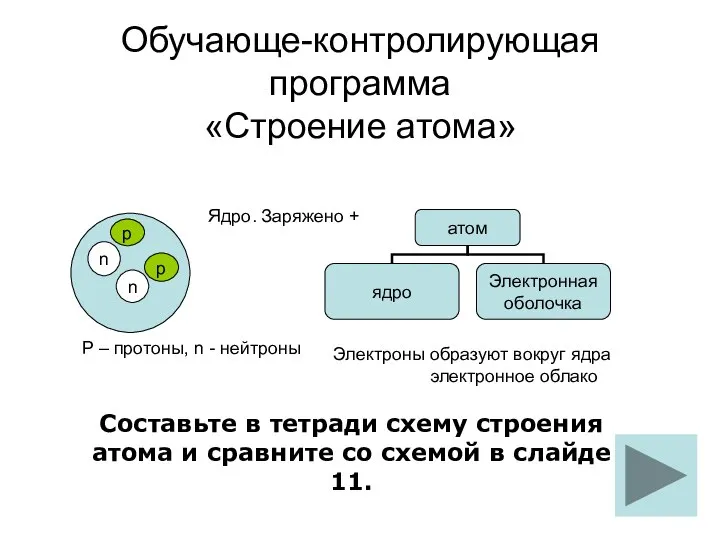 строение атома обуч-контр прогр
строение атома обуч-контр прогр