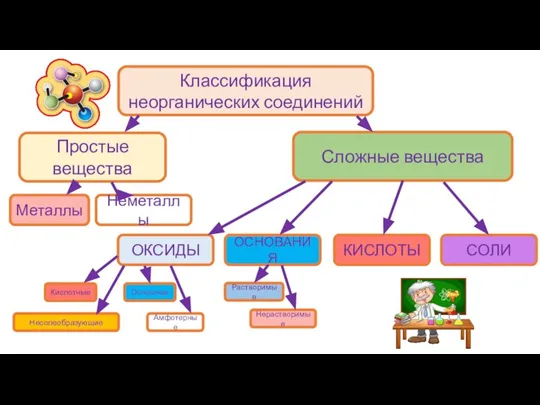
Слайд 3Классификация неорганических соединений
Простые вещества
Сложные вещества
Металлы
Неметаллы
ОКСИДЫ
ОСНОВАНИЯ
КИСЛОТЫ
СОЛИ
Кислотные
Основные
Амфотерные
Несолеобразующие
Растворимые
Нерастворимые
Слайд 4Химические свойства оксидов
Кислотные
Основные
Амфотерные
Несолеобразующие оксиды: NO, CO, N2O, SiO
(не проявляют характерных основных или

кислотных свойств,
им не соответствуют гидроксиды)
Слайд 5Химические свойства кислот
Выучить формулы и названия неорганических кислот!!!
Первое правило ряда напряжений (активности):
С

растворами кислот взаимодействуют металлы, которые расположены левее водорода
Слайд 6Химические свойства оснований
Запомни:
Водный раствор аммиака NH3 H2O – основание, образует сложный однозарядный

катион аммония NH4 и существует только в растворе (нашатырный спирт). Он легко разлагается на аммиак и воду!
Слайд 7Химические свойства солей
Второе правило ряда напряжений (активности):
Каждый металл вытесняет из растворов солей

все другие металлы, расположенные правее его в ряду напряжений.
Условия протекания реакции:
А) Обе соли должны быть растворимы.
Б) Металлы не должны взаимодействовать с водой
(поэтому металлы 1 и 2 групп главных подгрупп не вытесняют другие металлы из растворов солей)






 Цианоакрилатовая камера для выявления жировых следов
Цианоакрилатовая камера для выявления жировых следов Кислоты. состав, номенклатура и их их классификация
Кислоты. состав, номенклатура и их их классификация Судьба углеродного скелета аминокислот
Судьба углеродного скелета аминокислот Строение атома
Строение атома Техника безопасности при использовании различных видов топлива. Практическая работа № 3
Техника безопасности при использовании различных видов топлива. Практическая работа № 3 Общие свойства неметаллов
Общие свойства неметаллов Пиримидин (шестичленный гетероцикл с двумя атомами азота)
Пиримидин (шестичленный гетероцикл с двумя атомами азота) Презентация на тему Соли: свойства, получение, применение (8 класс)
Презентация на тему Соли: свойства, получение, применение (8 класс)  Презентация на тему Применение кислорода
Презентация на тему Применение кислорода  Презентация на тему Кремний в природе
Презентация на тему Кремний в природе  Неорганические вещества
Неорганические вещества Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Презентация на тему Жиры, их строение и свойства
Презентация на тему Жиры, их строение и свойства  Horenie
Horenie Основания. 8 класс
Основания. 8 класс Ионная связь
Ионная связь Презентация по Химии "Строении атомов. Химическая связь"
Презентация по Химии "Строении атомов. Химическая связь"  Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева
Галогены. Элементы главной подгруппы 7 группы Периодической системы Менделеева Простые вещества - неметаллы
Простые вещества - неметаллы Пропи́н (метилацетилен, аллилен)
Пропи́н (метилацетилен, аллилен) Практическая работа №5. Качественные реакции на анионы 1-3 групп
Практическая работа №5. Качественные реакции на анионы 1-3 групп Кислоты основания и соли как электролиты
Кислоты основания и соли как электролиты Тотығу - тотықсыздану реакциясы
Тотығу - тотықсыздану реакциясы Физико-химические свойства растворов ВМС
Физико-химические свойства растворов ВМС Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В.
Учитель химии МАОУ СОШ № 61 города Тюмени Белова Н.В. Основные классы неорганических веществ
Основные классы неорганических веществ Презентация на тему Соли
Презентация на тему Соли