Содержание
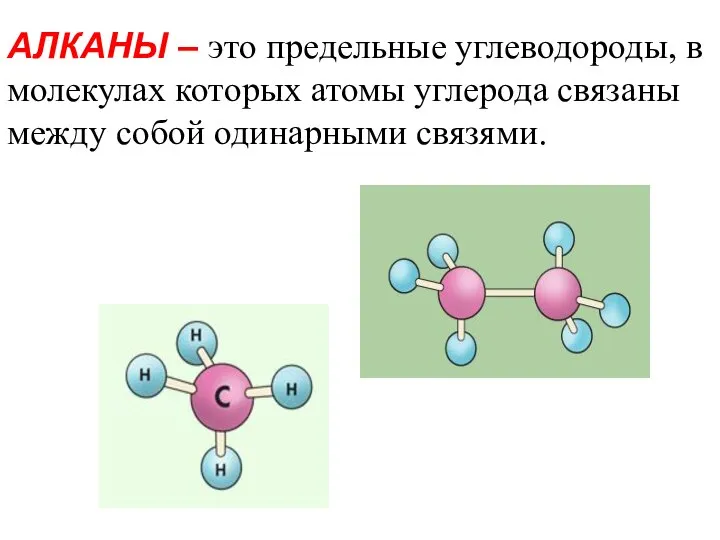
- 2. АЛКАНЫ – это предельные углеводороды, в молекулах которых атомы углерода связаны между собой одинарными связями.
- 3. Общая формула СnH2n+2 , где n=1,2,3…
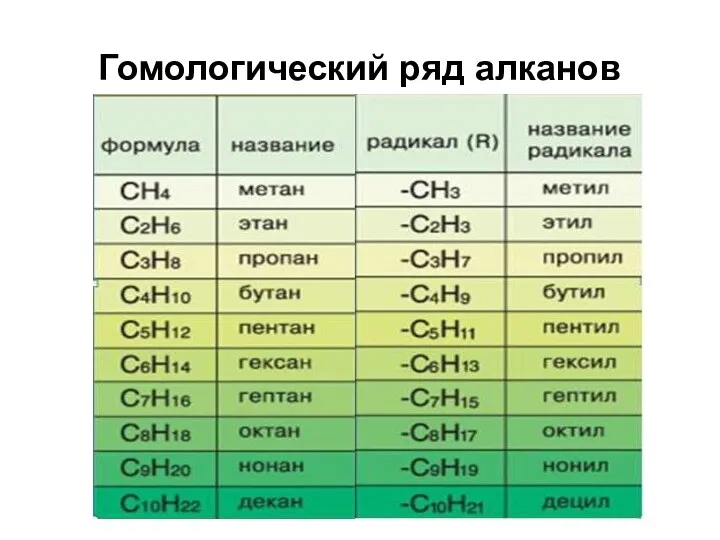
- 4. Гомологический ряд алканов
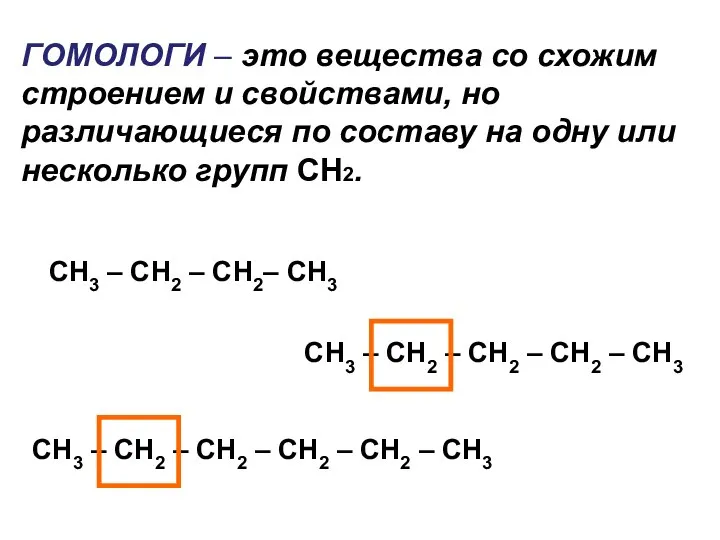
- 5. ГОМОЛОГИ – это вещества со схожим строением и свойствами, но различающиеся по составу на одну или
- 6. ИЗОМЕРЫ – вещества, имеющие одинаковый состав молекул, но различное химическое строение и обладающие поэтому разными свойствами.
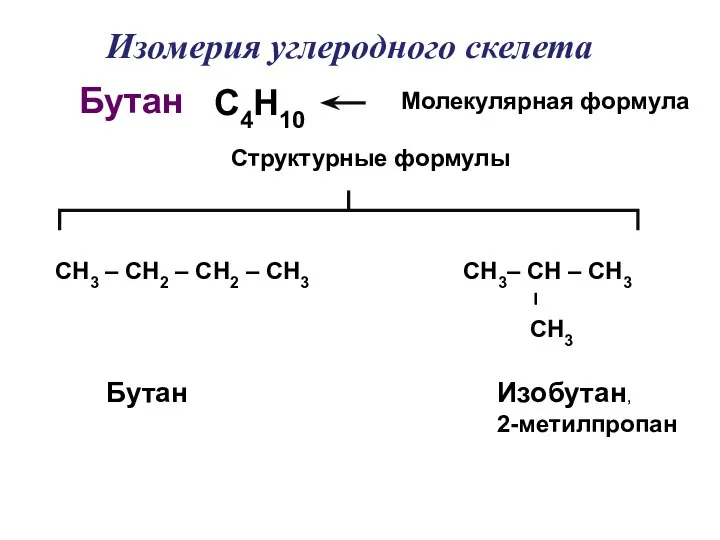
- 7. С4Н10 СН3 – СН2 – СН2 – СН3 Молекулярная формула Структурные формулы Бутан Бутан Изобутан, 2-метилпропан
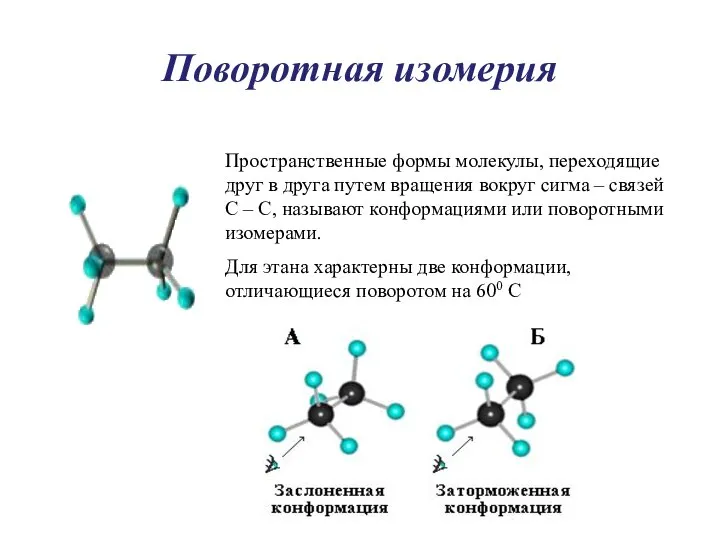
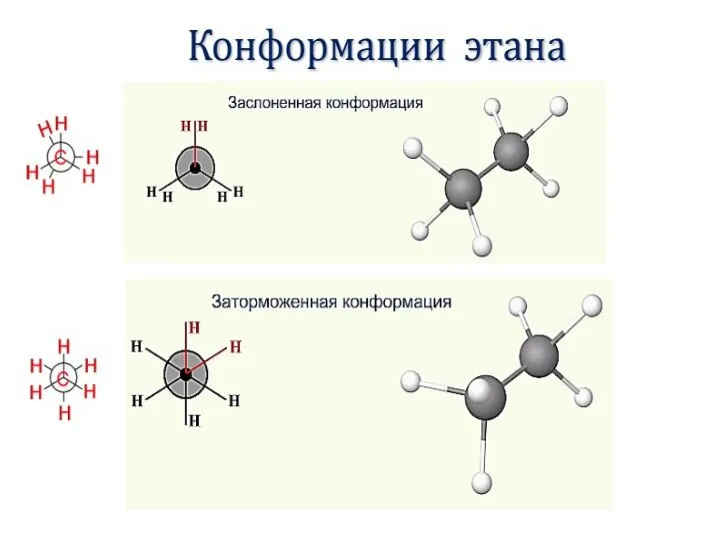
- 8. Поворотная изомерия Пространственные формы молекулы, переходящие друг в друга путем вращения вокруг сигма – связей С
- 10. Зеркальная изомерия (оптическая) Если атом углерода связан с четырьмя другими атомами, то возможно существование двух соединений
- 11. НОМЕНКЛАТУРА АЛКАНОВ Алгоритм: Выбор главной, самой длинной цепи: CH3 – CH - CH2 - CH3 │
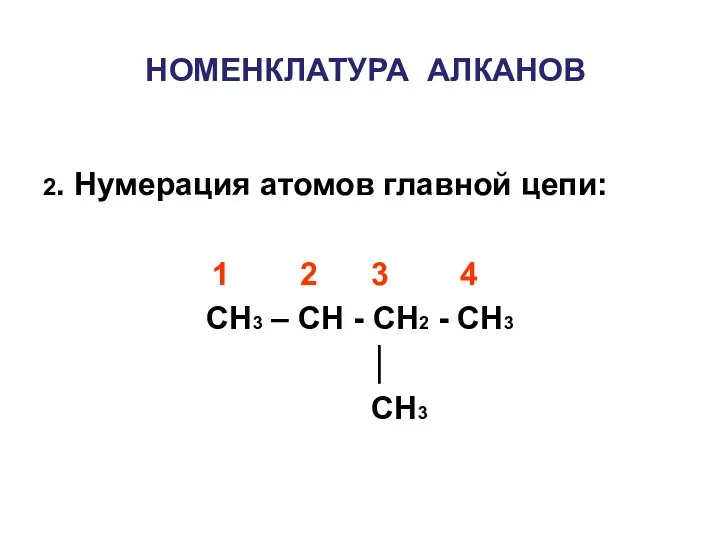
- 12. НОМЕНКЛАТУРА АЛКАНОВ 2. Нумерация атомов главной цепи: 1 2 3 4 CH3 – CH - CH2
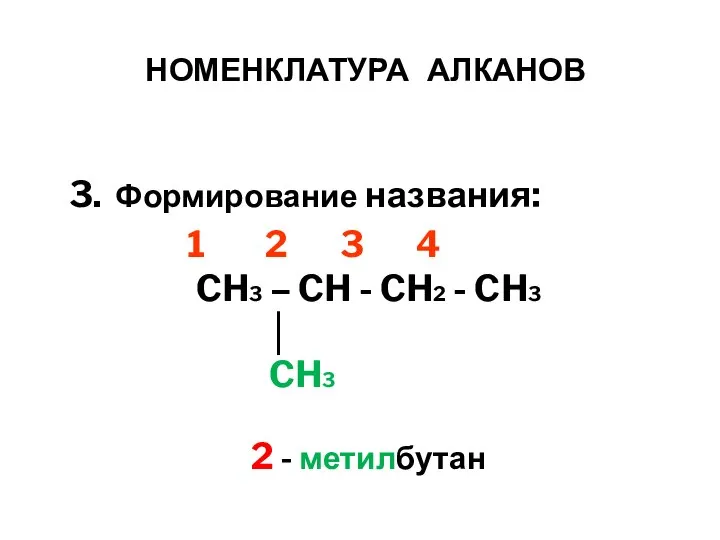
- 13. НОМЕНКЛАТУРА АЛКАНОВ 3. Формирование названия: 1 2 3 4 CH3 – CH - CH2 - CH3
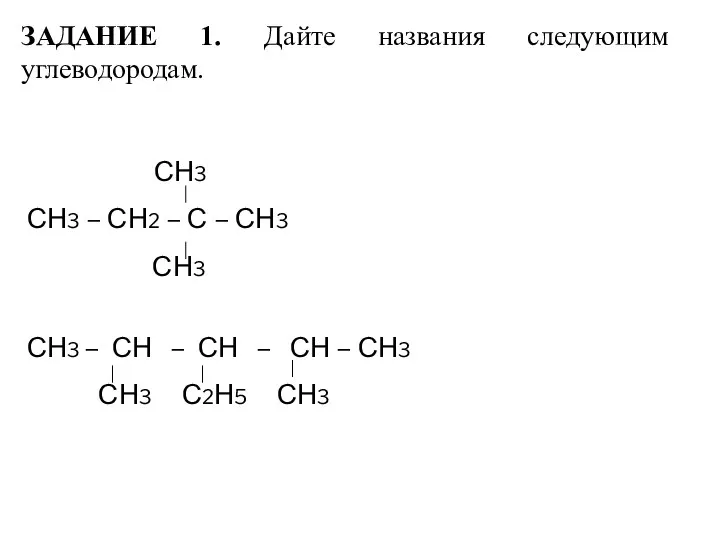
- 14. ЗАДАНИЕ 1. Дайте названия следующим углеводородам. СН3 СН3 – СН2 – С – СН3 СН3 СН3
- 15. СН3 І СН3 –СН2 – С – СН2 –СН3 І І СН3 СН3
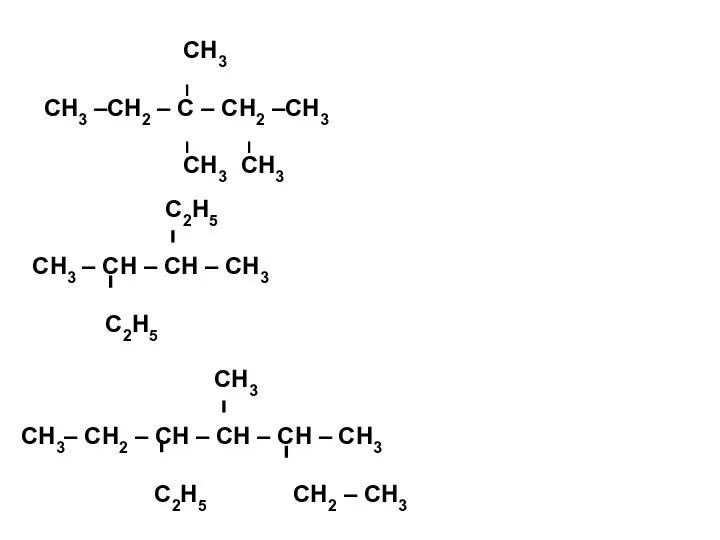
- 16. ЗАДАНИЕ 2. Составьте структурные формулы следующих веществ: 1. 2,3 – диметилпентан; 2. 3,3,4 – триметилгексан; 3.
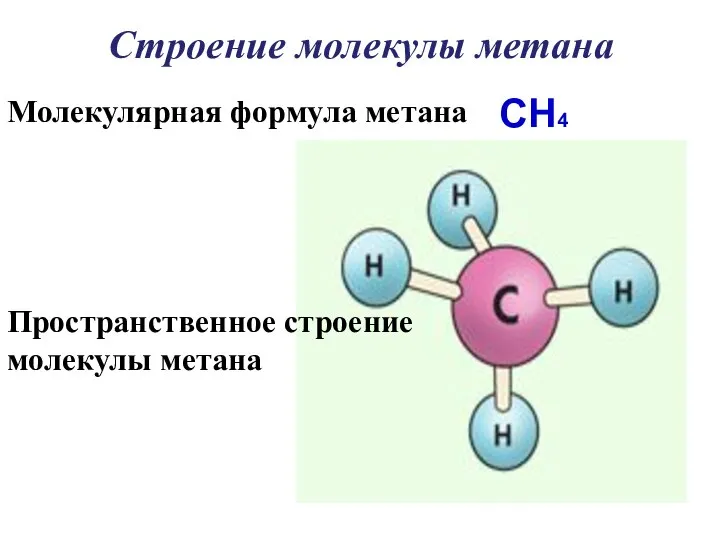
- 17. Строение молекулы метана Молекулярная формула метана CH4 Пространственное строение молекулы метана
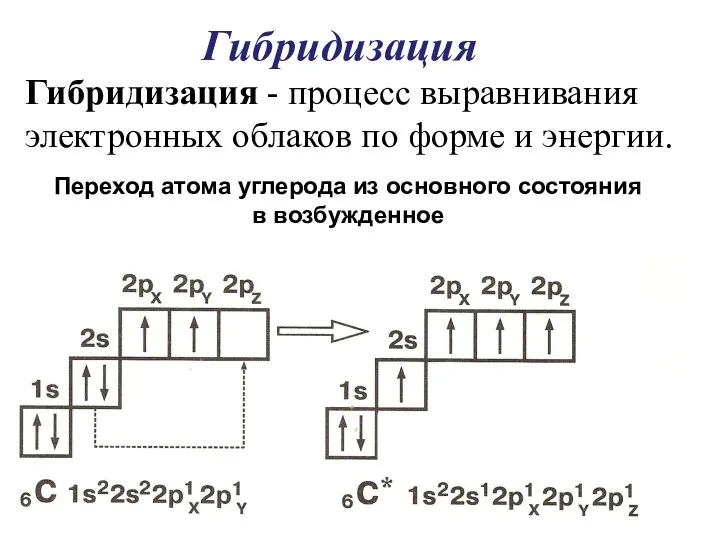
- 18. Гибридизация Переход атома углерода из основного состояния в возбужденное Гибридизация - процесс выравнивания электронных облаков по
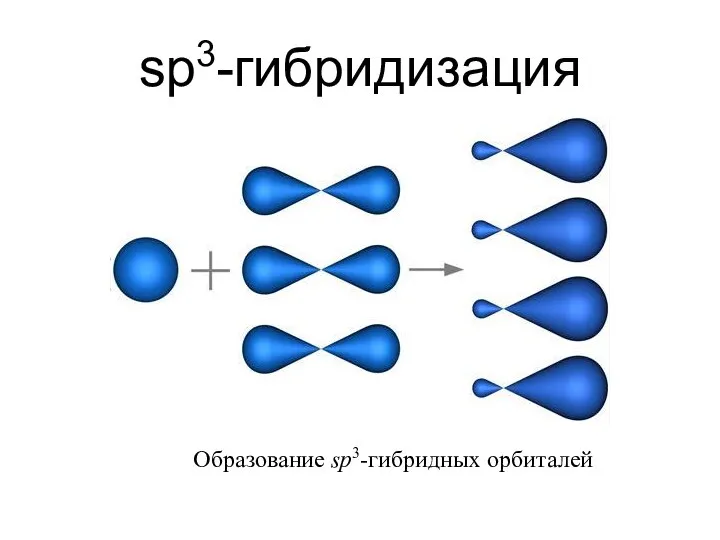
- 19. sp3-гибридизация Образование sp3-гибридных орбиталей
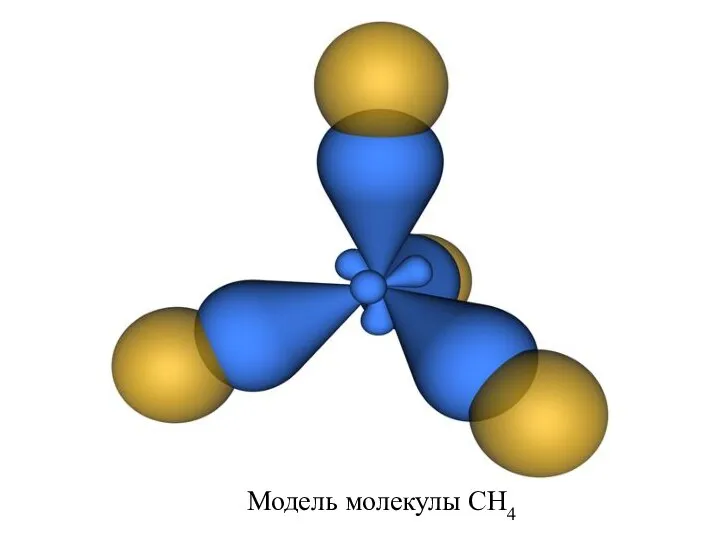
- 20. Модель молекулы CH4
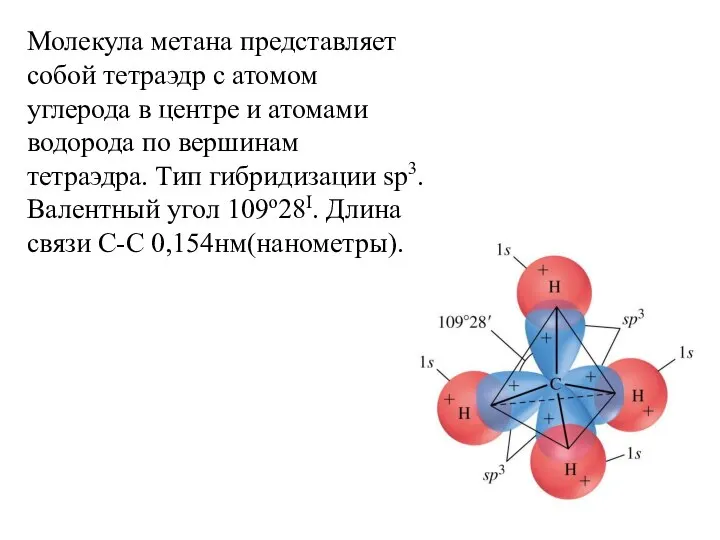
- 21. Молекула метана представляет собой тетраэдр с атомом углерода в центре и атомами водорода по вершинам тетраэдра.
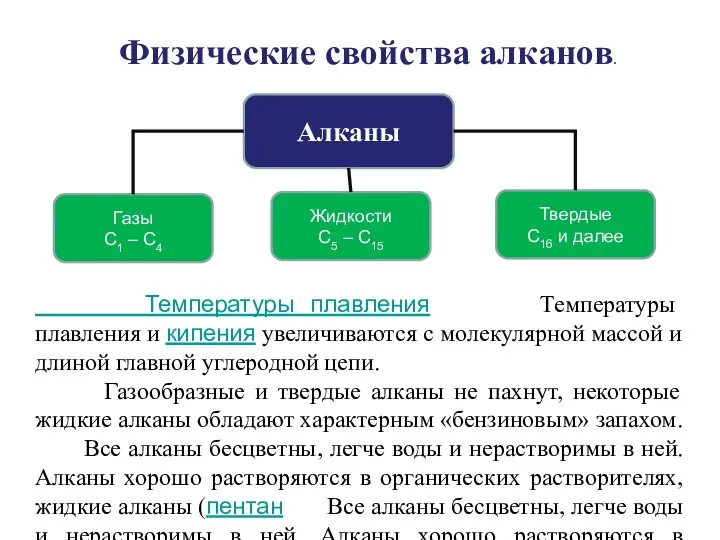
- 22. Алканы Жидкости С5 – С15 Газы С1 – С4 Твердые С16 и далее Физические свойства алканов.
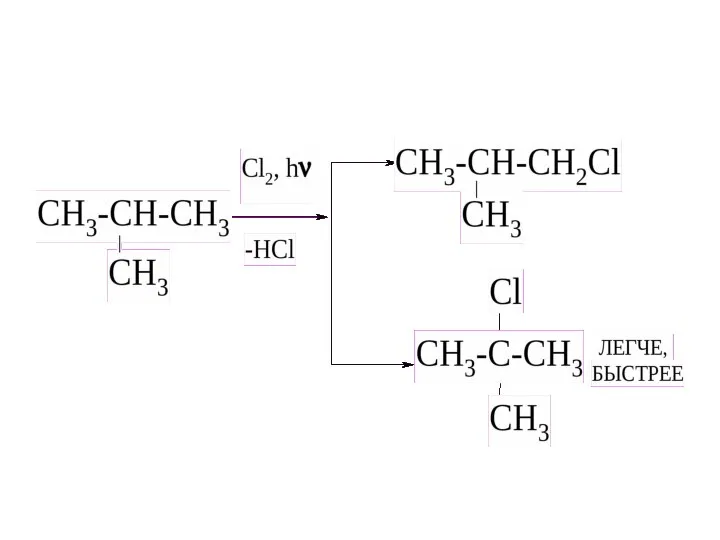
- 23. 1. Реакции замещения Протекают по механизму радикального замещения. а) с галогенами (с Cl2 – на свету,
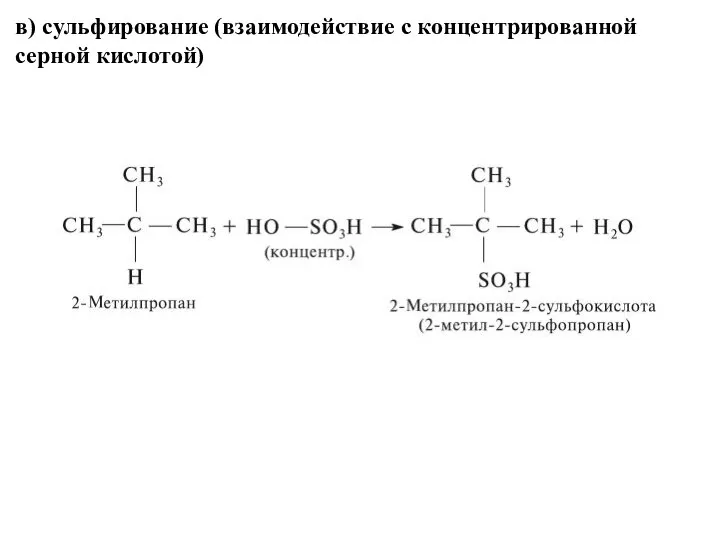
- 27. в) сульфирование (взаимодействие с концентрированной серной кислотой)
- 28. 2. Реакции окисления CnH2n+2 + (3n+1)/2O2 → nCO2 + (n+1)H2O CH4 + 2O2 → CO2 +
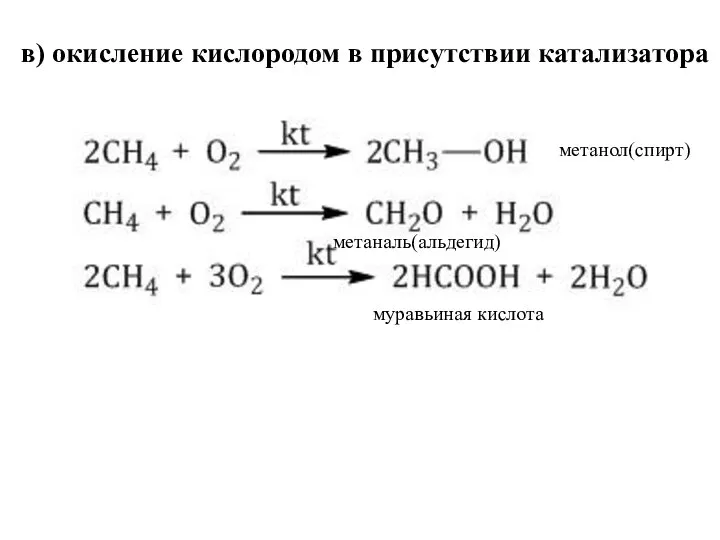
- 29. в) окисление кислородом в присутствии катализатора метанол(спирт) метаналь(альдегид) муравьиная кислота
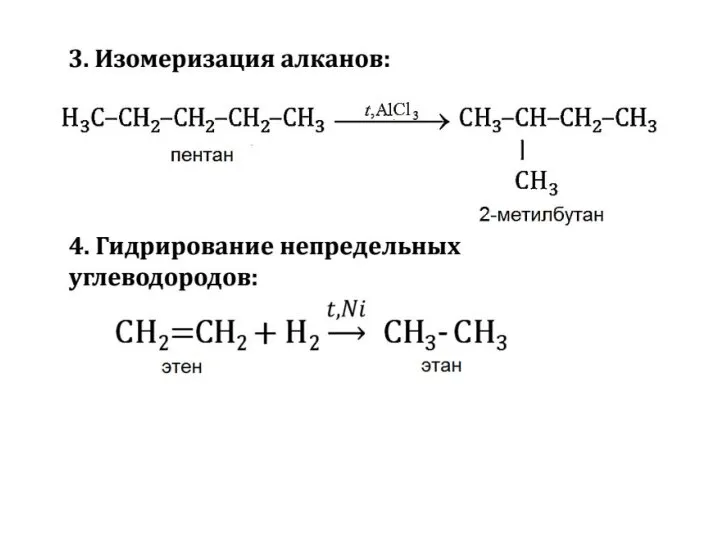
- 30. 3. Термические превращения алканов а) дегидрирование(отщепление водорода) в присутствии катализатора при высоких температурах : CH3 –
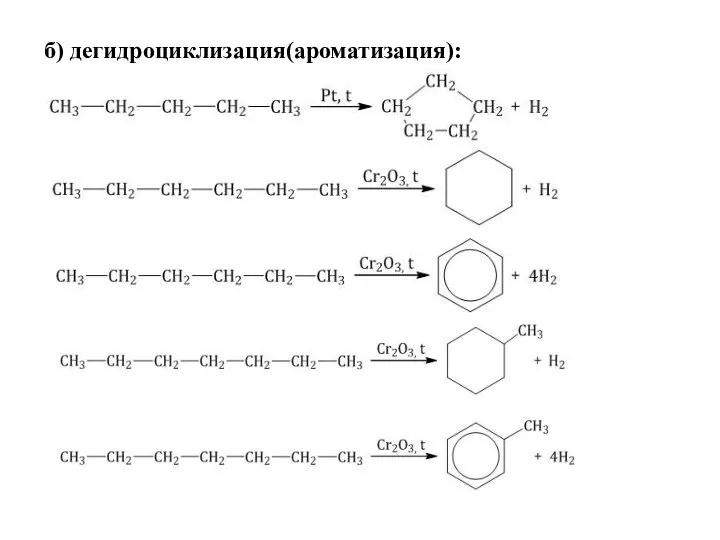
- 31. б) дегидроциклизация(ароматизация):
- 32. в) крекинг - это реакция разложения алкана с длинной углеродной цепью на алканы и алкены с
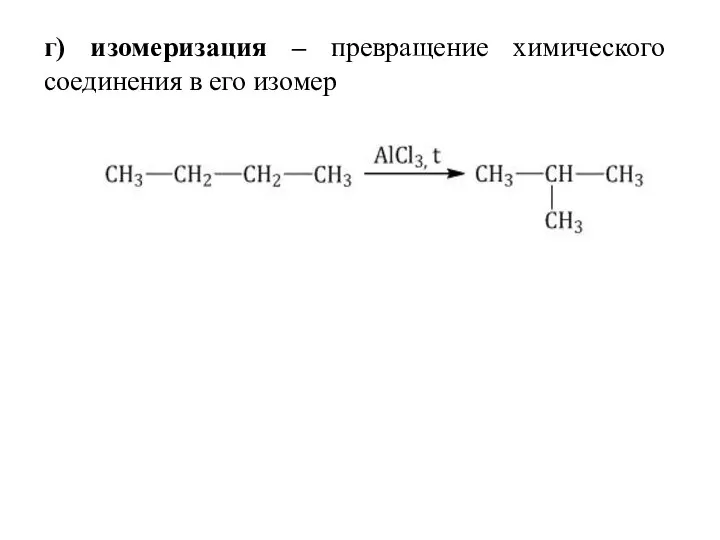
- 33. г) изомеризация – превращение химического соединения в его изомер
- 34. Способы получения
- 36. 1926г. Фишер-Тропш
- 40. Задания для самостоятельной работы: Задание 1. Назовите вещества
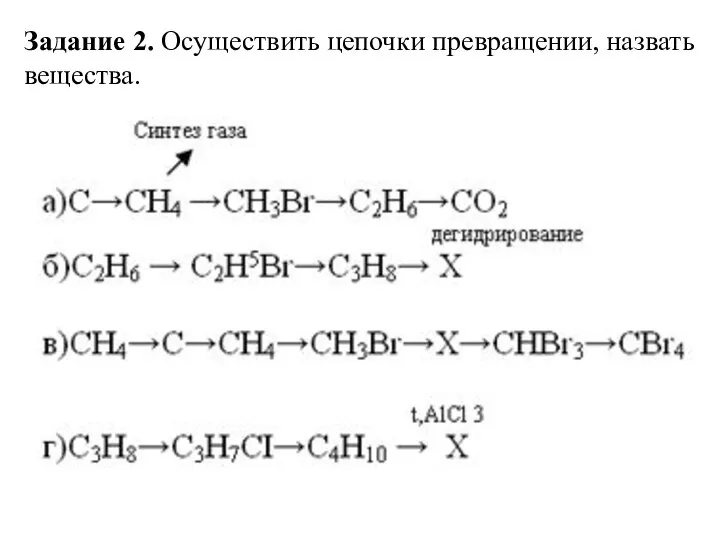
- 41. Задание 2. Осуществить цепочки превращении, назвать вещества.
- 42. Домашние задание
- 44. Скачать презентацию


















 О чем не узнаешь на уроке
О чем не узнаешь на уроке Обобщение сведений об основных классах неорганических веществ. 8 класс
Обобщение сведений об основных классах неорганических веществ. 8 класс Скорость химических реакций. Факторы, влияющие на скорость химической реакции
Скорость химических реакций. Факторы, влияющие на скорость химической реакции Кислородные соединения углерода
Кислородные соединения углерода Сущность химических реакций и признаки их протекания
Сущность химических реакций и признаки их протекания Свойства аминов
Свойства аминов Презентация на тему Дисперсные системы и растворы
Презентация на тему Дисперсные системы и растворы 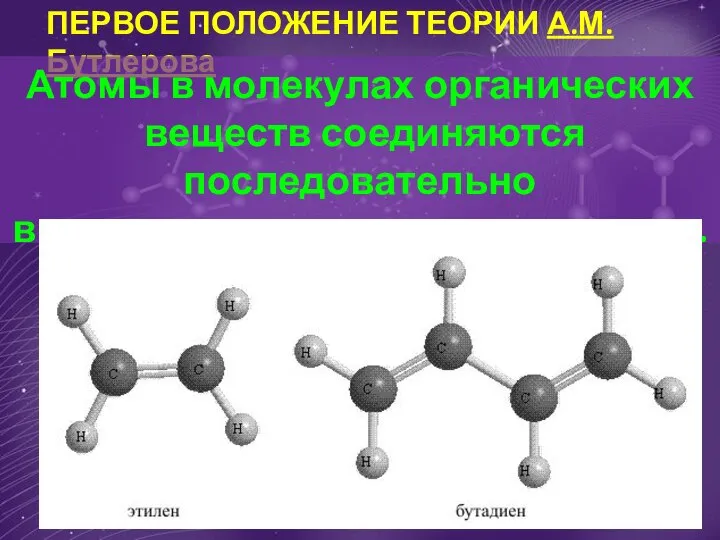 Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно
Первое положение теории А.М. Бутлерова Атомы в молекулах органических веществ соединяются последовательно Простые и сложные вещества
Простые и сложные вещества Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4
Комплексное изучение системы NiO-ZnO-CoO с целью модифицирования свойств исходной матрицы никель-цинкового феррита xZnxFe2O4 Свойства алкенов
Свойства алкенов Относительная молекулярная масса вещества
Относительная молекулярная масса вещества Витамины и их роль в жизни людей
Витамины и их роль в жизни людей Основные сведения о строении атома
Основные сведения о строении атома Метод окислительно - восстановительного титрования
Метод окислительно - восстановительного титрования Здравствуйте, химия! Что изучает химия
Здравствуйте, химия! Что изучает химия G11. Химический состав
G11. Химический состав Особо чистые вещества. Занятие 12
Особо чистые вещества. Занятие 12 Бишофит - новый старый антигололедный реагент
Бишофит - новый старый антигололедный реагент Типы химических связей
Типы химических связей Физическая химия, термодинамика
Физическая химия, термодинамика Уравнения химических реакций
Уравнения химических реакций Химические структуры
Химические структуры teoria_Butlerova
teoria_Butlerova Тренажёр: знаки химических элементов
Тренажёр: знаки химических элементов Получение функциональных плёнок на основе TiO2
Получение функциональных плёнок на основе TiO2 Гармонизации терминологии аналитической химии с использованием электронной системы на основе MS WSS (Windows SharePoint Services) Широкова В.И.,
Гармонизации терминологии аналитической химии с использованием электронной системы на основе MS WSS (Windows SharePoint Services) Широкова В.И.,  Производство органических препаратов ароматического ряда
Производство органических препаратов ароматического ряда