Содержание
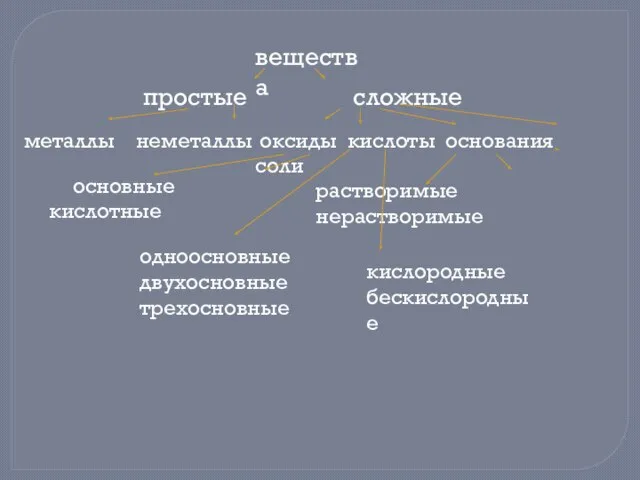
- 2. вещества простые сложные металлы неметаллы оксиды кислоты основания соли основные кислотные растворимые нерастворимые одноосновные двухосновные трехосновные
- 3. Распределить вещества по классам K2CO3, BaO, Ca(OH)2, H3PO4, CuCl2, SO3 , H2S, LiOH, Na2O, Mg(OH)2, HNO3,
- 4. С какими из предложенных веществ будет реагировать: а) серная кислота б) гидроксид калия: BaCl2, CuO, H2O,
- 5. А) H2SO4 + BaCl2 → BaSO4↓ + 2HCl CuO + H2SO4 → CuSO4 + H2O Ca(OH)2
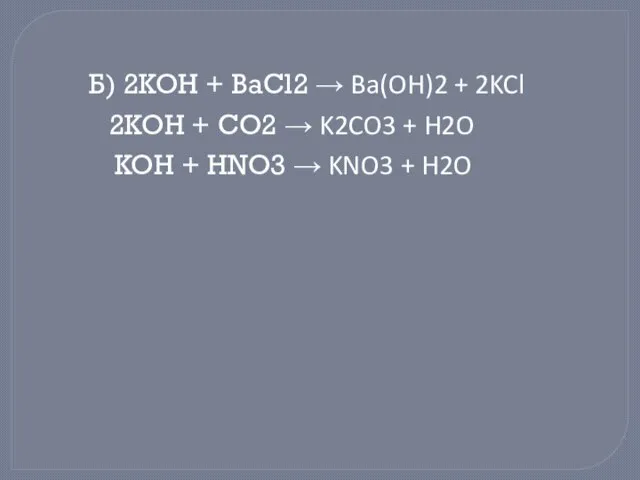
- 6. Б) 2KOH + BaCl2 → Ba(OH)2 + 2KCl 2KOH + CO2 → K2CO3 + H2O KOH
- 7. Цепочка превращений Ba → Ba(OH)2 → Cu(OH)2 → CuO → Cu(NO3)2 → Cu(OH)2 Ba + 2H2O
- 9. Скачать презентацию




 Атом
Атом Презентация 1
Презентация 1 Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Получение аминов
Получение аминов Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Оксиды, их классификация и химические свойства. 8 класс
Оксиды, их классификация и химические свойства. 8 класс Строение вещества
Строение вещества Виды химической связи. Обобщение и систематизация знаний
Виды химической связи. Обобщение и систематизация знаний Химические реакции
Химические реакции Морфологогия минералов
Морфологогия минералов Природа и типы химических связей
Природа и типы химических связей Презентация на тему Вещества и их свойства
Презентация на тему Вещества и их свойства  ВКР: Определение показателей качества мясной и колбасной продукции различных производителей
ВКР: Определение показателей качества мясной и колбасной продукции различных производителей Презентация на тему Физические и химические явления 8 класс
Презентация на тему Физические и химические явления 8 класс  Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Халькогены
Презентация на тему Халькогены  Азотная кислота
Азотная кислота Метелёва И.Е. учитель химии
Метелёва И.Е. учитель химии Решение заданий ОГЭ по химии (1 - 15)
Решение заданий ОГЭ по химии (1 - 15) Химия и производство
Химия и производство Алканы
Алканы Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Салициловая кислота
Салициловая кислота Масляная кислота
Масляная кислота Кумарон - индендық полимерлер
Кумарон - индендық полимерлер Классификация химических реакций
Классификация химических реакций Нефть
Нефть Водородная химическая связь
Водородная химическая связь