Содержание
- 2. План: Скорость химической реакции Гетерогенные и гомогенные реакции Зависимость скорости реакции от различных факторов: Природа реагирующих
- 3. Скорость химической реакции Обозначается ν 1 моль/л∙с 1 кмоль/м3∙мин определяется изменением концентрации одного из реагирующих веществ
- 4. Раздел химии, изучающий скорость химической реакции, называется химической кинетикой.
- 5. Гетерогенные реакции Это реакции идущие между веществами в неоднородной среде. Например, на поверхности соприкосновения твердого вещества
- 6. Гомогенные реакции Это реакции протекающие в однородной среде(нет поверхности раздела реагирующих веществ). Например в смеси газов
- 7. Факторы, влияющие на скорость химической реакции природа реагирующих веществ; концентрация реагирующих веществ поверхность соприкосновения реагирующих веществ
- 8. 1. Природа реагирующих веществ. Под природой реагирующих веществ понимают их состав, строение, взаимное влияние атомов в
- 9. Теория столкновений. Основная идея теории: реакции происходят при столкновении частиц реагентов, которые обладают определённой энергией. Чем
- 10. 2. Концентрации реагирующих веществ. На основе большого экспериментального материала в 1867 г. норвежские учёные К. Гульдберг,
- 11. Закон действующих масс. Гульдберг (1836-1902). Норвежский физикохимик. П. Вааге (1833-1900). Норвежский ученый. V=kcAacBb Скорость химической реакции
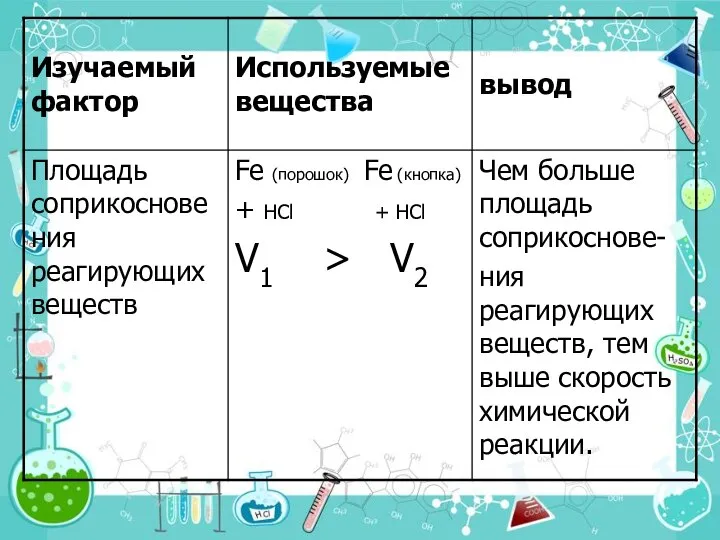
- 12. 3.Поверхность соприкосновения реагирующих веществ. Скорость реакции увеличивается благодаря: -увеличению площади поверхности соприкосновения реагентов (измельчение); -повышению реакционной
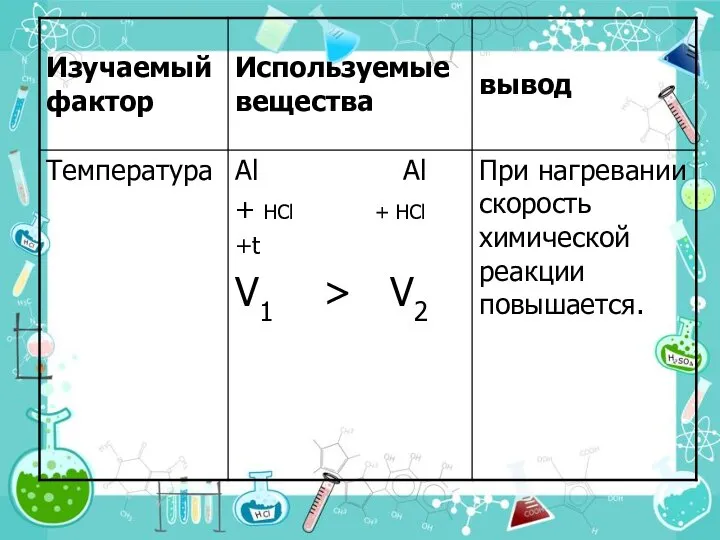
- 14. 4. Температура При увеличении температуры на каждые 10° С общее число столкновений увеличивается только на ~
- 15. Правило Вант-Гоффа Я. Вант-Гофф (1852 -1911). Голландский химик. Один из основателей физической химии и стереохимии При
- 17. 5. Действие катализатора Можно изменить скорость реакции, используя специальные вещества, которые изменяют механизм реакции и направляют
- 18. Различают два вида катализа: Гомогенный катализ, при котором и катализатор, и реагирующие вещества находятся в одном
- 21. Скачать презентацию
















 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)