Содержание
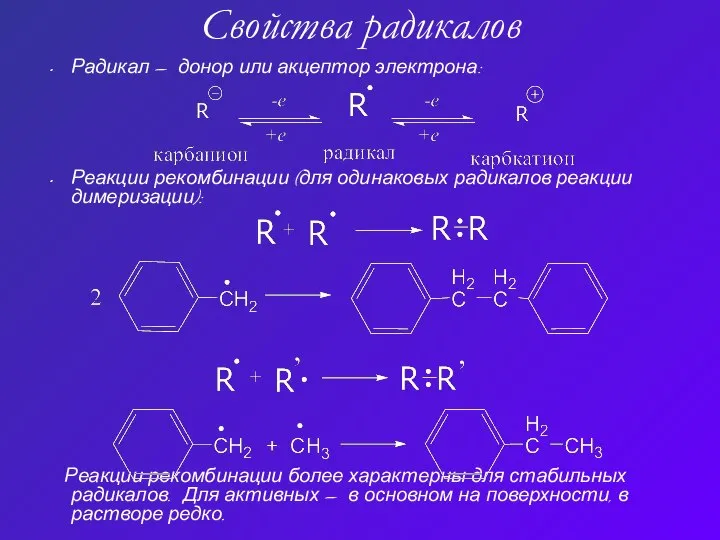
- 2. Свойства радикалов Радикал – донор или акцептор электрона: Реакции рекомбинации (для одинаковых радикалов реакции димеризации): Реакции
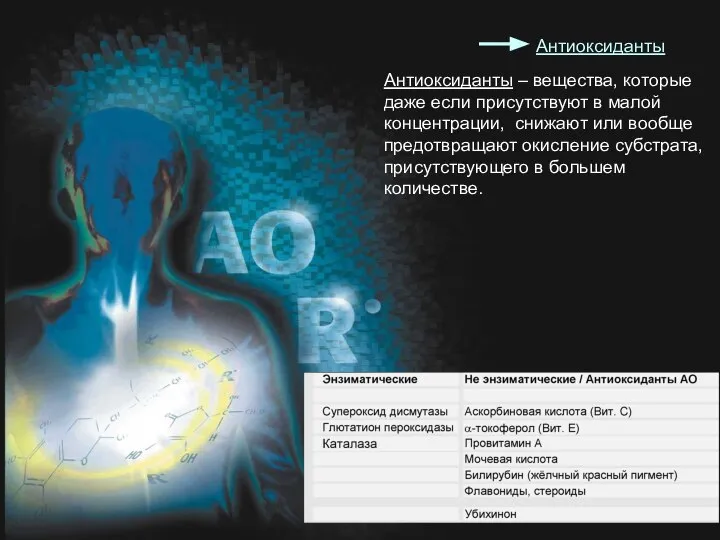
- 3. Антиоксиданты Антиоксиданты – вещества, которые даже если присутствуют в малой концентрации, снижают или вообще предотвращают окисление
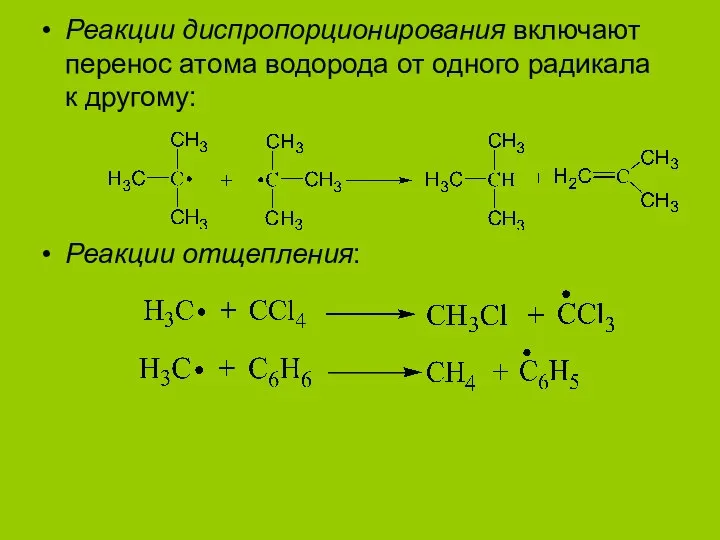
- 4. Реакции диспропорционирования включают перенос атома водорода от одного радикала к другому: Реакции отщепления:
- 5. Ион-радикалы Ион –радикалы – одновременно несут заряд и неспаренный электрон Анион-радикалы образуются при одноэлектронном восстановлении нейтральных
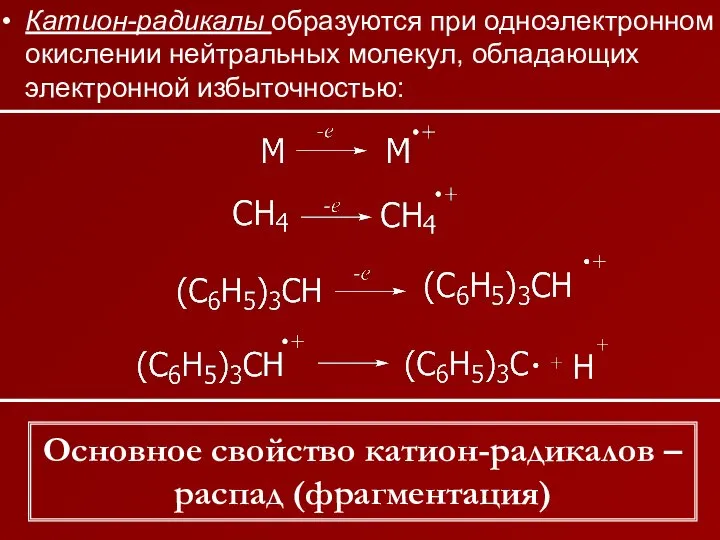
- 6. Катион-радикалы образуются при одноэлектронном окислении нейтральных молекул, обладающих электронной избыточностью: Основное свойство катион-радикалов – распад (фрагментация)
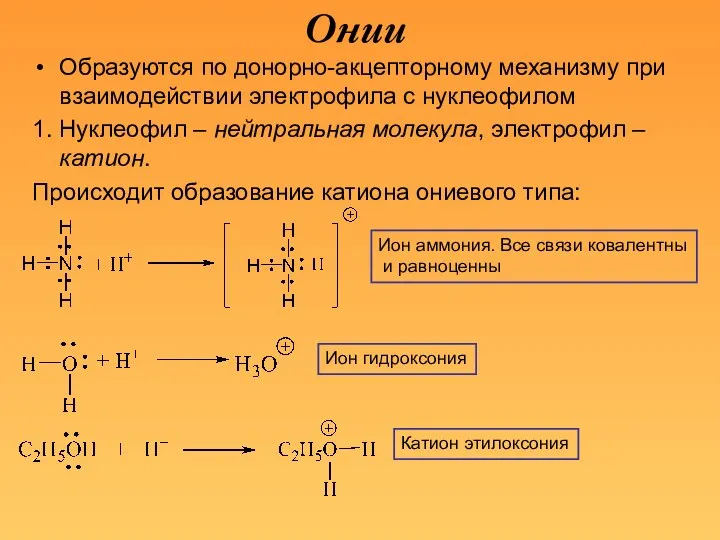
- 7. Онии Образуются по донорно-акцепторному механизму при взаимодействии электрофила с нуклеофилом 1. Нуклеофил – нейтральная молекула, электрофил
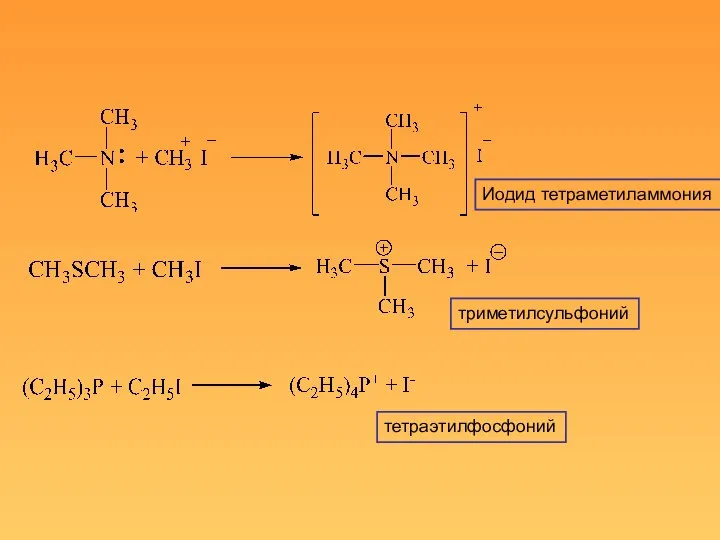
- 8. Иодид тетраметиламмония триметилсульфоний тетраэтилфосфоний
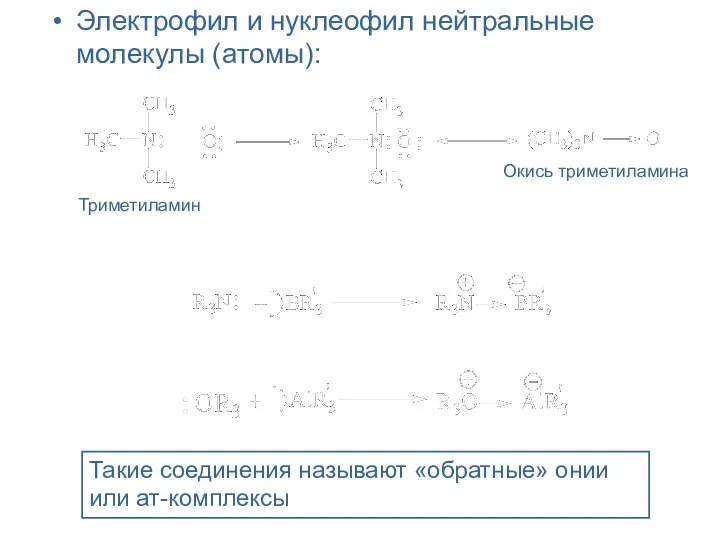
- 9. Электрофил и нуклеофил нейтральные молекулы (атомы): Триметиламин Окись триметиламина Такие соединения называют «обратные» онии или ат-комплексы
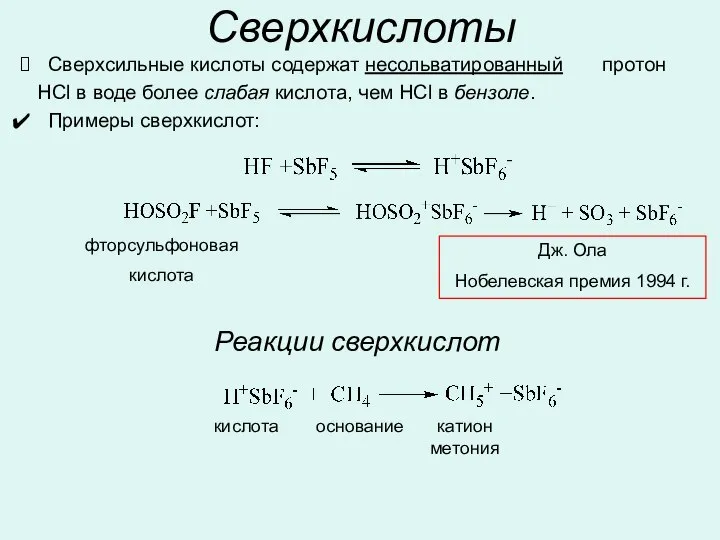
- 10. Сверхкислоты Сверхсильные кислоты содержат несольватированный протон HCl в воде более слабая кислота, чем HCl в бензоле.
- 11. Алканы (СnH2n+2) Насыщенные углеводороды (парафины) sp3-конфигурация
- 13. Номенклатура А) Тривиальная (эмпирическая) – исторически сложившаяся Б) Рациональная Основной принцип – обозначение всех изомеров углеводородов
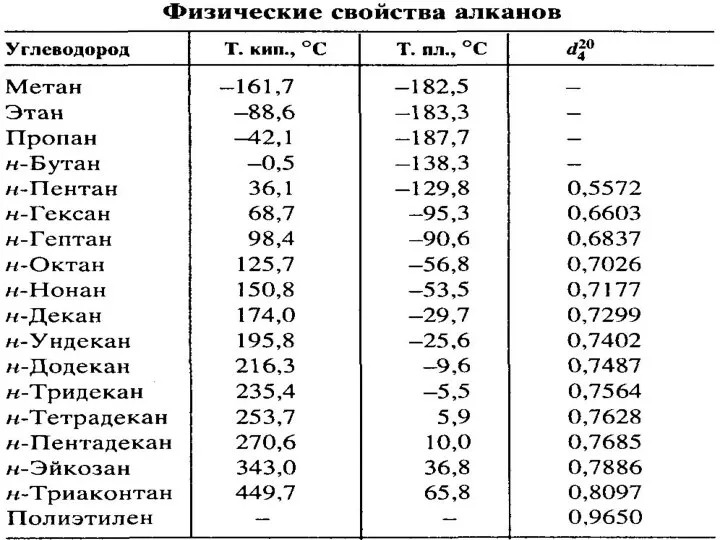
- 15. Молекула метана представляет собой тетраэдр. Это жесткая конструкция. Расстояние C-H = 1,1 Å (данные РСА). Длина
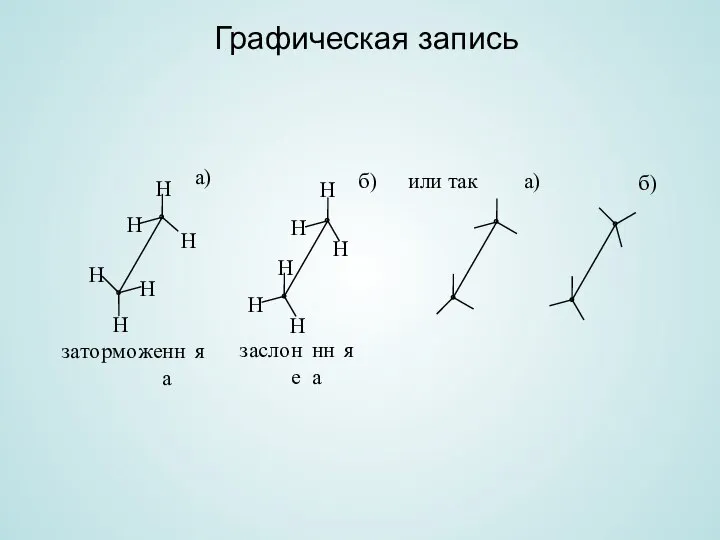
- 17. Графическая запись
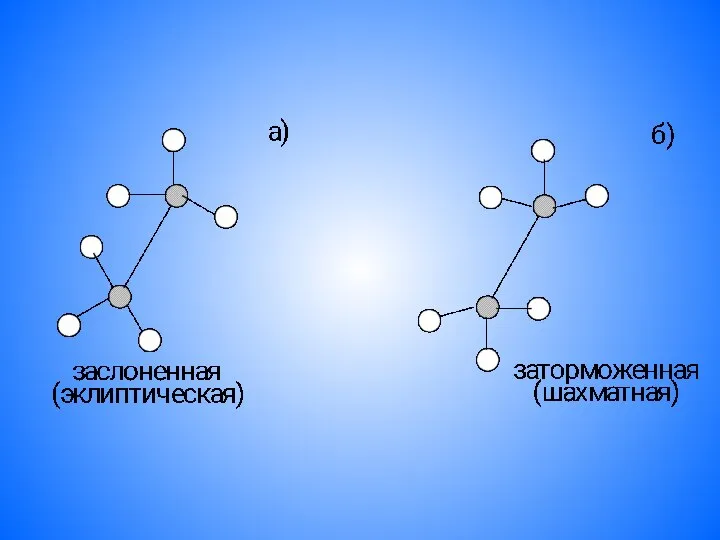
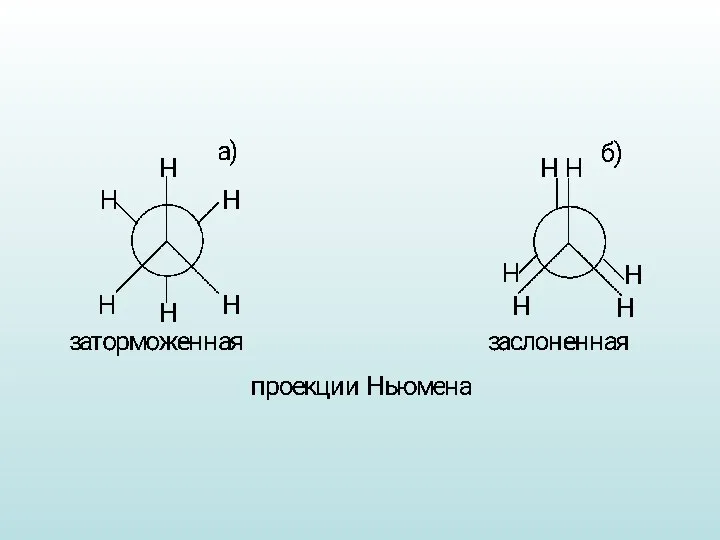
- 19. а) В заслоненной конформации (эклиптической) все атомы водорода лежат на одной линии, расстояние между водородами минимальные.
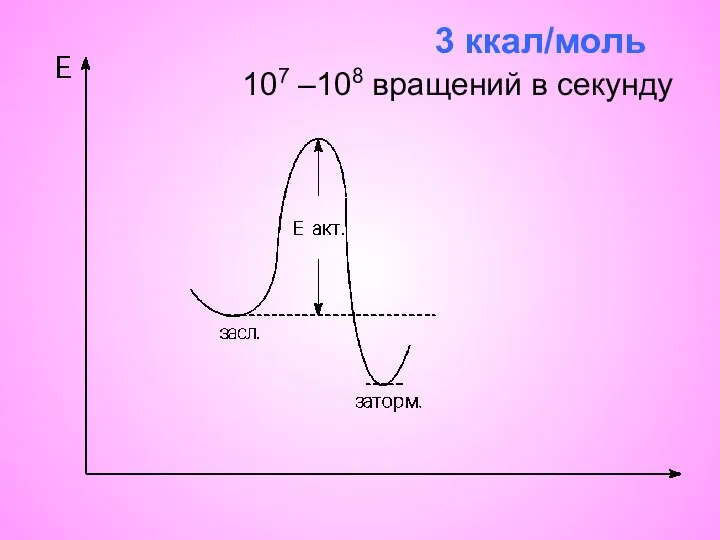
- 20. 3 ккал/моль 107 –108 вращений в секунду
- 21. Начиная с 5 ккал/моль видно спектроскопически – это уже изомеры. Принципиальной разницы между конформацией и пространственной
- 24. Скачать презентацию







 Карбоновые кислоты. Альдегиды
Карбоновые кислоты. Альдегиды Дзержинский политехнический институт. Отчет о работе химической школы
Дзержинский политехнический институт. Отчет о работе химической школы Комплексные соединения
Комплексные соединения Решение задач
Решение задач Методы диагностики плазмы
Методы диагностики плазмы Реакционная способность органических соединений
Реакционная способность органических соединений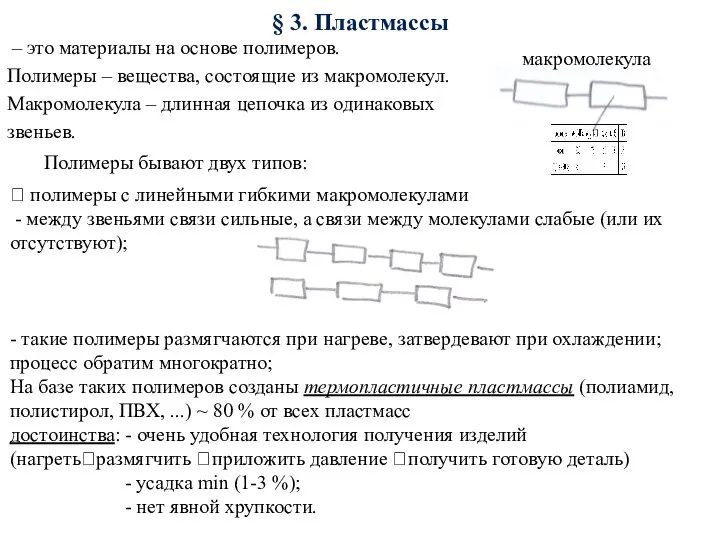 Пластмассы. Материалы, устойчивые против агрессивой среды
Пластмассы. Материалы, устойчивые против агрессивой среды Тема урока «Ионная связь»
Тема урока «Ионная связь» Газообразное состояние вещества
Газообразное состояние вещества Презентация на тему Жесткость воды
Презентация на тему Жесткость воды  Лекарственные растения содержащие флавоноиды
Лекарственные растения содержащие флавоноиды Презентация на тему Химия наука о веществах
Презентация на тему Химия наука о веществах  Какую воду мы пьем
Какую воду мы пьем Презентация на тему Карбоновые кислоты и их производные
Презентация на тему Карбоновые кислоты и их производные  Натуральный каучук
Натуральный каучук Основания. Классификация
Основания. Классификация Зависимость знака заряда белка от pH
Зависимость знака заряда белка от pH Презентация на тему Степень окисления
Презентация на тему Степень окисления  Металлы p-семейства
Металлы p-семейства Строение и химические свойства галогенов
Строение и химические свойства галогенов Электролиз. Применение электролиза
Электролиз. Применение электролиза Реакции обмена
Реакции обмена Важнейшие породообразующие минералы
Важнейшие породообразующие минералы Галогены
Галогены Алкены (часть 2)
Алкены (часть 2) 5 Нефть. Нефтепереработка. Конверсия метана
5 Нефть. Нефтепереработка. Конверсия метана Конкурс О, химия – ты муза вдохновения!
Конкурс О, химия – ты муза вдохновения! Закономерности изменения свойств галогенов
Закономерности изменения свойств галогенов