Слайд 3БЕРИЛЛИЙ (Beryllium) Be – химический элемент II группы периодической системы Менделеева, атомный

номер 4, атомная масса 9,0122; легкий светло-серый металл. Имеет один стабильный изотоп 9Ве.
Слайд 4*Прежде всего несколько (их может быть гораздо больше!) ответов на вопрос: «Что

может нам дать бериллий?»... Самолет, вес которого вдвое меньше обычного; ...ракетное топливо с наивысшим удельным импульсом; ...пружины, способные выдержать до 20 миллиардов (!) циклов нагрузки – пружины, не знающие усталости, практически вечные.
*А в начале нашего века в справочниках и энциклопедиях о бериллии говорилось: «Практического применения не имеет». Открытый еще в конце XVIII в. бериллий 100 с лишним лет оставался «безработным» элементом, хотя химикам уже были известны его уникальные и очень полезные свойства. Для того чтобы эти свойства перестали быть «вещью в себе», требовался определенный уровень развития науки и техники. В 30-х годах академик А.Е. Ферсман называл бериллий металлом будущего. Сейчас о бериллии можно и должно говорить как о металле настоящего.
Слайд 5Бериллиесодержащие минералы известны с древности. Некоторые из них добывались на Синайском полуострове

еще в 17 в. до н.э. Название берилл встречается у греческих и латинских (Beryll) античных писателей. Сходство берилла и изумруда отмечал Плиний Старший: «Берилл, если подумать, имеет ту же природу, что и смарагд (изумруд), или, по крайней мере, очень похожую»
Слайд 6Бериллий был открыт в 1798. Французский кристаллограф и минералог Рене Жюст Гаюи

(1743–1822), отметив сходство твердости, плотности и внешнего вида зеленовато-голубых кристаллов берилла из Лиможа и зеленых кристаллов изумруда из Перу
Слайд 7Рене Жюст предложил французскому химику Никола Луи Воклену (1763–1829) проанализировать берилл и

изумруд, чтобы узнать, не являются ли они химически идентичными. В результате Воклен показал, что оба минерала содержат не только оксиды алюминия и кремния, как было известно и раньше, но также и новую «землю», которая очень напоминала оксид алюминия, но, в отличие от него, реагировала с карбонатом аммония и не давала квасцов. Именно этими свойствами Воклен и воспользовался для разделения оксидов алюминия и неизвестного элемента.
Слайд 8В виде простого вещества элемент, открытый Вокленом, впервые получил немецкий химик Фридрих

Вёлер (1800–1882) в 1828, восстанавливая хлорид бериллия калием:
BeCl2 + 2K = Be + 2KCl
Слайд 9Бериллий легко растворяется в разбавленных водных растворах кислот (соляной, серной, азотной), однако

холодная концентрированная азотная кислота пассивирует металл. Реакция бериллия с водными растворами щелочей сопровождается выделением водорода и образованием гидроксобериллатов:
Be + 2NaOH(р) + 2H2O = Na2[Be(OH)4] + H2
Слайд 10При проведении реакции с расплавом щелочи при 400–500° С образуются диоксобериллаты:
Be + 2NaOH(ж)

= Na2BeO2 + H2
Слайд 11Металлический бериллий быстро растворяется в водном растворе NH4HF2. Эта реакция имеет технологическое значение

для получения безводного BeF2 и очистки бериллия:
Be + 2NH4HF2 = (NH4)2[BeF4] + H2
Слайд 12Для выделения металлического бериллия его оксид или гидроксид сначала переводят в хлорид

или фторид. Металл получают электролизом расплавленных смесей хлоридов бериллия и щелочных элементов или действием магния на фторид бериллия при температуре около 1300° С:
BeF2 + Mg = MgF2 + Be
Слайд 13Смесь соединений радия и бериллия долгое время использовалась как удобный лабораторный источник

нейтронов, образующихся по ядерной реакции:
9Be + 4He = 12C + 1n
*В 1932 при использовании именно этой смеси английским физиком Джеймсом Чедвиком был открыт нейтрон.
Слайд 14С помощью бериллия улучшают качество поверхности деталей машин и механизмов. Для этого

готовое изделие выдерживают в порошке бериллия при 900–1000° С, и его поверхность делается тверже, чем у лучших сортов закаленной стали.
Слайд 15Еще одна важная область применения бериллия – в ядерных реакторах, так как
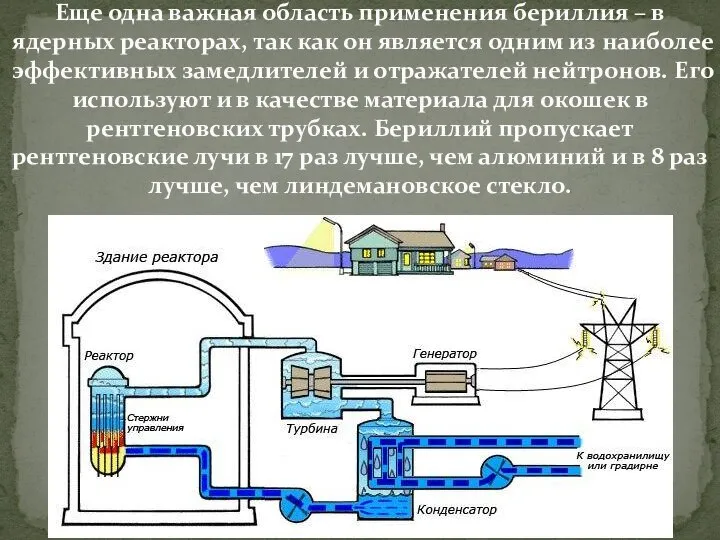
он является одним из наиболее эффективных замедлителей и отражателей нейтронов. Его используют и в качестве материала для окошек в рентгеновских трубках. Бериллий пропускает рентгеновские лучи в 17 раз лучше, чем алюминий и в 8 раз лучше, чем линдемановское стекло.
Слайд 17Бериллий не относится к биологически важным химическим элементам. В то же время,

повышенное содержание бериллия опасно для здоровья. Соединения бериллия очень ядовиты, особенно в виде пыли и дыма, обладают аллергическим и канцерогенным действием, раздражают кожу и слизистые оболочки. При попадании в легкие могут вызвать хроническое заболевание – бериллиоз (легочная недостаточность). Заболевания легких, кожи и слизистых оболочек могут возникнуть через 10–15 лет после прекращения контакта с бериллием.
Слайд 20ЧТО ТАКОЕ АЛЮМИНИЙ?
Лёгкий, прочный, стойкий к коррозии и функциональный – именно это

сочетание качеств сделало алюминий главным конструкционным материалом нашего времени. Алюминий есть в домах, в которых мы живем, автомобилях, поездах и самолетах, на которых мы преодолеваем расстояния, в мобильных телефонах и компьютерах, на полках холодильников и в современных интерьерах. А ведь еще 200 лет назад об этом металле мало что было известно.
Слайд 21Алюминий – серебристо-белый металл, 13-й элемент периодической таблицы Менделеева. Невероятно, но факт: алюминий

– самый распространенный металл на Земле, на него приходится более 8% всей массы земной коры, и это третий по распространенности химический элемент на нашей планете после кислорода и кремния.
Слайд 22Но каким бы распространенным ни был алюминий, его открытие стало возможным только,

когда в распоряжении ученых появился новый инструмент, позволяющий расщеплять сложные вещества на простые, – электрический ток.
Слайд 23И в 1824 году с помощью процесса электролиза датский физик Ханс Кристиан
Эрстед получил алюминий. Он был загрязнен примесями калия и ртути, задействованных в химических реакциях, однако это был первый случай получения алюминия.
Слайд 24Алюминий имеет редкое сочетание ценных свойств. Это один из самых легких металлов

в природе: он почти в три раза легче железа, но при этом прочен, чрезвычайно пластичен и не подвержен коррозии, так как его поверхность всегда покрыта тончайшей, но очень прочной оксидной пленкой. Он не магнитится, отлично проводит электрический ток и образует сплавы практически со всеми металлами.
Слайд 25Самый известный пример – термитная смесь, при горении которой выделяется так много

тепла, что полученное железо расплавляется:
8Al + 3Fe3O4 = 4Al2O3 + 9Fe
Слайд 26Вытеснение алюминием из растворов солей менее активных металлов часто затруднено защитной пленкой

на поверхности алюминия. Эта пленка быстро разрушается хлоридом меди, поэтому легко идет реакция
3CuCl2 + 2Al = 2AlCl3 + 3Cu ,
которая сопровождается
сильным разогревом
Слайд 27В крепких растворах щелочей алюминий легко растворяется с выделением водорода:
2Al +

6NaOH + 6Н2О = 2Na3[Al(OH)6] +3H2
(образуются и другие анионные гидроксо-комплексы)
Слайд 28При сплавлении со щелочами образуются безводные алюминаты:
Al2O3 + 2NaOH = 2NaAlO2 + H2O

Слайд 29Галогениды алюминия в водных растворах имеют кислую реакцию из-за гидролиза:
AlCl3 +

H2O Al(OH)Cl2 + HCl
Слайд 30Устойчивый в отсутствие влаги при комнатной температуре гидрид AlH3 получают в растворе безводного

эфира:
AlCl3 + LiH = AlH3 + 3LiCl.
При избытке LiH образуется солеобразный алюмогидрид лития LiAlH4 – очень сильный восстановитель, применяющийся в органических синтезах. Водой он мгновенно разлагается:
LiAlH4 + 4H2O = LiOH + Al(OH)3 + 4H2




























 Презентация на тему Занимательная химия
Презентация на тему Занимательная химия  Застосування рідких кристалів
Застосування рідких кристалів Углеводороды. Предельные (насыщенные) углеводороды
Углеводороды. Предельные (насыщенные) углеводороды Генетическая связь между классами неорганических соединений
Генетическая связь между классами неорганических соединений Агрегатные состояния вещества
Агрегатные состояния вещества Экстракция
Экстракция valentnost
valentnost Минеральные продукты
Минеральные продукты Оксиды
Оксиды Мыло и синтетические моющие средства
Мыло и синтетические моющие средства Kaloshina_Irina
Kaloshina_Irina Природные и искусственные материалы. Естествознание 6 класс
Природные и искусственные материалы. Естествознание 6 класс Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы
Реакцияға қабілетті олигомерлердің мономерлерге қарағанда артықшылығы obschaya_kharakteristika_prostykh_alifaticheskikh_efirov
obschaya_kharakteristika_prostykh_alifaticheskikh_efirov Белки
Белки Презентация на тему Основания
Презентация на тему Основания  Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс
Комментарии к выполненным заданиям по темам растворы и электролитическая диссоциация. 8 класс Электролитическая диссоциация
Электролитическая диссоциация Вещества простые и сложные
Вещества простые и сложные Соли. Применение солей
Соли. Применение солей Алкены. Пентен- С5Н10
Алкены. Пентен- С5Н10 Уравнение материального баланса технологического процесса. (Лекция 3)
Уравнение материального баланса технологического процесса. (Лекция 3) Альдегиды, свойства, получение, применение
Альдегиды, свойства, получение, применение Модельные представления силикатных структур
Модельные представления силикатных структур Строение вещества
Строение вещества Аморфные и кристаллические вещества
Аморфные и кристаллические вещества Тема урока: «Свойства тканей из химических волокон»
Тема урока: «Свойства тканей из химических волокон» Сера - химический элемент и простое вещество
Сера - химический элемент и простое вещество