Содержание
- 2. Тема урока : Основания Цель урока: 1. Сформировать знания о составе оснований, валентности гидроксильной группы, физических
- 3. Основаниями называются сложные неорганические соединения состоящие из атома металла и одной или нескольких гидрооксильных групп ОН
- 4. Основания Растворимые в воде -ЩЕЛОЧИ. NaOH Ba(OH) 2 Нерастворимые . Fe(OH) 3 Cu(OH) 2
- 5. Химические свойства .
- 6. Щёлочи 1.Щёлочи изменяют окраску индикаторов: Лакмус-синий Метилоранж-жёлтый Фенолфталеин-малиновый
- 7. 2.Реакция нейтрализации Ме(ОН)n +HR=H2O+MeR 2NaOH+H2SO4=Na2SO4+H2O ! Осторожно ! Едкие вещества !
- 8. Реакция между основанием и кислотой в результате которой образуется соль и вода-называется реакцией нейтрализации.
- 9. 3.Ме(ОН)n+неМеО=МеR+H2O 2Ca(OH)2+CO2=CaCO3+H2O 4.Ме(ОН)n+Me1R=MeR+Me1(OH)n Ba(OH)2+CuSO4=Cu(OH)2+BaSO4 Щёлочи разъедают кожу,ткани,бумагу. Осторожно! Смыть водой.
- 10. Нерастворимые основания . 1.Реакция нейтрализации . Ме(ОН)n+HR=MeR+H2O Fe(OH)2+H2SO4=FeSO4+2H2O
- 12. Скачать презентацию






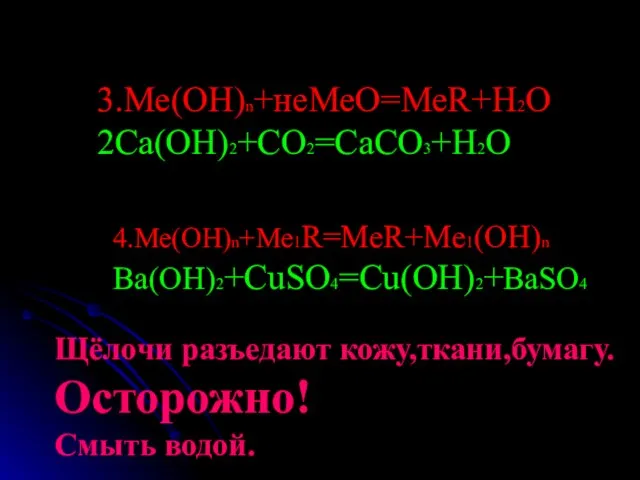

 Стекло. История открытия. Самое древнее производство Эпохи фараонов
Стекло. История открытия. Самое древнее производство Эпохи фараонов Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Кислородсодержащие органические соединения
Кислородсодержащие органические соединения Подготовка к ГИА по химии
Подготовка к ГИА по химии Презентация на тему Научная химическая лаборатория Ломоносова
Презентация на тему Научная химическая лаборатория Ломоносова  Гидроксиды металлов
Гидроксиды металлов Химические равновесия в растворах. Лекция 2 часть 2
Химические равновесия в растворах. Лекция 2 часть 2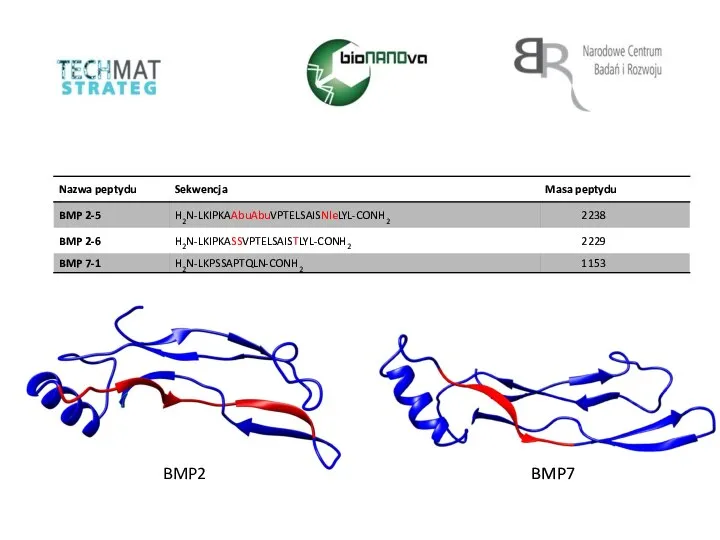 Nazwa peptydu. Sekwencja
Nazwa peptydu. Sekwencja Полімери. Пінополістирол
Полімери. Пінополістирол 5 группа элементов
5 группа элементов Химические свойства насыщенных альдегидов и кетонов (продолжение)
Химические свойства насыщенных альдегидов и кетонов (продолжение) Водородная химическая связь
Водородная химическая связь Коррозия. способы защиты от коррозии
Коррозия. способы защиты от коррозии Презентация на тему Спирты (9 класс)
Презентация на тему Спирты (9 класс)  Электролиз воды
Электролиз воды Генетические ряды углеводородов. Обобщение и систематизация знаний
Генетические ряды углеводородов. Обобщение и систематизация знаний Адсорбционные материалы. Цеолиты
Адсорбционные материалы. Цеолиты Химическая термодинамика
Химическая термодинамика Термодинамическое равновесие между фазами
Термодинамическое равновесие между фазами Физическая химия. Вводная лекция
Физическая химия. Вводная лекция Строение вещества. ОВР. Окислительно-восстановительные реакции
Строение вещества. ОВР. Окислительно-восстановительные реакции Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C
Материаловедение. Технология конструкционных материалов. Диаграмма состояния Fe-Fe3C Мыльная история
Мыльная история Оксиды. Классификация. Химические и физические свойства
Оксиды. Классификация. Химические и физические свойства алотропні модифікації неметалів
алотропні модифікації неметалів Презентация для заочников
Презентация для заочников Генетическая связь неорганических соединений
Генетическая связь неорганических соединений Алкины. Понятие об алкинах
Алкины. Понятие об алкинах