Содержание
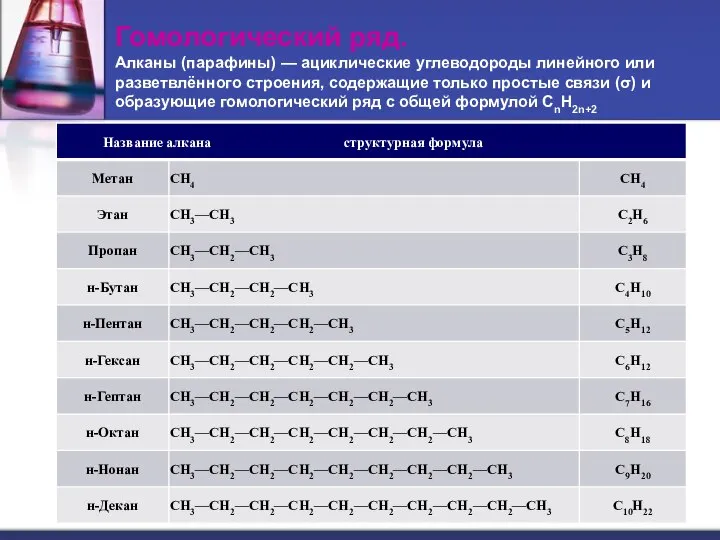
- 2. Гомологический ряд. Алканы (парафины) — ациклические углеводороды линейного или разветвлённого строения, содержащие только простые связи (σ)
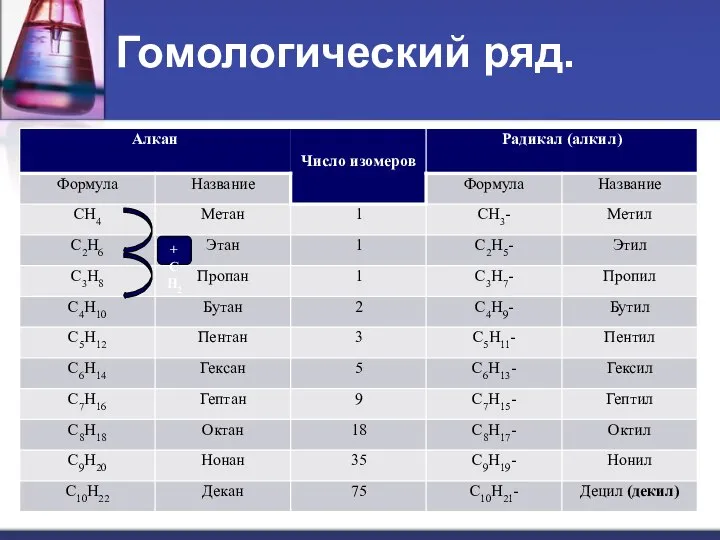
- 3. Гомологический ряд.
- 4. Наиболее часто встречающиеся углеводородные радикалы:
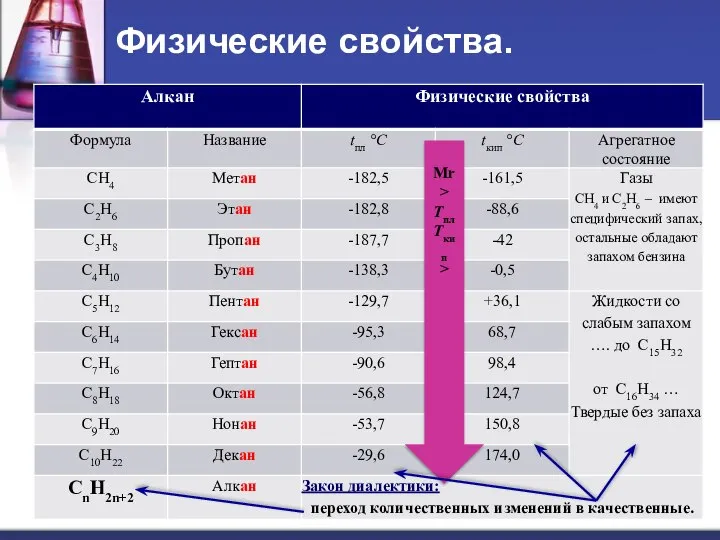
- 5. Мr > Tпл Tкип > Физические свойства.
- 6. Строение. В алканах имеются два типа химических связей: С–С и С–Н. Связь С–С является ковалентной неполярной.
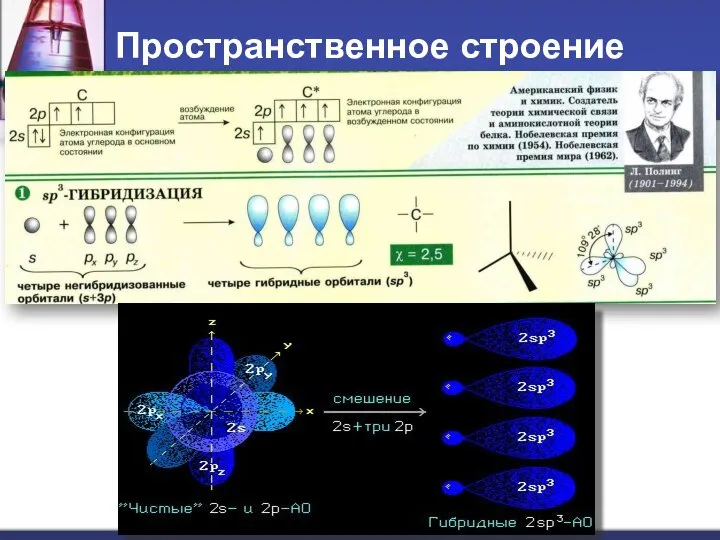
- 7. Пространственное строение
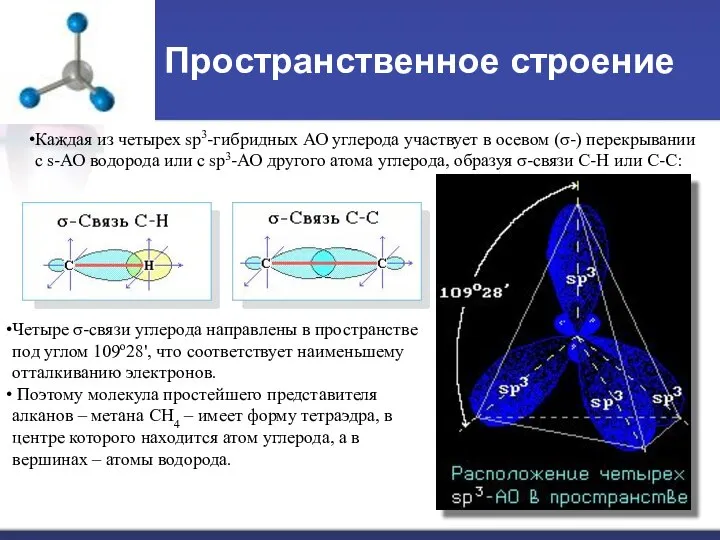
- 8. Пространственное строение Каждая из четырех sp3-гибридных АО углерода участвует в осевом (σ-) перекрывании с s-АО водорода
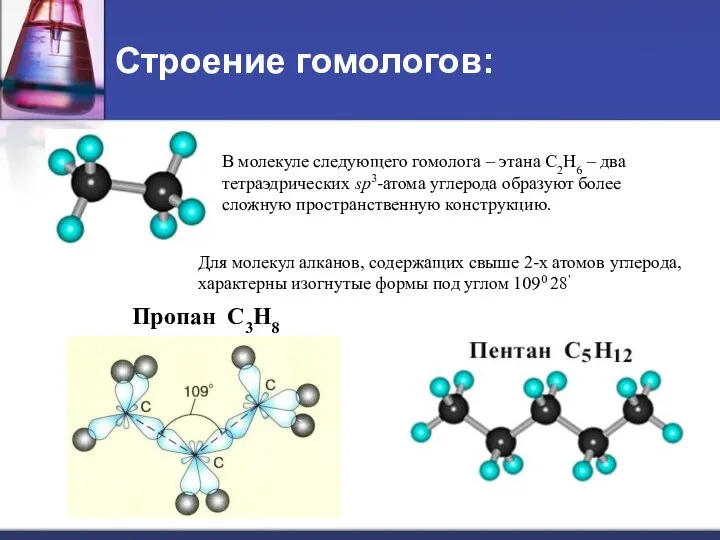
- 9. Строение гомологов: В молекуле следующего гомолога – этана С2Н6 – два тетраэдрических sp3-атома углерода образуют более
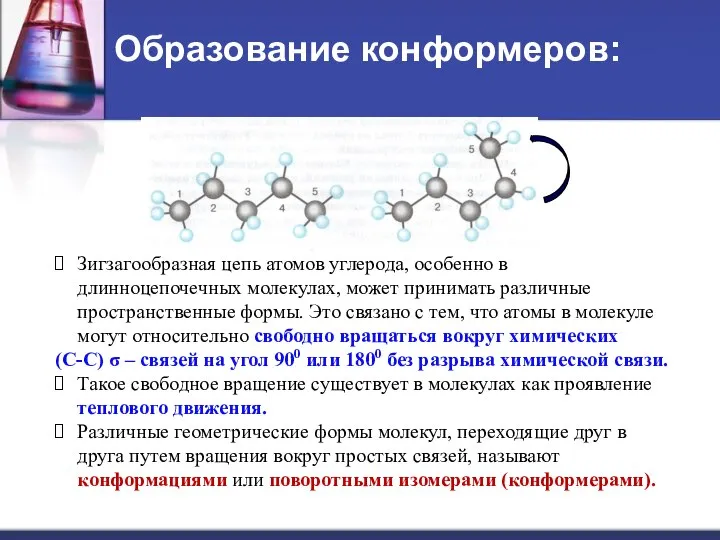
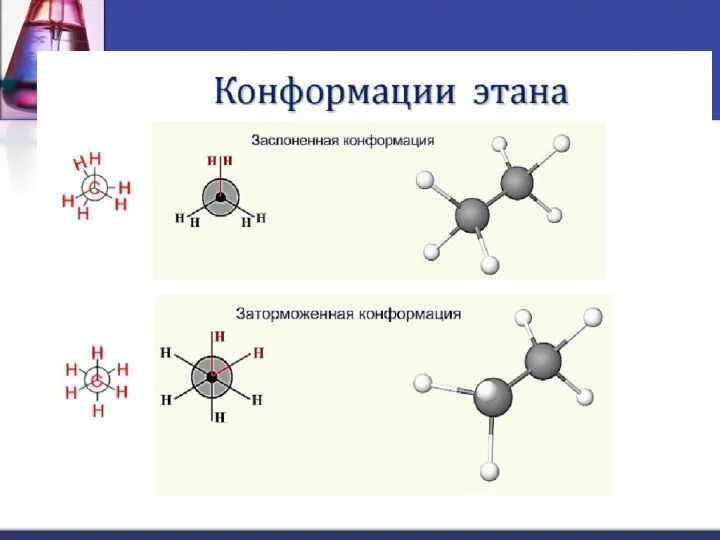
- 10. Образование конформеров: Зигзагообразная цепь атомов углерода, особенно в длинноцепочечных молекулах, может принимать различные пространственные формы. Это
- 12. Пространственное строение – самое главное !
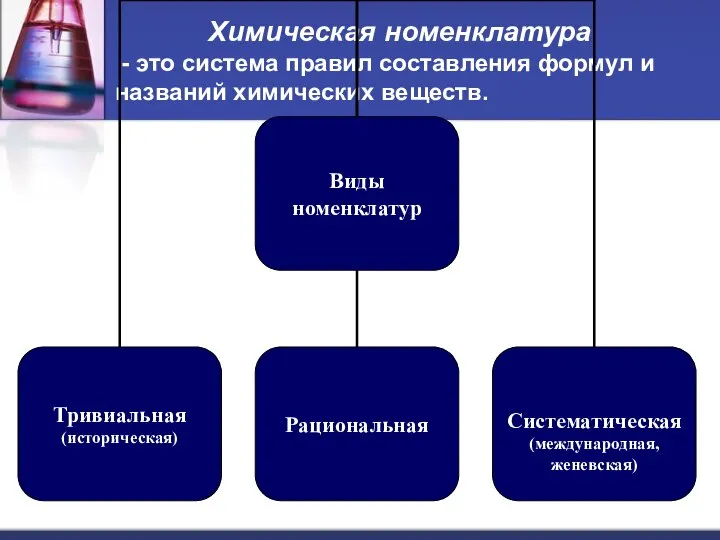
- 13. Химическая номенклатура - это система правил составления формул и названий химических веществ.
- 14. Тривиальная номенклатура Включает случайные названия и названия от греческих числительных (по количеству атомов углерода): С4Н10 –
- 15. Рациональная номенклатура Углеводороды рассматриваются как производные метана, у которого один или несколько атомов водорода замещены на
- 16. Правила систематической номенклатуры ЮПАК (IUPAC). Правило главной цепи: главную цепь выбирают, руководствуясь последовательно следующими критериями: Максимальное
- 17. Правила систематической номенклатуры ЮПАК (IUPAC). Правило радикалов: Все углеводородные боковые группы рассматривают как одновалентные (односвязные) радикалы.
- 18. Систематическая номенклатура Любая разветвленная цепь рассматривается как длинная (главная), в которой атомы водорода замещены на радикалы
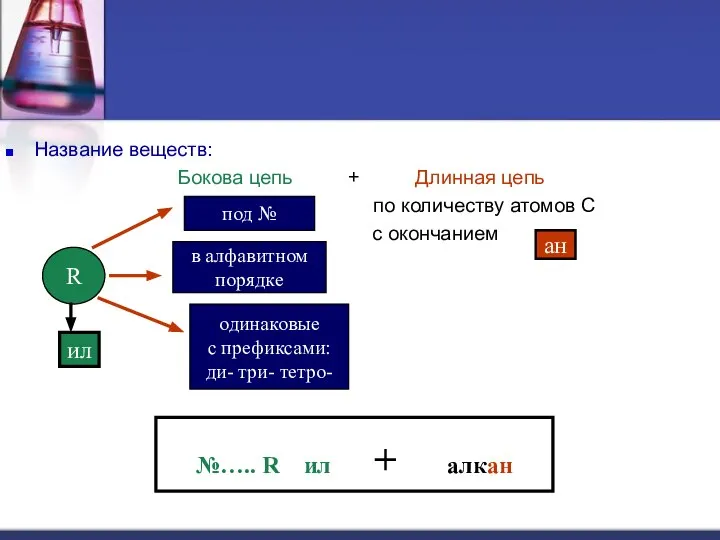
- 19. Название веществ: Бокова цепь + Длинная цепь по количеству атомов С с окончанием ан №….. R
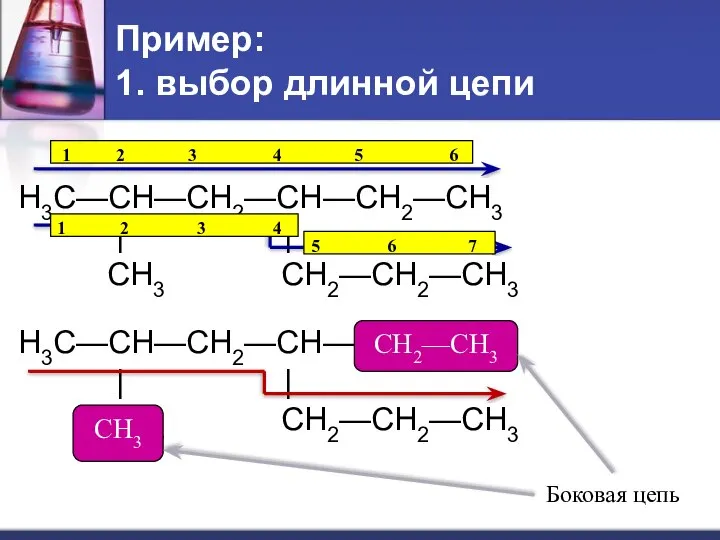
- 20. Пример: 1. выбор длинной цепи H3C—CH—CH2—CH—CH2—CH3 | | CH3 CH2—CH2—CH3 H3C—CH—CH2—CH—CH2—CH3 | | CH3 CH2—CH2—CH3 1
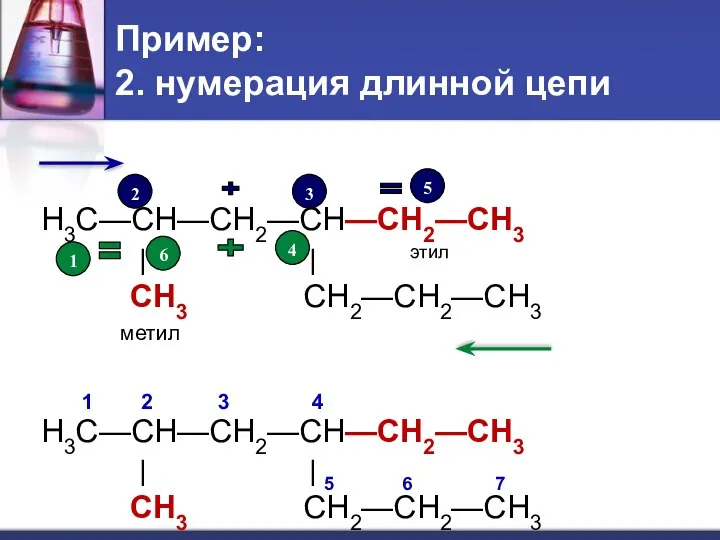
- 21. Пример: 2. нумерация длинной цепи H3C—CH—CH2—CH—CH2—CH3 | | этил CH3 CH2—CH2—CH3 метил 1 2 3 4
- 22. Систематическая номенклатура Любая разветвленная цепь рассматривается как длинная (главная), в которой атомы водорода замещены на радикалы
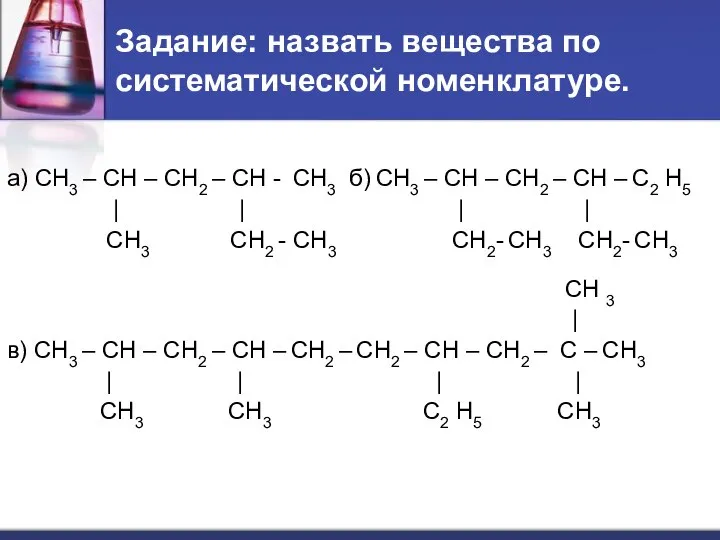
- 23. Задание: назвать вещества по систематической номенклатуре. а) СН3 – СН – СН2 – СН - СН3
- 24. Проверка: Примеры: 1 2 3 4 3 4 5 6,7 а) СН3 – СН – СН2
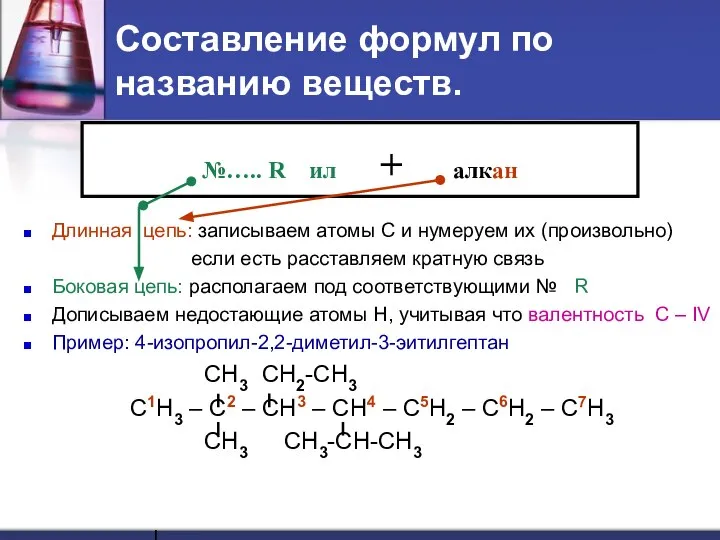
- 25. Составление формул по названию веществ. Длинная цепь: записываем атомы С и нумеруем их (произвольно) если есть
- 26. Изомерия алканов.
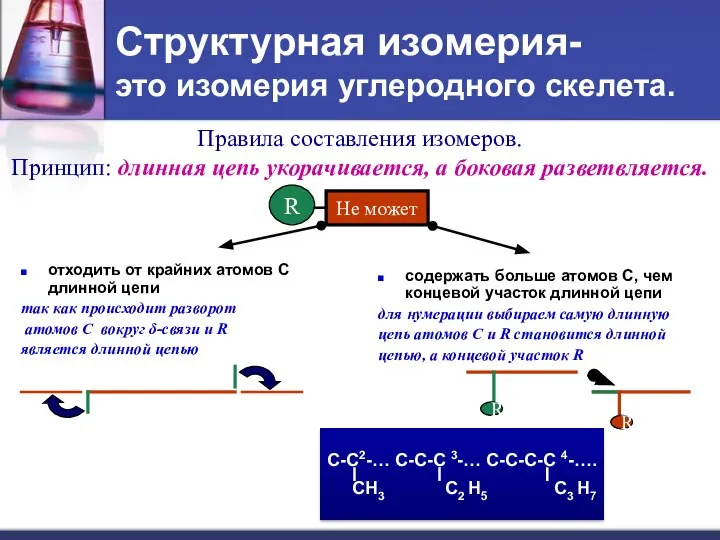
- 27. отходить от крайних атомов С длинной цепи так как происходит разворот атомов С вокруг δ-связи и
- 28. Пространственная изомерия - это изомерия расположения атомов в пространстве. Оптическая изомерия Оптические изомеры имеют одинаковое химическое
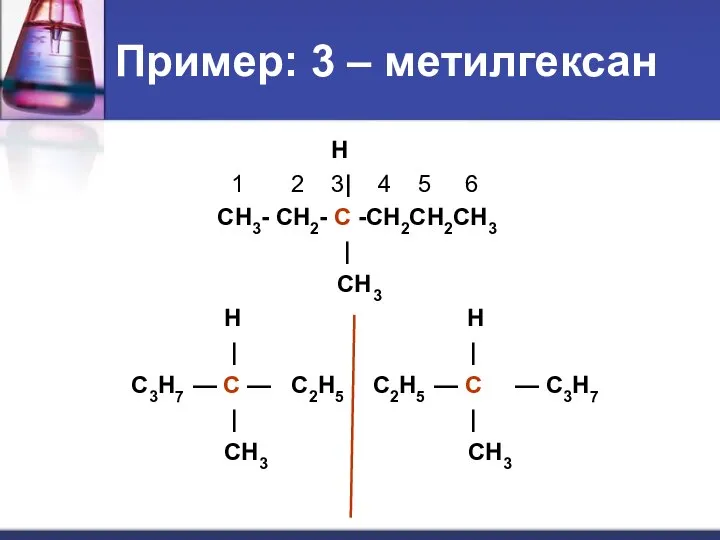
- 29. Пример: 3 – метилгексан Н 1 2 3| 4 5 6 СН3- СН2- С -СН2СН2СН3 |
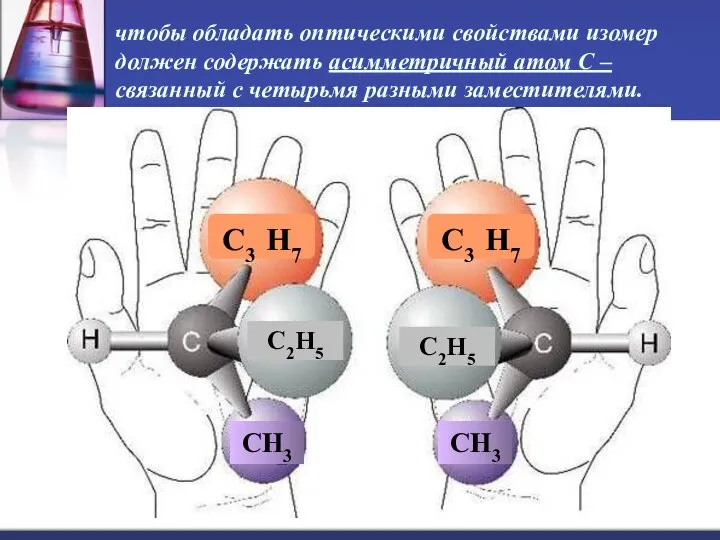
- 30. чтобы обладать оптическими свойствами изомер должен содержать асимметричный атом С – связанный с четырьмя разными заместителями.
- 32. Скачать презентацию











 Степень окисления. Составление формул бинарных соединений. 8 класс
Степень окисления. Составление формул бинарных соединений. 8 класс Химиялық есептердің кеңістіктік шешімдері
Химиялық есептердің кеңістіктік шешімдері Важнейшие классы неорганических соединений. Соли
Важнейшие классы неорганических соединений. Соли Классификация загрязняющих веществ по фазово-дисперсному составу
Классификация загрязняющих веществ по фазово-дисперсному составу Пример выполнения проверочной работы по теме углеводороды
Пример выполнения проверочной работы по теме углеводороды Физико-химические свойства нефтепродуктов
Физико-химические свойства нефтепродуктов Образование дипептида
Образование дипептида Химия и жизнь
Химия и жизнь Алканы. Физические свойствава алканов
Алканы. Физические свойствава алканов Сравнительная характеристика стиральных порошков
Сравнительная характеристика стиральных порошков Энергетические уровни
Энергетические уровни Морфологія та походження мінералів. Елементи кристалографії
Морфологія та походження мінералів. Елементи кристалографії Железо
Железо Белки
Белки Суд над химическим элементом Углерод
Суд над химическим элементом Углерод Приёмы работы с текстом на уроках химии
Приёмы работы с текстом на уроках химии Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях
Сравнительный анализ Фармакопейных статей для субстанций, представленных в мировых Фармакопеях Открытия в химии
Открытия в химии Газ тәрізді өнімдер бромды сутек
Газ тәрізді өнімдер бромды сутек Электролиз
Электролиз Концентрированная серная кислота
Концентрированная серная кислота Презентация на тему Основные законы науки химии
Презентация на тему Основные законы науки химии  хімія
хімія Типичные ошибки, допускаемые учащимися при выполнении задания повышенного уровня сложности С-5 ЕГЭ по химии
Типичные ошибки, допускаемые учащимися при выполнении задания повышенного уровня сложности С-5 ЕГЭ по химии Алканы: состав, строение, изомерия, номенклатура, получение
Алканы: состав, строение, изомерия, номенклатура, получение Основные свойства и опасности нефти. Безопасность для танкеров
Основные свойства и опасности нефти. Безопасность для танкеров Жиры
Жиры Карбораны. Особенности строения молекулы. Получение и химические свойства
Карбораны. Особенности строения молекулы. Получение и химические свойства