Содержание
- 2. Вспомним! Что называется: Оксидами Основаниями Кислотами
- 3. Назовите вещества Na2O CaO Al2О3 P2O5 NaOH Ca(OH)2 Al(OH)3 HCl HNO3 H2S H2SO4 H3PO4
- 4. Выберите отдельно кислоты, основания, соли CaO Ca(OH)2 HNO3 Al2(SO4)3 H3PO4 CO2 H2S NaCl Mg(OH)2 CaCO3
- 5. Назовите соли MgSO4 Al2(SO4)3 Fe(NO3)3 CaCO3 NaCl
- 6. Напишите формулы Хлорид магния Сульфат калия Нитрат алюминия Фосфат цинка
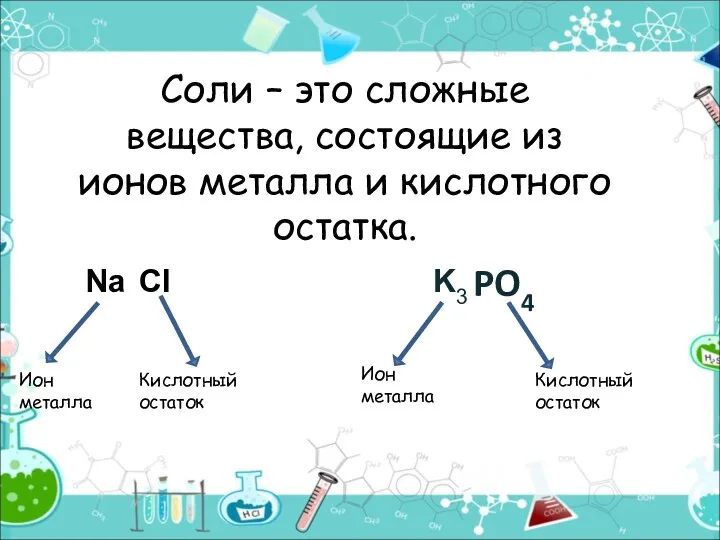
- 7. Соли – это сложные вещества, состоящие из ионов металла и кислотного остатка. PO4 Ион металла Кислотный
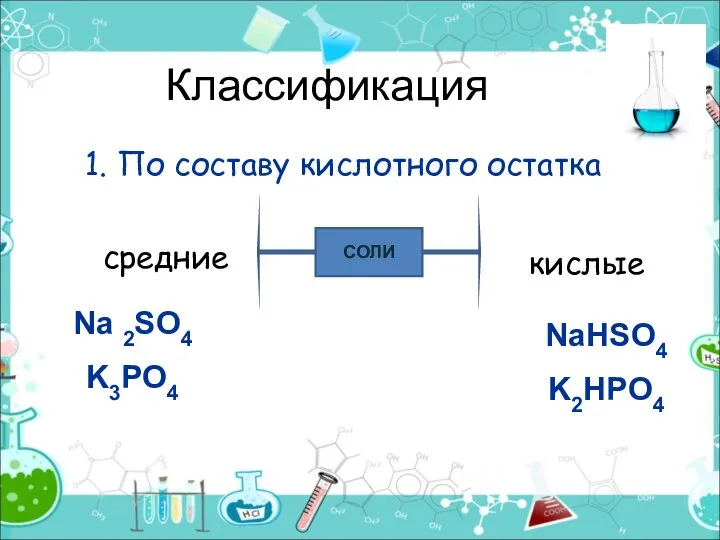
- 8. Классификация 1. По составу кислотного остатка СОЛИ средние кислые Na 2SO4 K3PO4 NaHSO4 K2HPO4
- 9. Номенклатура средних солей магния Название кислотного остатка Наименование металла в родительном падеже МgСL2 хлорид
- 10. Номенклатура кислых солей Указать название кислотного остатка К названию кислотного остатка прибавить «гидро-» Наименование металла в
- 11. Химические свойства 1. Взаимодействие с металлами: SnCl2 + Zn ? ZnCl2 + Sn
- 12. Химические свойства 2. Взаимодействие со щелочами: 2NaОН + CuSO4 → Cu(OH)2 + Na2SO4
- 13. Химические свойства 3. Взаимодействие солей между собой КСl + AgNO3 → AgCl + KNO3
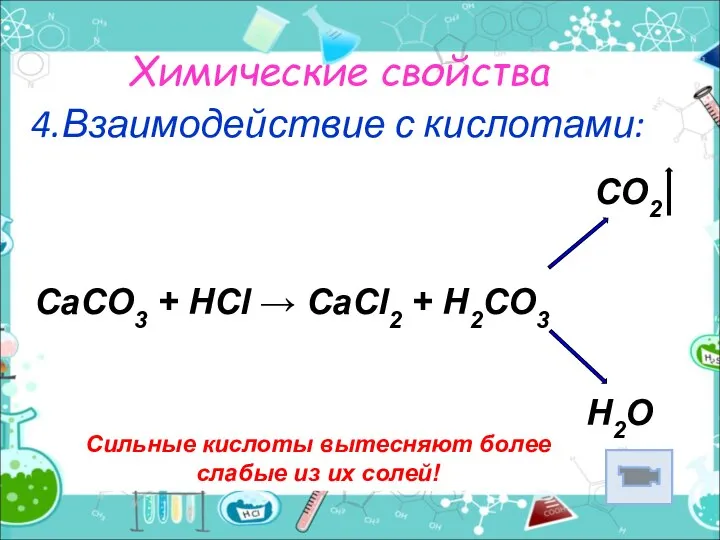
- 14. Химические свойства 4.Взаимодействие с кислотами: Сильные кислоты вытесняют более слабые из их солей! CO2 CaCO3 +
- 15. Химические свойства Разложение при нагревании СаСО3= СО2 + Н2О
- 16. Способы получения 1. Кислота + основание = соль + вода H2SO4 +2NaOH = Na2SO4 + 2H2O
- 17. Способы получения 5. Основание + соль = новое основание + новая соль 2КОН + СаSO4 =
- 20. Скачать презентацию













 Механизмы двухсубстатных реакций
Механизмы двухсубстатных реакций Производство концентрированной азотной кислоты (лекция 15)
Производство концентрированной азотной кислоты (лекция 15) Закон сохранения массы и энергии
Закон сохранения массы и энергии Химическая связь
Химическая связь Силикатная промышленность
Силикатная промышленность Образование и получение веществ
Образование и получение веществ 1_Galogeny
1_Galogeny Электролитическая диссоциация. 9 класс
Электролитическая диссоциация. 9 класс 4.1-2 Генетическая связь+
4.1-2 Генетическая связь+ Химия углеводов
Химия углеводов Радиоактивный распад. Чернобыль
Радиоактивный распад. Чернобыль Кислород. 8 класс
Кислород. 8 класс Ароматические углеводороды
Ароматические углеводороды Электрохимия. Решение задач. ИДЗ 4
Электрохимия. Решение задач. ИДЗ 4 Основания. 8 класс
Основания. 8 класс Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды
Ресурс Лови оксиды для систематизации знаний, умений, навыков по теме Оксиды Ароматические углеводороды. Бензол
Ароматические углеводороды. Бензол Знаки химических элементов
Знаки химических элементов Количество вещества. Моль
Количество вещества. Моль Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории
Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории Загадки химии. Занятие 4
Загадки химии. Занятие 4 Электролиз. Применение электролиза
Электролиз. Применение электролиза Коррозия металлов и способы борьбы с ней
Коррозия металлов и способы борьбы с ней Строение электронных оболочек атома
Строение электронных оболочек атома Предмет биоорганической химии. Лекция 1
Предмет биоорганической химии. Лекция 1 Фиды специфичности ферментов. Субстратная специфичность
Фиды специфичности ферментов. Субстратная специфичность Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь
Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь Расчет псевдокритических свойств конденсатного газа и пластовых газоконденсатных жидкостей. Анализ рекомбинированных проб
Расчет псевдокритических свойств конденсатного газа и пластовых газоконденсатных жидкостей. Анализ рекомбинированных проб