Содержание
- 2. Химия – наука о веществах, их строении, свойствах и превращениях. Химические свойства веществ – это способность
- 3. Атомно – молекулярное учение. Михаил Васильевич Ломоносов (1711 – 1765) Джон Дальтон (1766 – 1844) Учение
- 4. Основные положения атомно – молекулярного учения. Вещества состоят из молекул. Молекула - это наименьшая частица вещества,
- 5. 3. Вещества, молекулы которых состоят из атомов одного элемента простые вещества. Вещества, молекулы которых состоят из
- 6. Периодический закон – фундаментальный закон химии. В 1869 году Д. И. Менделеевым был сформулирован Периодический закон.
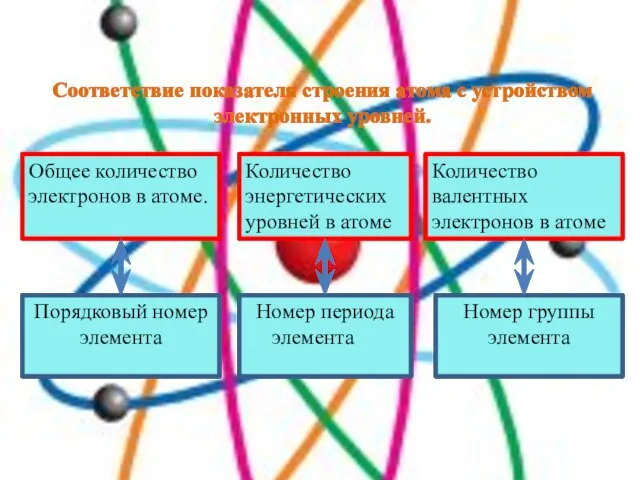
- 7. Соответствие показателя строения атома с устройством электронных уровней. Общее количество электронов в атоме. Порядковый номер элемента
- 8. Закон постоянства состава веществ. Жозеф Луи Пруст (1754 – 1826) Закон был открыт французским ученым в
- 9. Закон сохранения массы вещества. Антуан Лоран Лавуазье (1743 – 1794) Михаил Васильевич Ломоносов (1711 -1765) Закон
- 10. « Все перемены в натуре случающиеся такого суть состояния, что сколько чего у одного тела отнимается,
- 11. Закон Авогадро. Амедео Авогадро (1776 – 1856) В равных объемах различных газов при одинаковых условиях (температура,
- 12. Закон эквивалентов. Иеремия Вениамин Рихтер (1762 – 1807) «Если одно и то же количество какой-либо кислоты
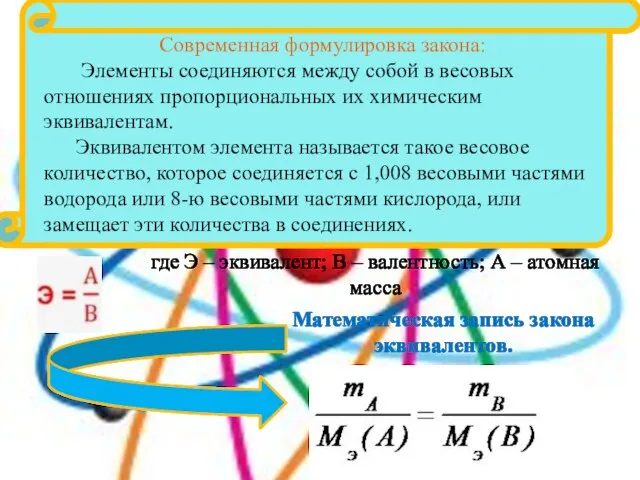
- 13. где Э – эквивалент; В – валентность; А – атомная масса Математическая запись закона эквивалентов. Современная
- 14. Закон кратных отношений. Джон Дальтон (1766 - 1844) Закон установлен в 1803 году Джоном Дальтоном. Если
- 15. Уравнение Менделеева – Клапейрона. Формула, устанавливающая зависимость между давлением, молярным объемом и абсолютной температурой идеального газа:
- 16. Закон Бойля – Мариотта. Роберт Бойль (1627 - 1691) В 1660 году открыл закон изменения объёма
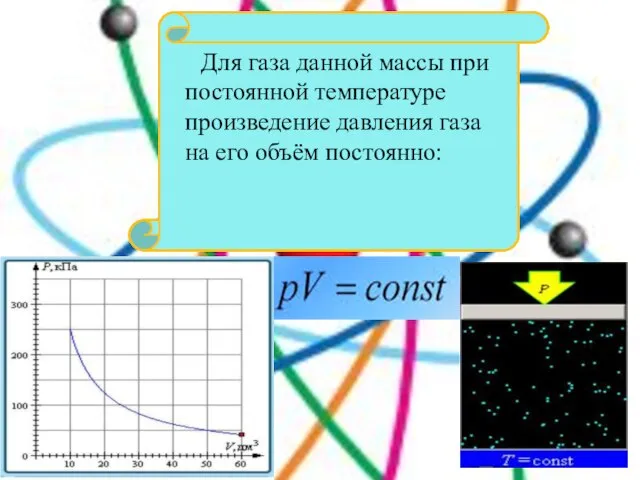
- 17. Для газа данной массы при постоянной температуре произведение давления газа на его объём постоянно:
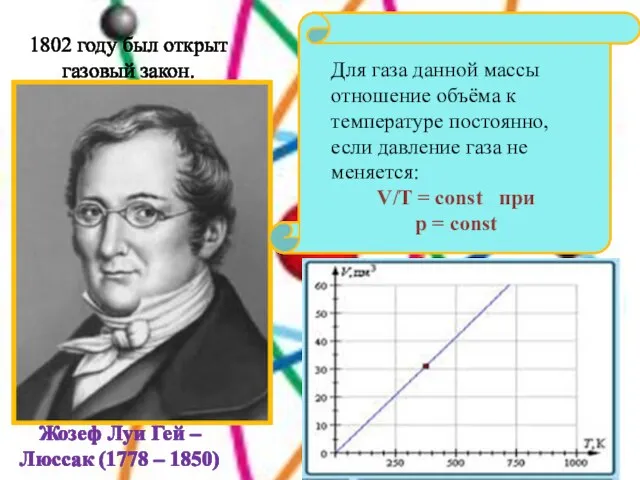
- 18. Для газа данной массы отношение объёма к температуре постоянно, если давление газа не меняется: V/T =
- 19. Задачи для закрепления. Задание № 1. Вычислите число атомов азота в 100г карбоната аммония, содержащего 10%
- 20. http://abouthist.net/wp-content/uploads/2011/09/ris15.png https://encryptedtbn2.gstatic.com/images?q=tbn:ANd9GcQIADrHB7WPhmwtO4xJPC3IcoSq5EUlnTioB7bYfL_Wxg_73M3 http://class-fizika.narod.ru/phys/15.jpg http://lichnosti.net/photos/2682/main.jpg http://img15.nnm.me/3/5/9/c/9/33e15b432c7b16d85194a2064d3.jpg https://encryptedtbn3.gstatic.com/images?q=tbn:ANd9GcSvAL6XFRPQl_il8l6HJixPr5ZvrCatdd4Ulnl7PCj1nlOy3QP http://school-box.ru/images/stories/prezentaziya-po-chimii-zakon-sochraneniya-massi-veshestva.jpg http://www.calend.ru/img/content_events/i0/349.jpg http://images.myshared.ru/199103/slide_9.jpg http://konspekta.net/studopediaorg/baza6/2104455695415.files/image005.png http://image.slidesharecdn.com/reaviz-1-140903150256-phpapp02/95/reaviz-1-19-638.jpg?cb=1409778579 http://www.samara.edu.ru/upload/iblock/4ba/Mendeleev.jpg http://posobie-opt.ru/files/school/175/6.jpg http://bigslide.ru/images/2/1607/960/img8.jpg https://encryptedtbn2.gstatic.com/images?q=tbn:ANd9GcRxVjjP02bKEwpLOCwDS9Z6jnm90MsNRFgRWuN8bvf3TRyEABSR8g
- 22. Скачать презентацию














 Презентация на тему Окислительно-восстановительные реакции
Презентация на тему Окислительно-восстановительные реакции  Презентация на тему Сложные эфиры. Жиры
Презентация на тему Сложные эфиры. Жиры  Пентоза - відновлювальна сировина для синтезу фуранових сполук
Пентоза - відновлювальна сировина для синтезу фуранових сполук Дождь из облака
Дождь из облака По страницам истории российской химической науки
По страницам истории российской химической науки Явление хемилюменисценции
Явление хемилюменисценции Сложные вещества кислоты
Сложные вещества кислоты Что изучает химия?
Что изучает химия? Окислительно-восстановительные реакции. Классификация ОВР
Окислительно-восстановительные реакции. Классификация ОВР Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем
Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем Аналитический обзор по теме Процесс разложения аммиака
Аналитический обзор по теме Процесс разложения аммиака Презентация на тему Игра «Путешествие в страну Атомолия»
Презентация на тему Игра «Путешествие в страну Атомолия»  Белки
Белки Углеводороды. Общие знания
Углеводороды. Общие знания Ca КАЛЬЦИЙ
Ca КАЛЬЦИЙ Органическая химия. Йенс Якоб Берцелиус (1779 - 1848)
Органическая химия. Йенс Якоб Берцелиус (1779 - 1848) Презентация на тему Альдегиды (10 класс)
Презентация на тему Альдегиды (10 класс)  Щелочные металлы
Щелочные металлы Жесткость воды и способы ее устранения
Жесткость воды и способы ее устранения Презентация на тему Валентность и степень окисления (8 класс)
Презентация на тему Валентность и степень окисления (8 класс)  Основной государственный экзамен. Химия 2022. Задание 2
Основной государственный экзамен. Химия 2022. Задание 2 Своя игра. Атомы
Своя игра. Атомы ИКТ как средство реализации проблемного обучения на уроках химии
ИКТ как средство реализации проблемного обучения на уроках химии Алюминий. Применение
Алюминий. Применение Хлороводород и соляная кислота
Хлороводород и соляная кислота Химические свойства оксидов
Химические свойства оксидов Химическая связь. Строение вещества
Химическая связь. Строение вещества Презентация на тему Основания и их классификация
Презентация на тему Основания и их классификация