Типичные ошибки, допускаемые учащимися при выполнении задания повышенного уровня сложности С-5 ЕГЭ по химии
- Главная
- Химия
- Типичные ошибки, допускаемые учащимися при выполнении задания повышенного уровня сложности С-5 ЕГЭ по химии

Содержание
- 2. Наиболее характерные причины, по которым выпускники теряют баллы при решении задач С-5: Некорректное оформление Решение не
- 3. 1. В задачах на продукты сгорания теряется водород, находящийся в составе галогенводородов, . Иногда - неправильный
- 4. 2.Решая задачи на определение формулы вещества нужно, как правило, приходить к строению вещества, т.е. приводить его
- 5. 3.Иногда условия задачи на определение формулы вещества настолько просты, что ученик определяет формулу «в уме». Например,
- 6. 4. В задачах на вывод молекулярных формул с нестандартной формулировкой условий задач, многие выпускники затруднились с
- 7. 5. Выпускники привыкли решать задачи, где даны массовые доли всех элементов. Есть задачи, где необходимо по
- 9. Скачать презентацию
Слайд 2Наиболее характерные причины,
по которым выпускники теряют баллы
при решении задач С-5:
Некорректное
Наиболее характерные причины,
по которым выпускники теряют баллы
при решении задач С-5:
Некорректное

Решение не математическим путем, а методом подбора
Неверное составление общей формулы вещества
Ошибки в уравнении реакции с участием вещества, записанного в общем виде.
Слайд 31. В задачах на продукты сгорания теряется водород, находящийся в составе галогенводородов,
1. В задачах на продукты сгорания теряется водород, находящийся в составе галогенводородов,

При сгорании газообразного органического вещества, не содержащего кислород, выделилось 4,48 л углекислого газа (н.у.), 3,6 г воды и 2 г фтороводорода. Установите молекулярную формулу соединения.
1.Найдено количество вещества оксида углерода(IV), HF, воды:
n(CO2) = V/VM = 4,48/22,4 = 0,2 моль
n(HF) = m/M = 2/20 = 0,1 моль
n(H2O) = m/M = 3,6/18 = 0,2 моль
2.Найдено количество вещества элементов:
углерода, n(C) = n(CO2) = 0,2 моль;
фтора, n(F) = n(HF) = 0,1 моль
водорода, n(H) = 2n(H2O) + n<(HF) = 0,2*2 + 0,1 = 0,5 моль
Соотношение: n(С):n(H):n(F) = 2:5:1; простейшая формула C2H5F
3.При умножении простейшей формулы на 2, 3 и т.д. получаются «пересыщенные» составы. Поэтому молекулярная формула совпадает с простейшей: C2H5F , фторэтан
Рекомендации: выпускникам советовать, проверять себя: чего больше молекул или атомов?
Слайд 42.Решая задачи на определение формулы вещества нужно, как правило, приходить к строению
2.Решая задачи на определение формулы вещества нужно, как правило, приходить к строению

Например, выпускники не всегда верно понимают понятия «первичный», «вторичный», «третичный» отнесенные к аминам.
Например:
CH 3-CHOH-CH 3 – вторичный спирт,
но CH 3-CH(NH 2)-CH 3 – первичный амин.
Формула вторичного амина: CH 3-CH 2-NH-CH 3 .
Рекомендации: в номенклатуре спиртов эти понятия означают тип атома углерода, в номенклатуре аминов они характеризуют число радикалов у атома азота.
Слайд 53.Иногда условия задачи на определение формулы вещества настолько просты, что ученик определяет
3.Иногда условия задачи на определение формулы вещества настолько просты, что ученик определяет

Например, определив молекулярную массу углеводорода равную 30, можно не использовать данные по продуктам его сгорания. Но необходимо будет записать, что, исходя из общей формулы углеводородов СхНу, в состав молекулы может входить только 2 атома углерода, следовательно, таким углеводородом может быть только этан, С2Н6
Рекомендации: ученик должен письменно обосновать свой вывод в решении. Только запись готовой формулы не может быть оценено максимальным баллом.
Слайд 64. В задачах на вывод молекулярных формул с нестандартной формулировкой условий задач,
4. В задачах на вывод молекулярных формул с нестандартной формулировкой условий задач,

При щелочном гидролизе 37 г некоторого сложного эфира получено 49 г калийной соли предельной одноосновной кислоты и 16 г спирта. Установите молекулярную формулу эфира.
Записываем уравнение реакции в общем виде:
RCOOR' + KOH = RCOOK + R'H.
2. Подставляя условия задачи, можно найти количество вещества гидроксида калия – 0,5 моль.
3. Сравнив количество вещества исходного эфира и щелочи, можно найти молекулярную массу эфира – 74 г/моль
4. Далее можно найти молекулярную формулу, установив молекулярную массу радикалов: M(R1 + R2) = 74 – (12?+?32) = 30 г/моль.
5. Искомая формула вещества – СН3 –СОО–СН3.
Рекомендации: начинать решение с представления уравнения реакции в общем виде.
Слайд 75. Выпускники привыкли решать задачи, где даны массовые доли всех элементов. Есть
5. Выпускники привыкли решать задачи, где даны массовые доли всех элементов. Есть

Дихлорпроизводное алкана содержит 5,31% водорода по массе. Определите молекулярную формулу дихлоралкана. Приведите структурную формулу одного из возможных изомеров и назовите его.
1.Общая формула дихлоралкана CnH2nCl2, его молекулярная масса Mr = 14n+71
2. Массовая доля водорода равна
3. Решаем уравнение 0,0531(14n+71) = 2n, n = 3
4.Формула дихлоралкана C3H6Cl2
Возможный изомер CH3-CH2-CHCl2 – 1,1- дихлорпропан
Рекомендации: в большинстве случаев желательно, чтобы эта общая формула показывала функциональные группы вещества.
Например спиртов (R-OH или CnH2n+1OH), альдегидов (R-CHO или CnH2n+1-CHO), карбоновых кислот (R-COOH или CnH2n+1-COOH), сложных эфиров (R1-COO-R2 или CnH2n+1-COO-CmH2m+1) и др.
 Закалка без полиморфного превращения
Закалка без полиморфного превращения Алюминий
Алюминий Амины. 10 класс
Амины. 10 класс Применение арт-технологии на уроках химии Обобщение опыта педагогической деятельности МОУ СОШ № 14 город Мончегорск Мурманск
Применение арт-технологии на уроках химии Обобщение опыта педагогической деятельности МОУ СОШ № 14 город Мончегорск Мурманск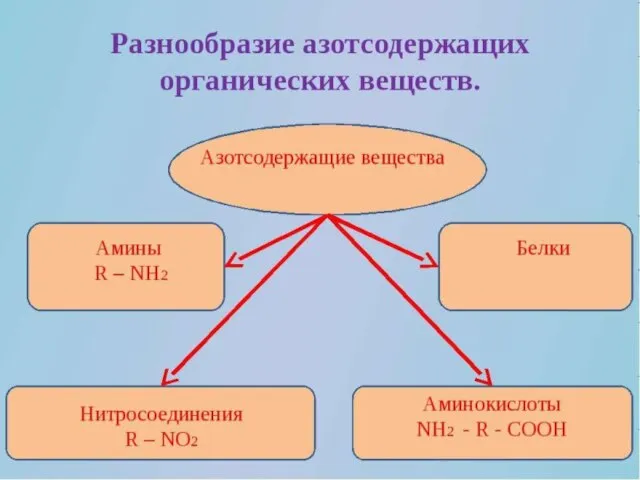 Разнообразие азотсодержащих органических веществ
Разнообразие азотсодержащих органических веществ Предмет органической химии. Органические вещества
Предмет органической химии. Органические вещества Классификация силикатов
Классификация силикатов ГИА по химии 2010-2011
ГИА по химии 2010-2011 Звездный час. Знатоки химии
Звездный час. Знатоки химии Гидроксид кальция – гашеная известь
Гидроксид кальция – гашеная известь صيغ المركبات وأسمائها
صيغ المركبات وأسمائها Увлекательный мир химии
Увлекательный мир химии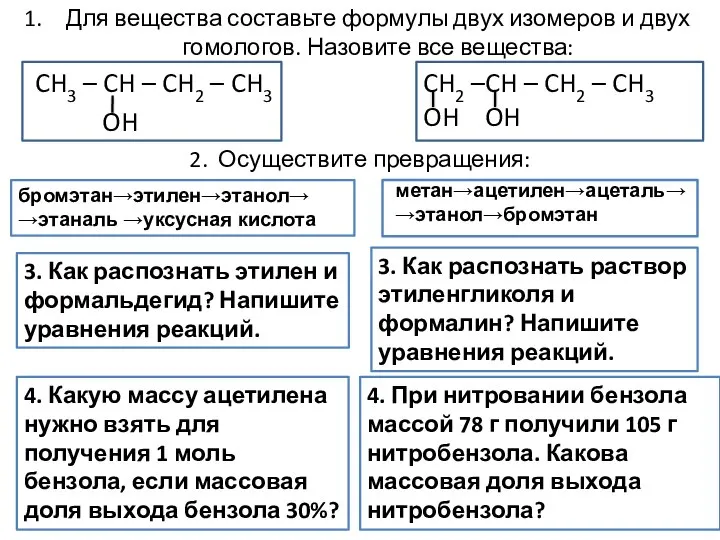 Формулы двух изомеров и двух гомологов
Формулы двух изомеров и двух гомологов gidroliz_soley (1)
gidroliz_soley (1) Презентация на тему Химия и сельское хозяйство (11 класс)
Презентация на тему Химия и сельское хозяйство (11 класс)  Арены. Бензол. 9 класс
Арены. Бензол. 9 класс Перициклические реакции
Перициклические реакции Образование дипептида
Образование дипептида alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1
alkany_stroenie_nomenklatura_izomeriya_10_klass (3)-1 Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс
Характеристика химического элемента-неметалла на основании его положения в ПСХЭ Д.И.Менделеева. 9 класс Производство аммиака
Производство аммиака Окисно-відновні реакції. Процеси окиснення та відновлення, окисники та відновники. 9 клас
Окисно-відновні реакції. Процеси окиснення та відновлення, окисники та відновники. 9 клас Неметаллы в ПСХЭ
Неметаллы в ПСХЭ Энергетические уровни
Энергетические уровни Сложные эфиры. Жиры
Сложные эфиры. Жиры Лекция 10. Неорганическая химия. Сероводород
Лекция 10. Неорганическая химия. Сероводород Exotermické a endotermické reakcie
Exotermické a endotermické reakcie Выращивание кристаллов медного купороса с использованием воды различной степени очистки
Выращивание кристаллов медного купороса с использованием воды различной степени очистки