Слайд 2Степень окисления. Составление формул бинарных соединений.
8 класс.

Слайд 3Цели урока:
1. Дать понятие степень окисления.
2. Научить рассчитывать степени окисления

по формулам бинарных соединений и составлять химические формулы по с.о.
3. Дать первоначальные представления о номенклатуре химических соединений.
4. Формировать химически правильную речь.
5. Содействовать формированию научного мировоззрения, нравственности.
Слайд 4
Степень окисления
– соответствует числу отданный, принятых или смещенных электронов.

Слайд 5I.Степень окисления для веществ с различными видами связи.

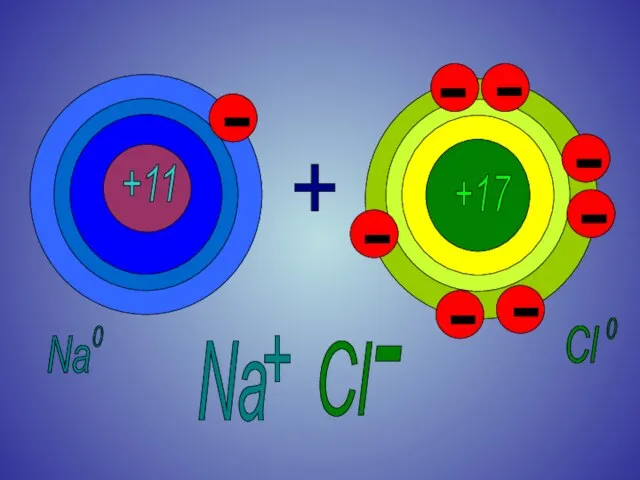
Слайд 6Степень окисления
для веществ с ионной связью
на примере NaCl.

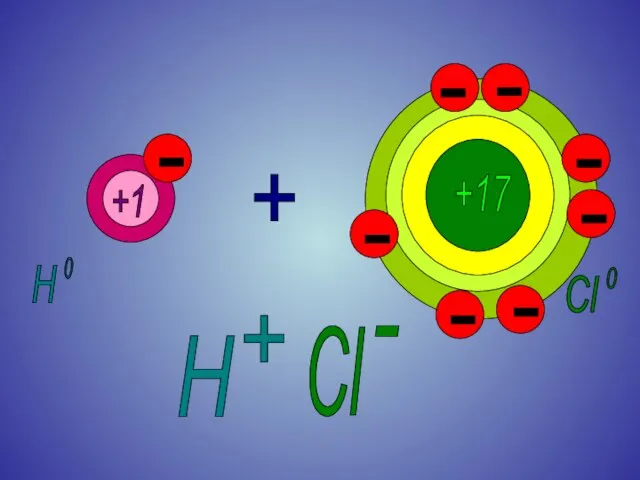
Слайд 8Степень окисления
для веществ с КПС
на примере HCl.

Слайд 10Степень окисления для простых веществ.

Слайд 12II.Определение
степени окисления в бинарных соединениях.

Слайд 13Определим основные ЗАКОНОМЕРНОСТИ.

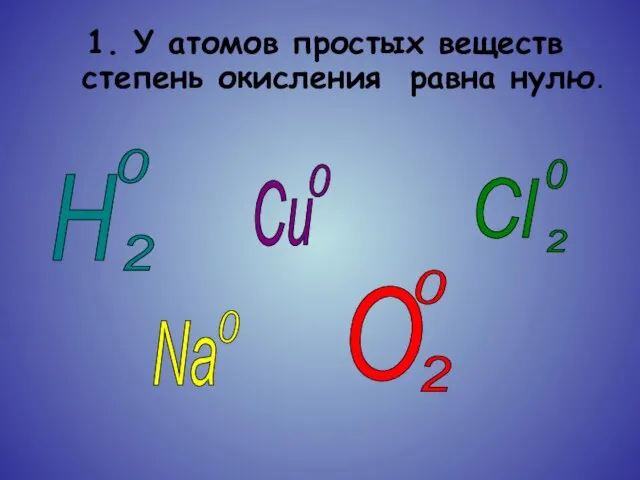
Слайд 141. У атомов простых веществ степень окисления равна нулю.
0
2
H
0
Cl
2
0
Cu
0
Na
Слайд 152. Степень окисления бывает:
Положительная
Отрицательная
Нулевая
+
Na
+2
Сa
+3
Al
0
2
H
0
Na
Cl
-

Слайд 163. Для более
электроотрицательного атома степень окисления высчитывают, как
№ группы -

8
Слайд 17Воспользуемся
Алгоритмом №1
для определения
степеней окисления.

Слайд 19Выполните задание №1 из Листов заданий.
Проверьте получившийся результат:
+4 -2 +4 -2

+7 -2 +6 -2
CO2, NO2, Cl2O7, CrO3
+4 -4 +4 -4 +14 -14 +6 -6
Слайд 20III.Составление формул по степеням окисления.

Слайд 21Воспользуемся
Алгоритмом №2
для составления формул.

Слайд 22даны элементы
более электроотрицательный
Si
O
и
6-8=-2
-2
+4
НОК
4
2
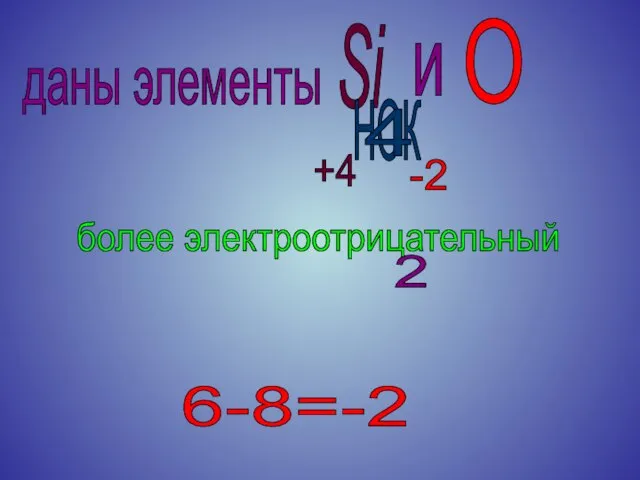
Слайд 23Выполните задание №2 из Листов заданий.
Проверьте получившийся результат:
НОК НОК НОК
6

6 5
+2 -3 +3 -2 +5 -
Mg N , Al S , PCl ,
3
2
2
3
5
Слайд 24IV.Номенклатура бинарных соединений.

Слайд 26Воспользуемся
Правилами номенклатуры бинарных соединений.

Слайд 27Для названия веществ воспользуйтесь таблицей
«Корни латинских названий некоторых элементов»

Слайд 28FeS
CrCl
3
P O
2
5
Na N
3
CaH
2
-
-
-
-
-
сульфид железа
хлорид хрома
гидрид кальция
нитрид натрия
оксид фосфора
(II)
(III)
(V)
Выполните задание №3 из

Листов заданий.
Слайд 29Домашнее задание.
§ 17 читать, упр 2 письменно.








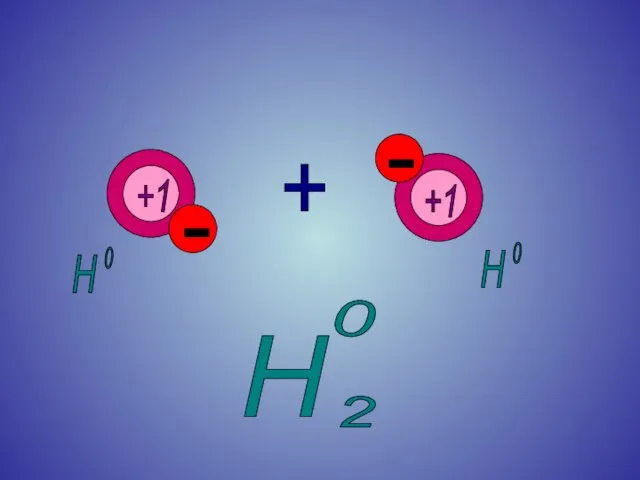










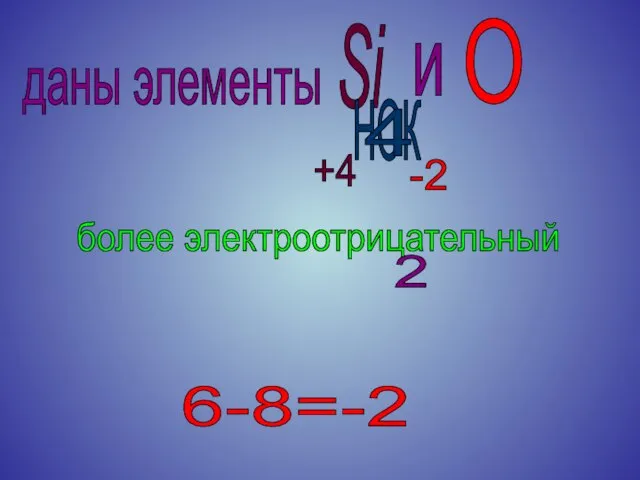







 Сложные эфиры. Жиры. Мыла
Сложные эфиры. Жиры. Мыла Алюминий. Применение
Алюминий. Применение Узагальнення знань з теми Вуглеводні
Узагальнення знань з теми Вуглеводні Классификация неорганических веществ
Классификация неорганических веществ Особенности строения вещества. Лекция №2. Строение кристаллов
Особенности строения вещества. Лекция №2. Строение кристаллов Степень окисления в соединениях
Степень окисления в соединениях Горные породы
Горные породы Основы химической термодинамики и термохимии. Лекция 5
Основы химической термодинамики и термохимии. Лекция 5 Гальванохимическая очистка. Сорбция
Гальванохимическая очистка. Сорбция 03. Основы номенклатуры
03. Основы номенклатуры Аппаратурное оформление процесса гидроочистки нефтяных фракций
Аппаратурное оформление процесса гидроочистки нефтяных фракций Многоатомные спирты
Многоатомные спирты Основания
Основания Органические вещества. 9 класс
Органические вещества. 9 класс Строение атома
Строение атома Модель атома
Модель атома Кислород
Кислород Природа и классификация химических связей
Природа и классификация химических связей Общие химические свойства металлов
Общие химические свойства металлов Тест по теме Основные классы неорганических соединений
Тест по теме Основные классы неорганических соединений Кислоты. Классификация сложных неорганических веществ
Кислоты. Классификация сложных неорганических веществ Типы химических реакций в органической химии
Типы химических реакций в органической химии Метан биогенный, абиогенный
Метан биогенный, абиогенный Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия
Реализация примерной адаптированной основной общеобразовательной программы по предмету Химия Природные источники углеводородов
Природные источники углеводородов Многоатомные спирты
Многоатомные спирты Презентация на тему Медь
Презентация на тему Медь  Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение
Технология производства пленок. Свойства полимерных пленочных материалов, модификация, применение