Содержание
- 2. Элемент, о котором пойдет речь на уроке, А.Е. Ферсман назвал “элементом мысли”. Открыт этот элемент в
- 3. Фосфор был открыт немецким алхимиком X. Брэндом в 1669 г. Позже А. Лавуазье доказал, что фосфор
- 4. период Фосфор как химический элемент III группа VА валентных электронов 5 степени окисления -3, +3, +5
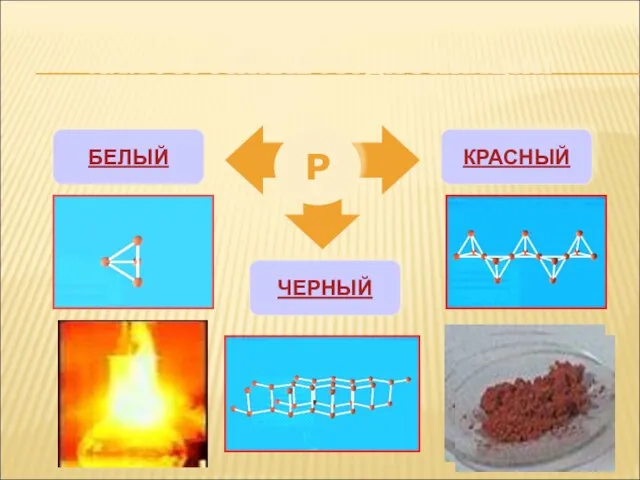
- 5. АЛЛОТРОПНЫЕ МОДИФИКАЦИИ Р БЕЛЫЙ КРАСНЫЙ ЧЕРНЫЙ
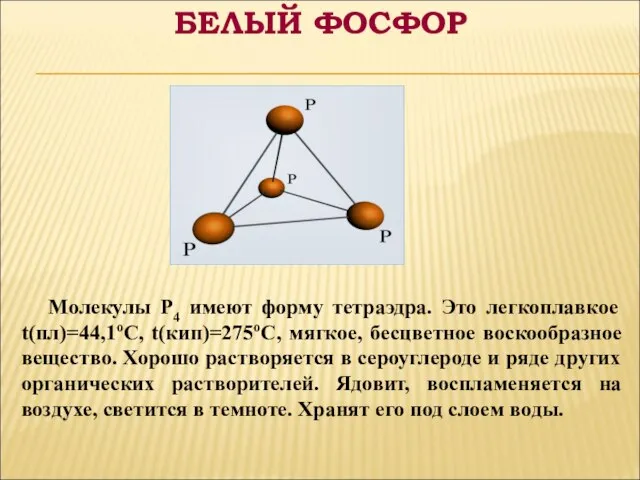
- 6. Молекулы P4 имеют форму тетраэдра. Это легкоплавкое t(пл)=44,1оС, t(кип)=275оС, мягкое, бесцветное воскообразное вещество. Хорошо растворяется в
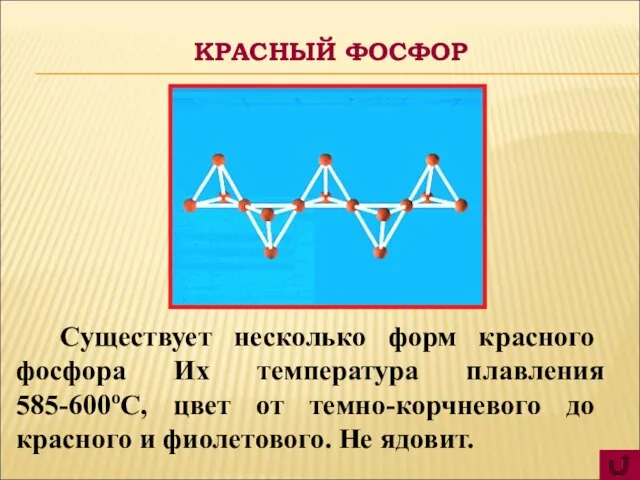
- 8. Существует несколько форм красного фосфора Их температура плавления 585-600оС, цвет от темно-корчневого до красного и фиолетового.
- 10. Черный фосфор имеет слоистую атомную кристаллическую решетку. По внешнему виду похож на графит, но является полупроводником.
- 12. Белый фосфор легко окисляется и самовоспламеняется на воздухе, поэтому его хранят под водой. Красный фосфор не
- 13. ХИМИЧЕСКИЕ СВОЙСТВА С металлами: Ca + P = C неметаллами: P + O2 = P +
- 14. с бертолетовой солью при ударе взрывается, воспламеняется: KClO3 + P = P2O5 + KCl
- 15. В промышленности фосфор получают из фосфоритов и апатитов, нагревая их в электрической печи без доступа воздуха
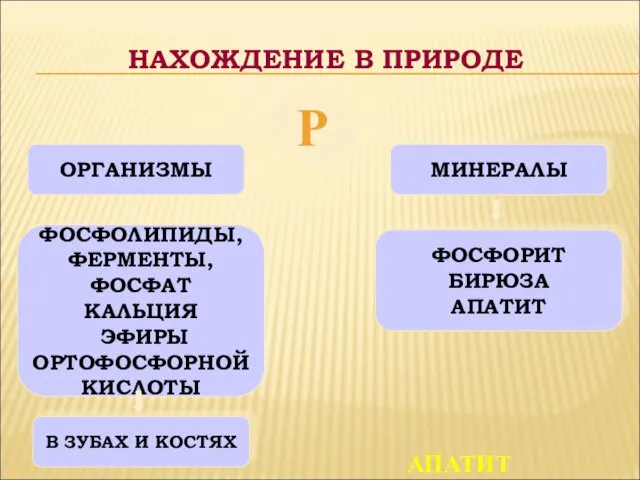
- 16. Р ОРГАНИЗМЫ МИНЕРАЛЫ ФОСФОЛИПИДЫ, ФЕРМЕНТЫ, ФОСФАТ КАЛЬЦИЯ ЭФИРЫ ОРТОФОСФОРНОЙ КИСЛОТЫ В ЗУБАХ И КОСТЯХ ФОСФОРИТ БИРЮЗА
- 17. НАХОЖДЕНИЕ ФОСФОРА В ПРИРОДЕ. В земной коре содержится около 0,08% фосфора. В природе фосфор содержится в
- 18. ФОСФОР В ОРГАНИЗМЕ ЧЕЛОВЕКА. Фосфор входит в состав белковых веществ в виде различных соединений. Содержание фосфора
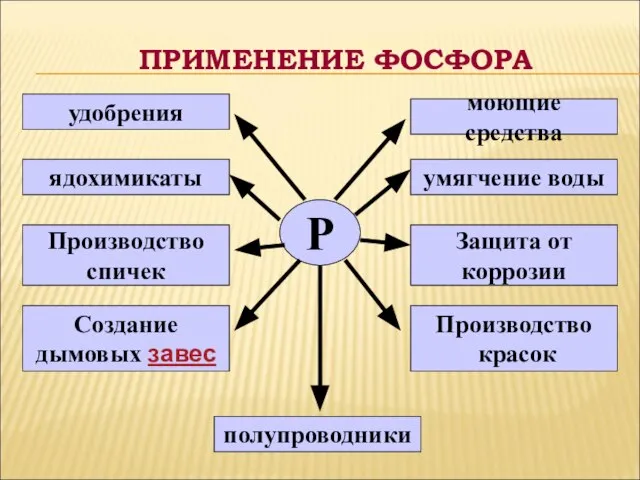
- 19. ПРИМЕНЕНИЕ ФОСФОРА Р удобрения ядохимикаты Производство спичек Создание дымовых завес полупроводники Производство красок Защита от коррозии
- 21. Скачать презентацию













 Графен. Нобелевская премия 2016
Графен. Нобелевская премия 2016 Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Реакции ионного обмена
Реакции ионного обмена Презентация на тему Интересные факты из жизни великого учёного Д. И. Менделеева
Презентация на тему Интересные факты из жизни великого учёного Д. И. Менделеева  Основы материаловедения. Раздел 1
Основы материаловедения. Раздел 1 Электронная структура атома углерода. Лекция 3
Электронная структура атома углерода. Лекция 3 Типы химических реакций
Типы химических реакций Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны
Полимеры с включением атомов бора и карборановой группировки - полиборорганосилоксаны и поликарборанорганосилосксаны Гидролиз солей
Гидролиз солей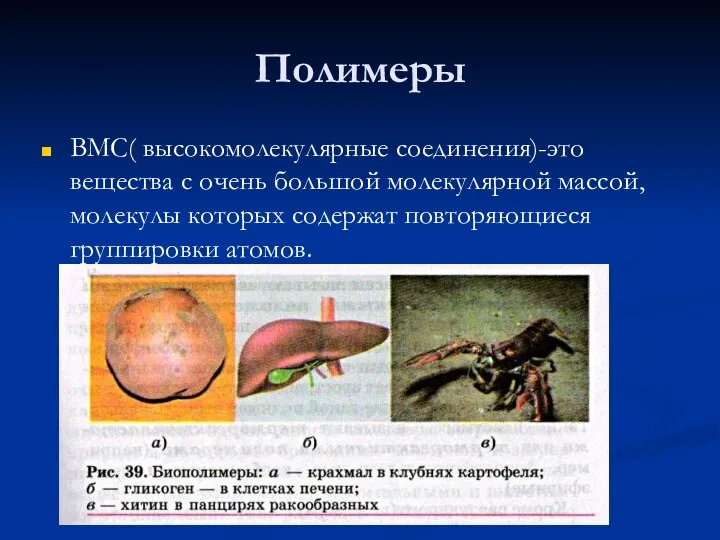 Полимеры
Полимеры Concise asymmetric total synthesis of lycopodine
Concise asymmetric total synthesis of lycopodine Основания. Равновесия в растворах
Основания. Равновесия в растворах Строение атома. Химическая связь
Строение атома. Химическая связь Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества Порох. Сера, халькогены
Порох. Сера, халькогены Сравнение активностей металлов
Сравнение активностей металлов Скорость химических реакций
Скорость химических реакций Химия в жизни общества
Химия в жизни общества Органическая химия
Органическая химия Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Серная кислота и для чего используется
Серная кислота и для чего используется Превращения в нашей жизни: физические и химические
Превращения в нашей жизни: физические и химические Школа юных ученых. Соль
Школа юных ученых. Соль Соли
Соли Строение углеводородов
Строение углеводородов Электродные процессы. Электроды. Потенциометрия
Электродные процессы. Электроды. Потенциометрия Презентация на тему Интересные факты из жизни Д. И. Менделеева
Презентация на тему Интересные факты из жизни Д. И. Менделеева  Нефть и её переработка
Нефть и её переработка