Содержание
- 2. Реакции Фаворского Обычно галогенкетон смешивают с концентрированным раствором основания (напр., в спирте) или с суспензией основания
- 3. Реакции Фаворского α,α-Дигалогенкетоны и α,αʹ-дигалогенкетоны, содержащие α-H-атомы* в условиях Фаворского реакции образуют одну и ту же
- 4. Основные побочные продукты - эпоксиэфиры ф-лы I, образующиеся из них гидроксикетали и α-гидроксикетоны, продукты расщепления связей
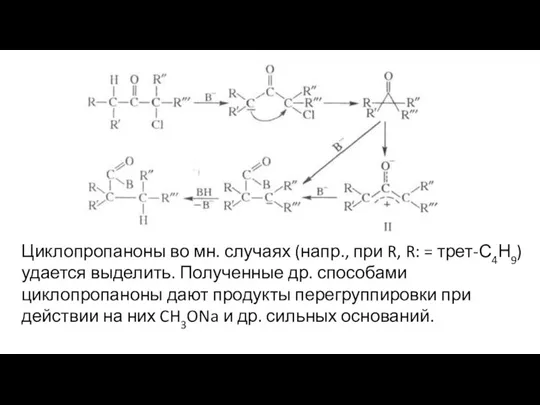
- 5. Циклопропаноны во мн. случаях (напр., при R, R: = трет-С4Н9)удается выделить. Полученные др. способами циклопропаноны дают
- 6. Реакции Фаворского Квазиперегруппировка Фаворского протекает по так называемому Семибензильному механизму:
- 7. Реакции Фаворского Превращения, аналогичные этой перегруппировке, претерпевают под действием оснований амиды α-галогенкарбоновых кислот, α-галогеналкилсульфамиды, α-галогеналкилсульфоны, α-гидроксикетоны
- 8. Реакция Реппе Синтез карбоновых кислот и их производных взаимодействуют СО с различными органическими соединениями (в т.ч.
- 9. Реакция Реппе Реппе реакция относится к реакциямциям карбонилирования. Ее осуществляют в присутствии карбонилов металлов (обычно карбонилы
- 10. Реакция Реппе Карбонилирование ацетилена приводит к акриловой кислоте. Монозамещенные ацетилены обычно образуют один продукт, дизамещенные-два возможных
- 11. Селективность карбонилирования сопряженных диенов значительно зависит от условий реакции. Так, в реакции 1,4-бутадиена в присутсвие пиридина
- 12. Карбонилирование метанола до уксусной кислоты с использованием карбонилов Со или Ni происходит в очень жестких условиях
- 13. Синтез простых и сложных виниловых эфиров, винил-сульфидов и виниламинов взаимодействия ацетилена со спиртами, фенолами, кислотами, меркаптанами
- 14. Механизм реакцииции включает стадию образования карбаниона (В-основание): В условиях Реппе реакции, используя в качестве катализаторов Zn-или
- 15. Конденсация ацетилена и его монозамещенных гомологов с альдегидами или кетонами (алкинолъный синтез), аминами (аминобутиновый синтез) или
- 16. В случае альдегидов (R' = Н) присоединение второй молекулы затрудняется с ростом длины углеводородной цепи. Аминобутиновый
- 17. Циклоолигомеризация ацетилена и его гомологов с образованием бензола, циклооктатетраена и их производных, а также циклополиолефинов более
- 18. Реакцию осуществляют при 60-120 °С и 1,5-2,5 МПа в органическом растворителе (бензоле, циклогексане, ТГФ, диоксане, ДМФА
- 19. http://www.xumuk.ru/encyklopedia/2/4688.html
- 21. Скачать презентацию

















 Драгоценные камни
Драгоценные камни Калифорний Cf
Калифорний Cf Понятие биотехнологии
Понятие биотехнологии Количество вещества. Моль. Молярная масса
Количество вещества. Моль. Молярная масса Вязкоупругие свойства полимеров
Вязкоупругие свойства полимеров Кремний и 4 группа. 9 класс
Кремний и 4 группа. 9 класс Строение и свойства металлов
Строение и свойства металлов Валентность химических элементов
Валентность химических элементов Строение веществ
Строение веществ Щелочноземельные металлы
Щелочноземельные металлы Актиний. Нахождение в природе
Актиний. Нахождение в природе Кремень. Нахождение в природе
Кремень. Нахождение в природе Исследование свойств модельной смеси сополимера Акритана-С с ЛД-70
Исследование свойств модельной смеси сополимера Акритана-С с ЛД-70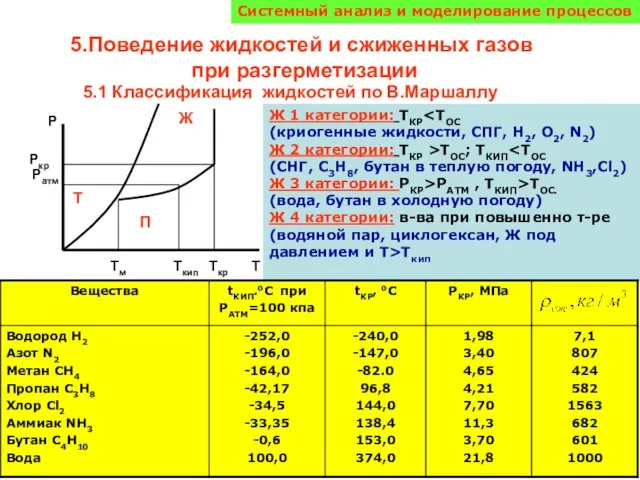 Поведение жидкостей и сжиженных газов при разгерметизации
Поведение жидкостей и сжиженных газов при разгерметизации Непредельные углеводороды. Алкены
Непредельные углеводороды. Алкены Типичные экспериментальные кинетические данные
Типичные экспериментальные кинетические данные Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь
Задача №2 Спящий Амур. Команда гимназии №1 Берлинская лазурь Окислительно-восстановительные реакции
Окислительно-восстановительные реакции Химические явления. Закон сохранения массы веществ
Химические явления. Закон сохранения массы веществ Химическая связь
Химическая связь Алифатические и ароматические амины
Алифатические и ароматические амины Окислительно-восстановительные реакции. 8 класс
Окислительно-восстановительные реакции. 8 класс Шаблон презентации по химии
Шаблон презентации по химии Выращивание кристаллов соли (домашний эксперимент)
Выращивание кристаллов соли (домашний эксперимент) Научные принципы химического производства
Научные принципы химического производства Материалы космической техники
Материалы космической техники Минералы
Минералы Вещества простые и сложные
Вещества простые и сложные