Содержание
- 2. Сплавы железа с углеродом, содержащие углерода от 2,14 до 6,67 % называют чугунами.
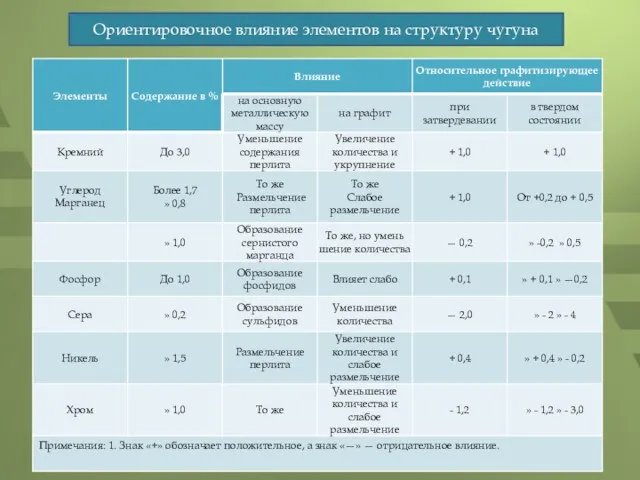
- 3. Ориентировочное влияние элементов на структуру чугуна
- 4. Процесс графитизации. Графит – это полиморфная модификация углерода. Способы образования графита в чугуне - из жидкой
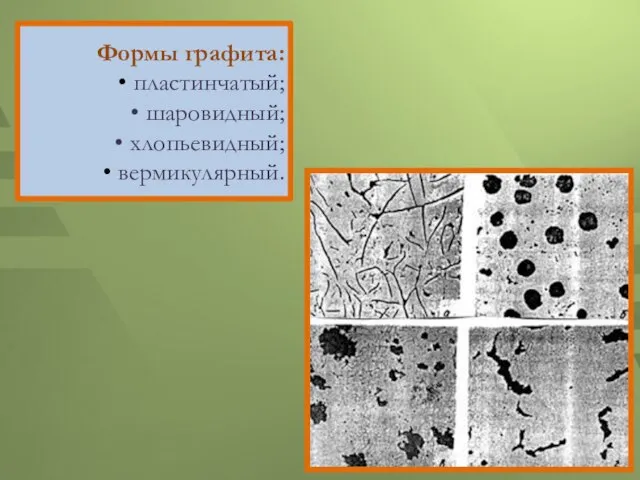
- 5. Формы графита: • пластинчатый; • шаровидный; • хлопьевидный; • вермикулярный.
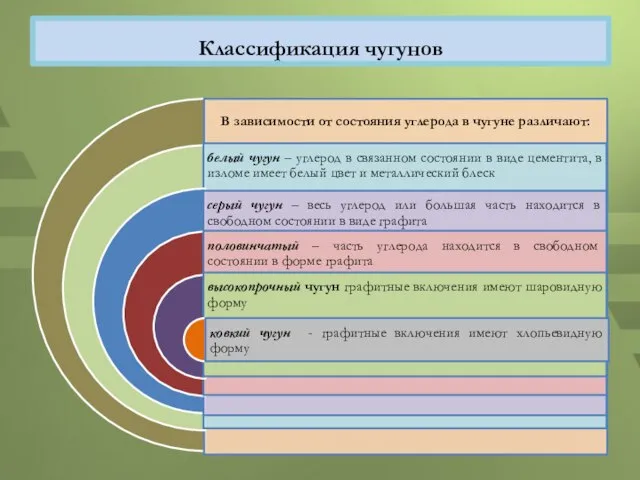
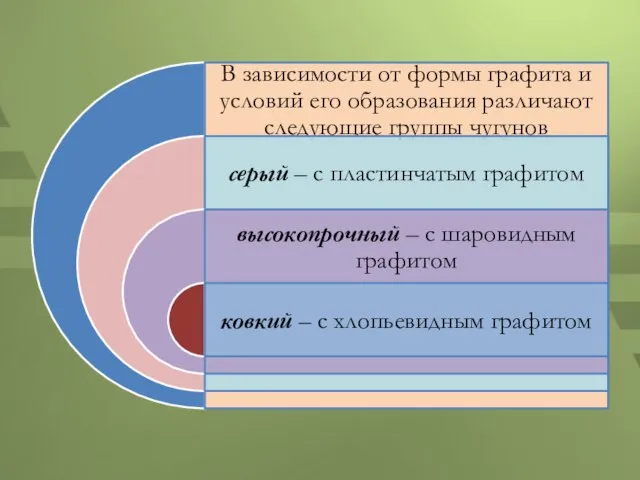
- 6. Классификация чугунов
- 8. Схемы микроструктур чугуна в зависимости от металлической основы и формы графитовых включений
- 9. Свойства Механические свойства серого чугуна зависят от количества и размера графитных включений. По сравнению с металлической
- 10. Применение Учитывая малое сопротивление отливок из серого чугуна растягивающим и ударным нагрузкам, следует использовать этот материал
- 11. Свойства Эти чугуны обладают высокой жидкотекучестью, линейная усадка – около 1%. Литейные напряжения в отливках несколько
- 12. Применение Из высокопрочного чугуна изготовляют тонкостенные отливки (поршневые кольца), шаботы ковочных молотов, станины и рамы прессов
- 13. Свойства Ферритные ковкие чугуны (КЧ 33-8, КЧ 37-12) имеют более высокую пластичность, а перлитные (КЧ 50-4,
- 14. Применение Отливки из ковкого чугуна применяют для деталей, работающих при ударных и вибрационных нагрузках. Из ферритных
- 15. Отбеленные и другие чугуны Отбеленные – отливки, поверхность которых состоит из белого чугуна, а внутри серый
- 16. Применение Используются для изготовления прокатных валов, вагонных колес с отбеленным ободом, шаров для шаровых мельниц. Для
- 17. Маркировка чугунов СЧ23 КЧ30-6 ВЧ35-22 СЧ15 КЧ30-6
- 18. Серый чугун маркируется буквами СЧ с добавлением цифры, которая указывает предел прочности чугуна при растяжении. Например:
- 19. Ковкий чугун маркируется буквами КЧ и цифрами. Первые две цифры указывают предел прочности на растяжение, а
- 20. Высокопрочный чугун маркируется буквами ВЧ и цифрами. Первые две цифры указывают предел прочности на растяжение, а
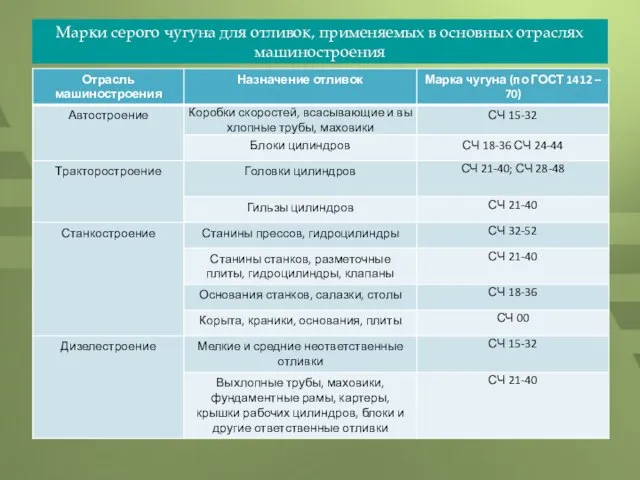
- 21. Марки серого чугуна для отливок, применяемых в основных отраслях машиностроения
- 23. Скачать презентацию














 Применение алкенов
Применение алкенов Кристаллы и минералы
Кристаллы и минералы Презентация по химии на тему _Высокомолекулярные Соединения_ (1)
Презентация по химии на тему _Высокомолекулярные Соединения_ (1) Презентация на тему Коллоидная химия
Презентация на тему Коллоидная химия  Хімічні формули
Хімічні формули Презентация на тему Витамин C
Презентация на тему Витамин C  Полимеры. Получение и применение полимеров
Полимеры. Получение и применение полимеров Материалы космической техники
Материалы космической техники Сера
Сера Презентация по Химии "Соединения алюминия"
Презентация по Химии "Соединения алюминия"  Основания: номенклатура, классификация, применение, физические свойства
Основания: номенклатура, классификация, применение, физические свойства Химический элемент калий
Химический элемент калий Химическая термодинамика. Термодинамические потенциалы
Химическая термодинамика. Термодинамические потенциалы Серная кислота H2SO4
Серная кислота H2SO4 Характеристика элемента по его положению в периодической системе
Характеристика элемента по его положению в периодической системе Ароматические углеводороды
Ароматические углеводороды Соли
Соли Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме
Масс-спектрометрия – аналитический метод определения молекулярной массы свободных ионов в высоком вакууме Валентность химических элементов
Валентность химических элементов Презентация на тему Химические свойства алкенов
Презентация на тему Химические свойства алкенов  proekt_TTU_3_1
proekt_TTU_3_1 Полиморфизм кристаллов изатина
Полиморфизм кристаллов изатина Химия в быту
Химия в быту Количество вещества. Моль
Количество вещества. Моль Презентация на тему Угольная и кремниевая кислоты и их соли
Презентация на тему Угольная и кремниевая кислоты и их соли  Классификация методов переработки пластмасс
Классификация методов переработки пластмасс Презентация на тему Химические реакции
Презентация на тему Химические реакции  Сера. Физические и химические свойства. Нахождение в природе
Сера. Физические и химические свойства. Нахождение в природе