Содержание
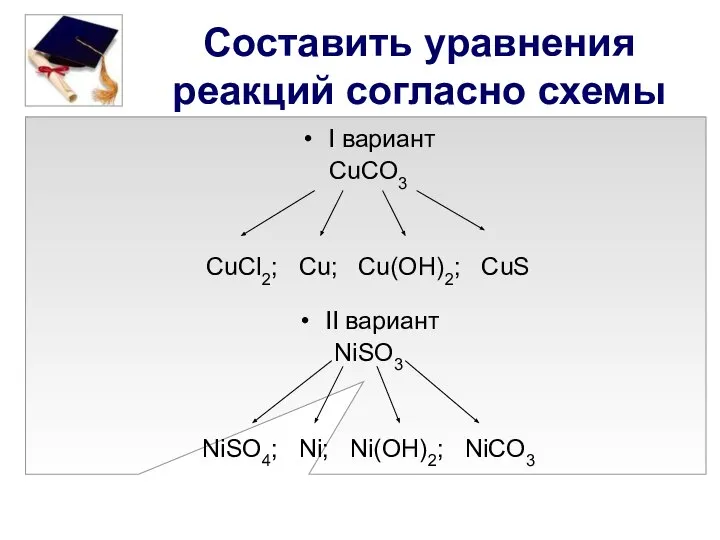
- 2. Составить уравнения реакций согласно схемы I вариант CuCO3 CuCl2; Cu; Cu(OH)2; CuS II вариант NiSO3 NiSO4;
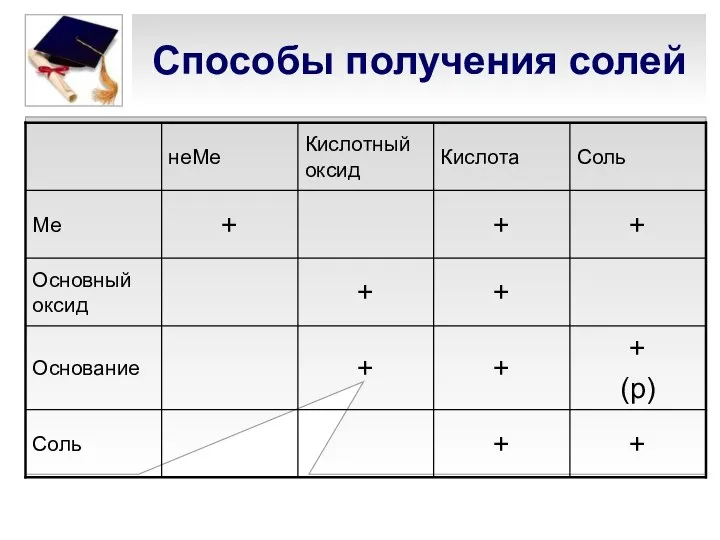
- 3. Способы получения солей
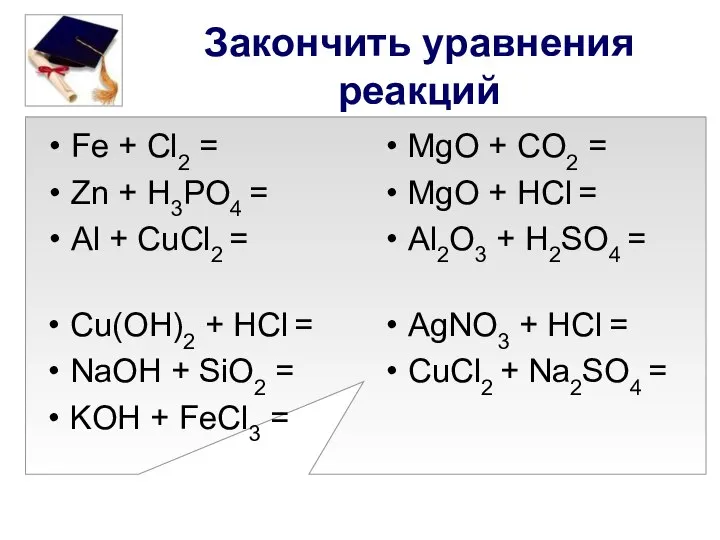
- 4. Закончить уравнения реакций Fe + Cl2 = Zn + H3PO4 = Al + CuCl2 = MgO
- 5. Составьте уравнения реакций нейтрализации, в результате которых образуются следующие соли. Хлорид Al Сульфат Ba Нитрат Ba
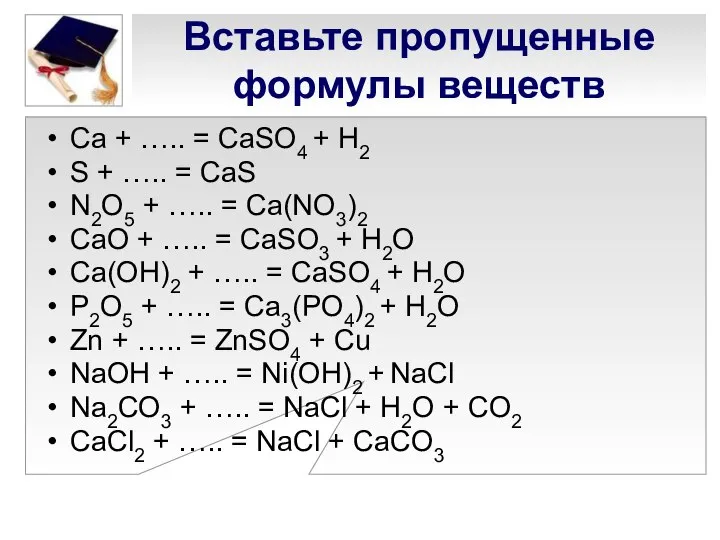
- 6. Вставьте пропущенные формулы веществ Ca + ….. = CaSO4 + H2 S + ….. = CaS
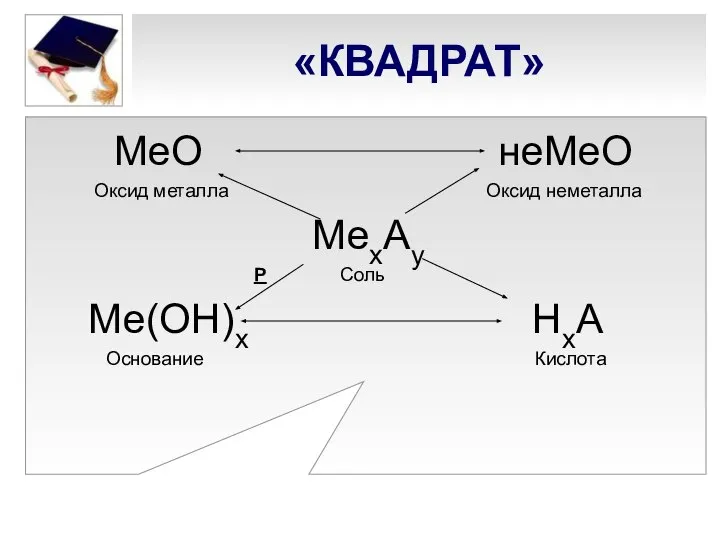
- 7. «КВАДРАТ» МеО неМеО Оксид металла Оксид неметалла МехАу Р Соль Ме(ОН)х НхА Основание Кислота
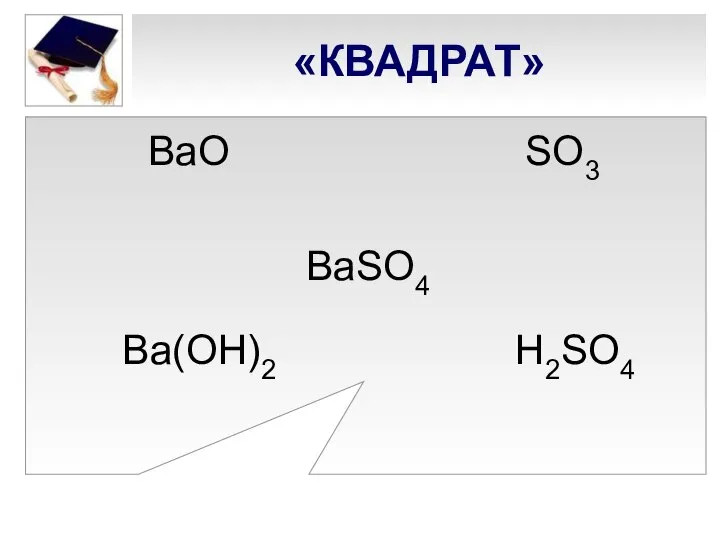
- 8. «КВАДРАТ» BaО SО3 BaSO4 Ba(ОН)2 Н2SO4
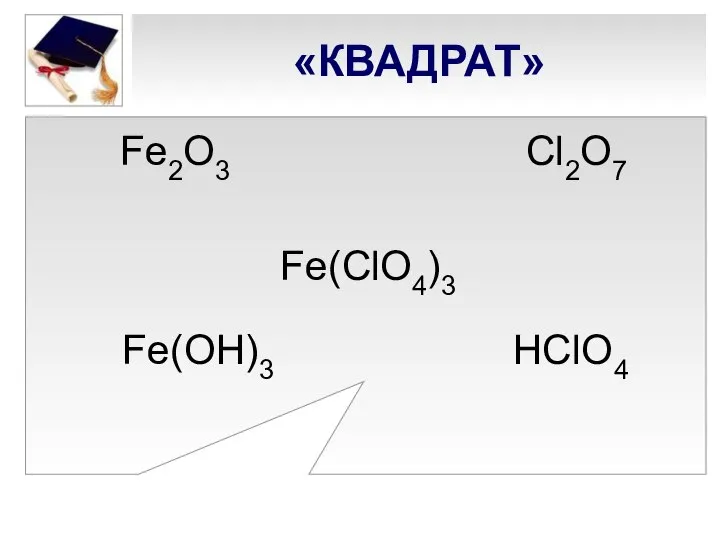
- 9. «КВАДРАТ» Fe2O3 Cl2О7 Fe(ClO4)3 Fe(ОН)3 НClO4
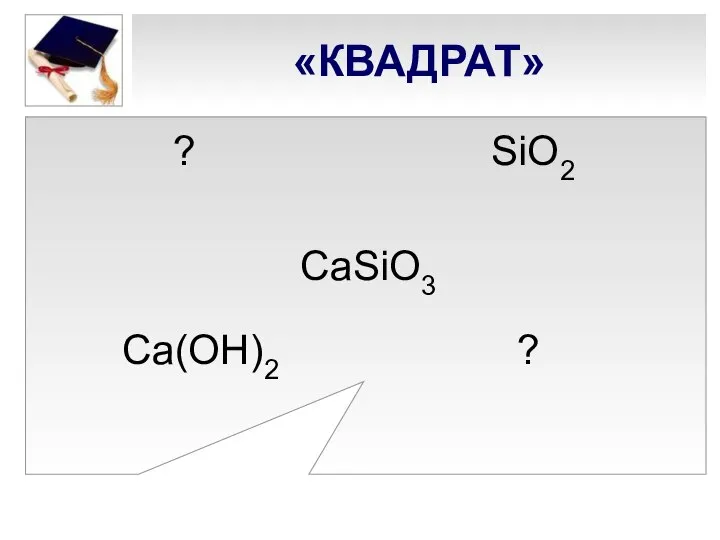
- 10. «КВАДРАТ» ? SiО2 CaSiO3 Ca(ОН)2 ?
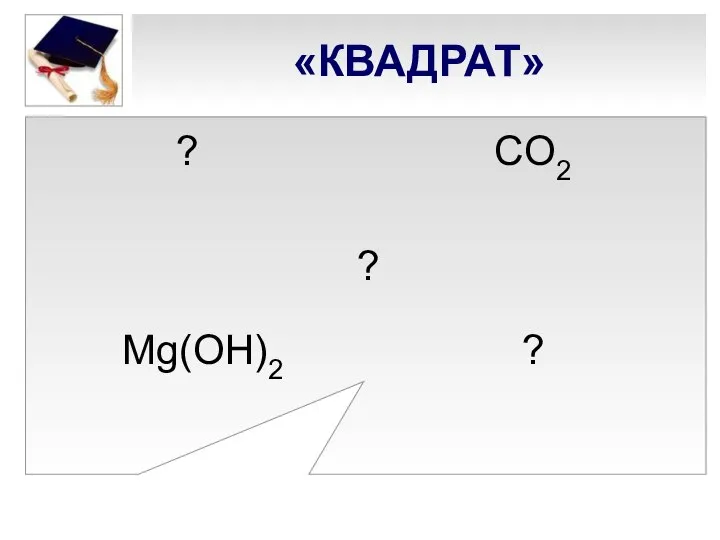
- 11. «КВАДРАТ» ? CО2 ? Mg(ОН)2 ?
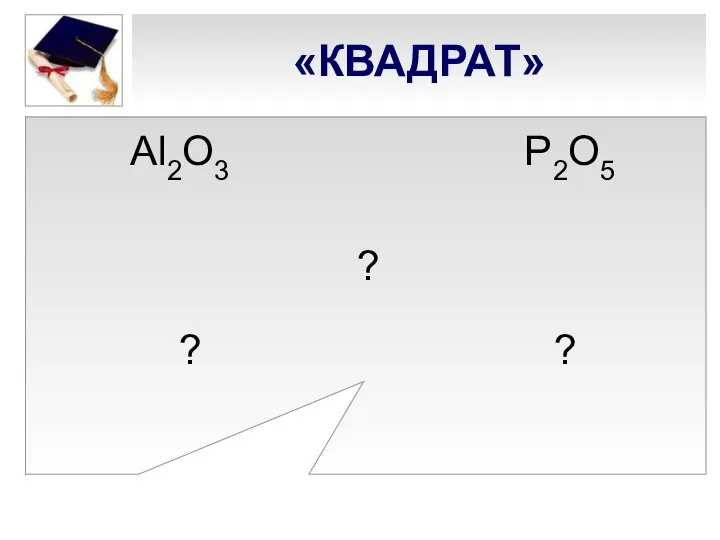
- 12. «КВАДРАТ» Al2O3 P2О5 ? ? ?
- 14. Скачать презентацию

 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества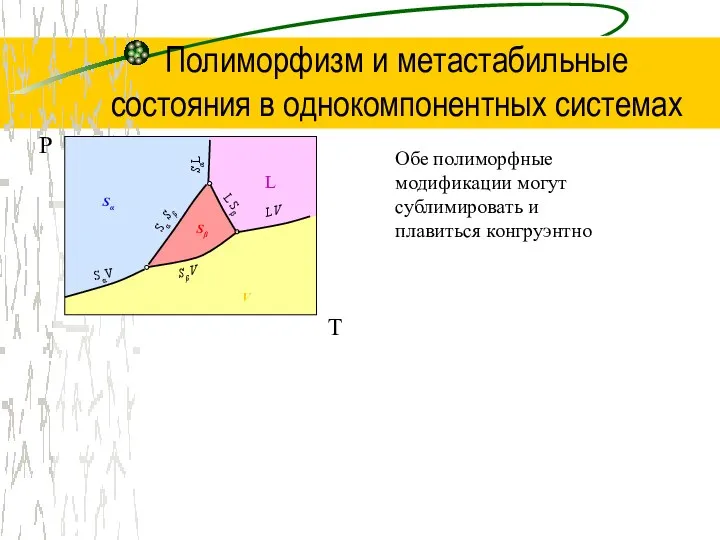 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі