Содержание
- 2. Thermo – тепло Термохимия вокруг: ДВС, турбины, плиты История: огонь, термоеда, обогрев (и охлаждение!) Тепло и
- 3. Thermo – ТЕРМО... [от греч. thermē тепло, жар] Первая часть сложных слов: 1.Относящийся к теплоте, температуре.
- 4. ТЕРМО... в химии ТЕРМОХИМИЯ, раздел физической химии, изучающий ТЕПЛОВЫЕ эффекты, сопровождающие химические процессы: выделение или поглощение
- 5. ТЕРМО... в химии В широкой трактовке Большинство реакций протекают под действием тепла Кроме фотохимических, радиационно-химических, механохимических)
- 6. Термохимия вокруг: ДВС, турбины, плиты И многое, многое другое
- 7. История: огонь, термоеда, обогрев (и охлаждение!)
- 8. Тепло и холод Попробуйте определить эти понятия Почему t = 0°C, но T = 273 K?
- 9. Что такое Т = 0 К? Может ли быть Т
- 10. Теория теплорода (Лавуазье) XXVIII – начало XIX века Чем больше теплорода в веществе, тем оно теплее.
- 11. Опыт Б. Томсона (графа Румфорда) 1798 Б. Томсон (гр. Румфорд) 1753 - 1814
- 12. Опыт Х. Дэви с трением льда 1799 Х. Дэви 1778 - 1829
- 13. 20 °С = 36 °F = 16 °R
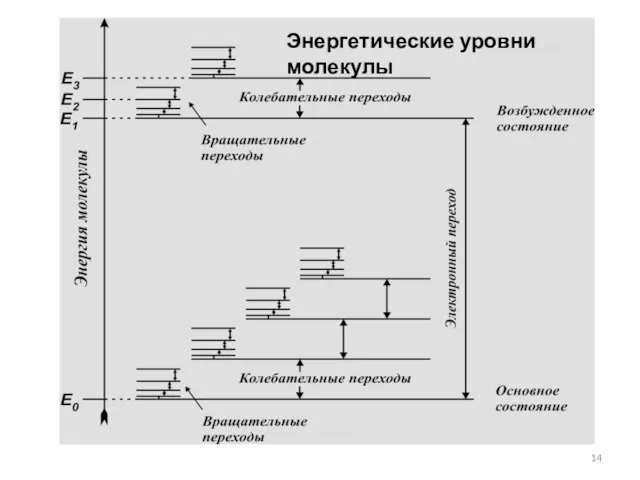
- 14. Энергетические уровни молекулы
- 15. E(пост.) = 3×(1/2) ×kT E(вращ.) = 3×(1/2) ×kT E(кол.) = i×kT ~ Т E(тепл.) = E(пост.)
- 16. Если кажется, что вам холодно – это неправда! Просто вам недостаточно тепло. В науке есть только
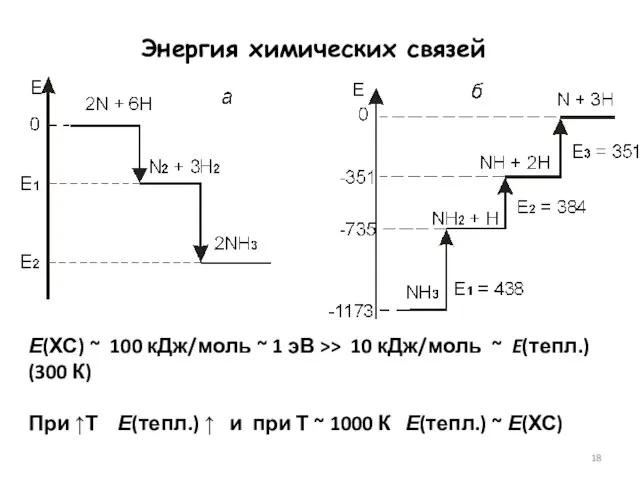
- 18. Е(ХС) ~ 100 кДж/моль ~ 1 эВ >> 10 кДж/моль ~ E(тепл.) (300 К) При ↑Т
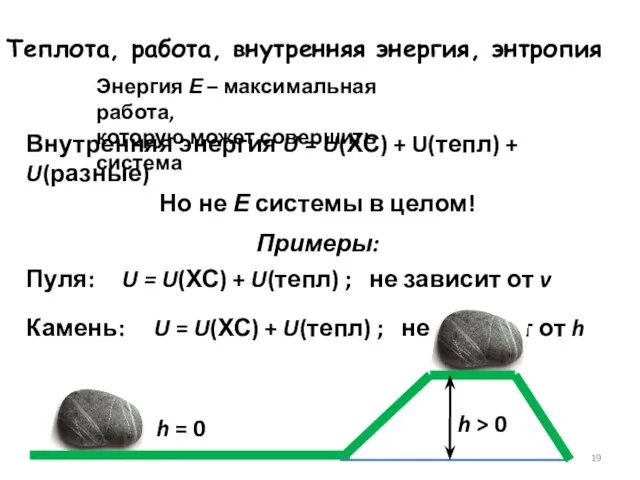
- 19. Теплота, работа, внутренняя энергия, энтропия Энергия Е – максимальная работа, которую может совершить система Внутренняя энергия
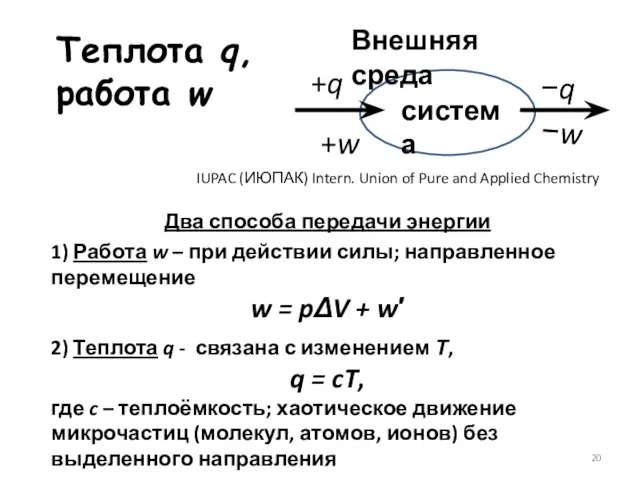
- 20. Теплота q, работа w Два способа передачи энергии 1) Работа w – при действии силы; направленное
- 21. система Внешняя среда +q −q +w −w 1-е начало термодинамики ΔU = q + w q
- 22. Энтальпия H = U + pV ΔH = ΔU + рΔV = Qp при p =
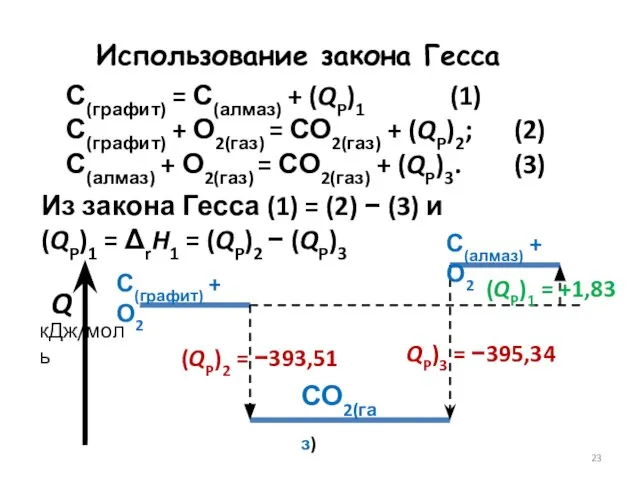
- 23. С(графит) = С(алмаз) + (QP)1 (1) С(графит) + О2(газ) = СО2(газ) + (QP)2; (2) С(алмаз) +
- 24. Энтропия S = Δq/T S = k×lnΩ Δ S ≥ Δq/T Δ S = Δq/T при
- 25. 1 2 3 Ω = 3 Ω = 1 S = k×ln1 = 0 S =
- 26. Невозможна самопроизвольная передача теплоты от холодного тела к теплому. Клаузиус лед тает, а не наоборот при
- 27. Энтропия Вселенной как замкнутой системы стремится к максимуму, и в конце концов во Вселенной закончатся все
- 28. Вопрос: Возможно ли состояние, при котором все молекулы воздуха окажутся в одной половине аудитории, или это
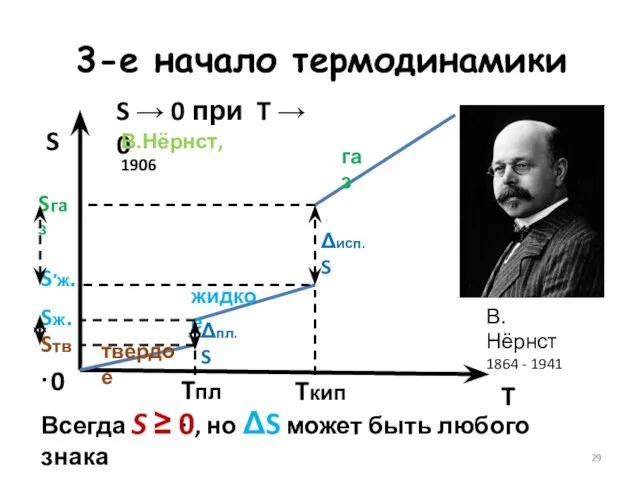
- 29. 3-е начало термодинамики S T Tпл. Tкип. 0 твердое жидкое газ S → 0 при T
- 30. 1 – Энергия Вселенной постоянна 2 – Энтропия Вселенной стремится к максимуму А. Зоммерфельд: Закон сохранения
- 31. Объединение 1-го и 2-го начала Энергия (функция) Гиббса G = H - TS ΔrG = ΔrG°
- 32. Критерии равновесия для изобарно-изотермических процессов Дж. Гиббс 1839 - 1903
- 33. lnK = –ΔrG° / RT = –ΔrH° / RT + ΔrS° / R lnK = А
- 34. 2NaHCO3(тв.) + SO2(газ) = Na2SO3(тв.) + 2CO2(газ) + H2O(газ) КС = [SO3]2 / [SO2]2 · [O2];
- 35. «гептил» – несимм. диметил гидразин H CH3 N N H CH3 6NH4ClO4 + 10Al = 3N2
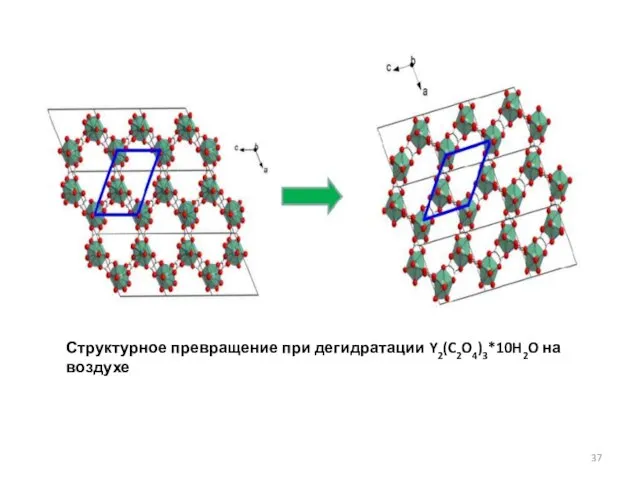
- 36. Изменение формы кристалла Y2(C2O4)3*10H2O при дегидратации на воздухе Реакция Y2(C2O4)3*10H2O = Y2(C2O4)3*6H2O + 4H2O(газ)
- 37. Структурное превращение при дегидратации Y2(C2O4)3*10H2O на воздухе
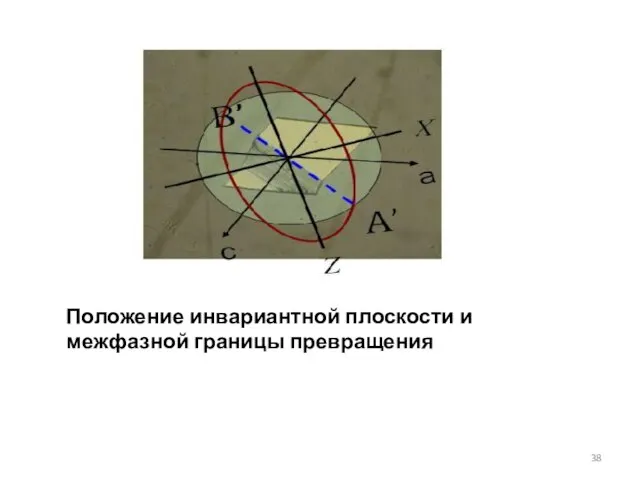
- 38. Положение инвариантной плоскости и межфазной границы превращения
- 39. Изменние формы кристалла Y2(C2O4)3*10H2O при дегидратации при повышенной влажности
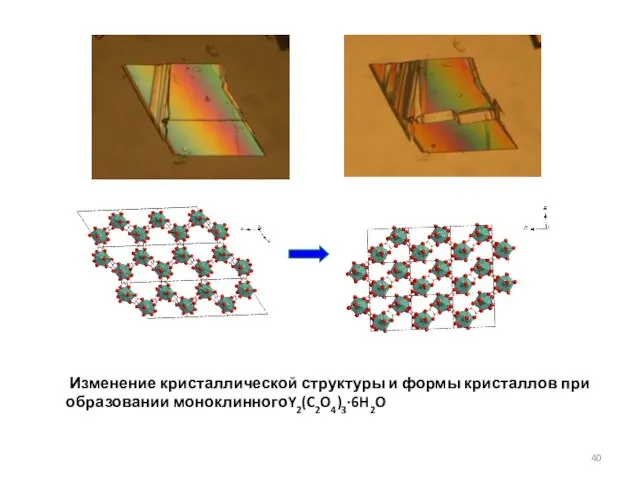
- 40. Изменение кристаллической структуры и формы кристаллов при образовании моноклинногоY2(C2O4)3∙6H2O
- 42. Скачать презентацию

![Thermo – ТЕРМО... [от греч. thermē тепло, жар] Первая часть сложных слов:](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/851676/slide-2.jpg)























![2NaHCO3(тв.) + SO2(газ) = Na2SO3(тв.) + 2CO2(газ) + H2O(газ) КС = [SO3]2](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/851676/slide-33.jpg)



 Химические реакции в органической химии
Химические реакции в органической химии Графический диктант. Азот и Аммиак
Графический диктант. Азот и Аммиак Неньютоновская жидкость
Неньютоновская жидкость Язык естествознания. Химия
Язык естествознания. Химия Презентация на тему Химия и сельское хозяйство Пестициды
Презентация на тему Химия и сельское хозяйство Пестициды  Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах
Экстракция молибдена из азотнокислых растворов карбамоилметилфосфиноксидом, растворенным в высших спиртах 12 принципов зелёной химии
12 принципов зелёной химии Алканы
Алканы Химическая связь. Строение вещества
Химическая связь. Строение вещества Диены. Понятие о диенах
Диены. Понятие о диенах Минералы и горные породы
Минералы и горные породы Типы химических реакций. 8 класс
Типы химических реакций. 8 класс Кварцевые пески
Кварцевые пески Вода как хладагент (R718)
Вода как хладагент (R718) Кроссворд по теме Металлы
Кроссворд по теме Металлы Оксиды
Оксиды Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Щелочные металлы
Щелочные металлы Органическая химия
Органическая химия Периодическая система химических элементов. Периоды. Группы
Периодическая система химических элементов. Периоды. Группы Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна
Углерод 9 класс Подготовила учитель химии СШ№16 Самойлова Регина Львовна Кислород – основа жизни?
Кислород – основа жизни? Урок-путешествие по теме «Первоначальные химические понятия»
Урок-путешествие по теме «Первоначальные химические понятия» Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии
Метод высокоэффективной жидкостной хроматографии и тандемной масс-спектрометрии Введение в органическую химию. Состав и структура органических веществ
Введение в органическую химию. Состав и структура органических веществ Многоатомные спирты
Многоатомные спирты Строение атома. Планетарная модель атома Резерфорда
Строение атома. Планетарная модель атома Резерфорда Презентация по Химии "Химическая номенклатура и филология"
Презентация по Химии "Химическая номенклатура и филология"