Содержание
- 2. Изучить тему по ссылкам: http://ru.solverbook.com/spravochnik/ximiya/11-klass/amfoternye-organicheskie-i-neorganicheskie-soedineniya/ https://www.youtube.com/watch?v=-_EQTpNTRs0
- 3. Амфотерные соединения Амфотерными называют соединения, которые в зависимости от условий могут быть как донорами катионов водорода
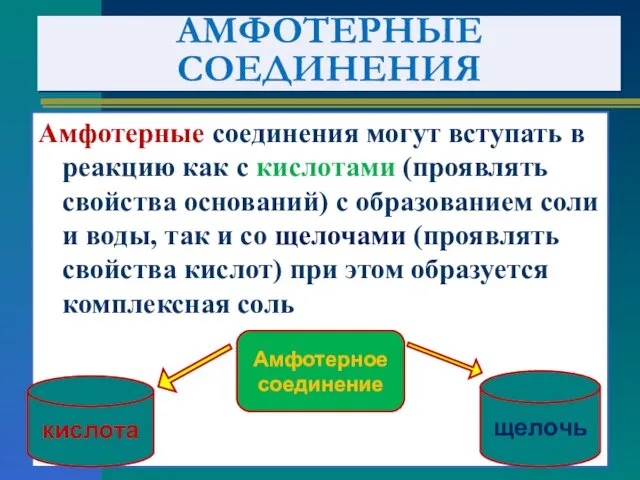
- 4. АМФОТЕРНЫЕ СОЕДИНЕНИЯ Амфотерные соединения могут вступать в реакцию как с кислотами (проявлять свойства оснований) с образованием
- 5. Амфотерные соединения Такими являются в неорганической химии: Аl(ОН)3, Zn(ОН)2, Cr(ОН)3, Ве(ОН)2, Gе(ОН)2, Sn(ОН)4, Pb(ОН)2 и др.
- 6. В реакциях с кислотами амфотерные оксиды ведут себя как основные оксиды Например: Аl2О3 + 6НСl =
- 7. Амфотерные гидроксиды взаимодействуют с растворами кислот и ведут себя как нерастворимые основания Аl(ОН)3 + ЗНСl =
- 8. Свойства аминокислот NH2 – CH – C O OH R Аминогруппа, – NH2 – акцептор водорода,
- 9. Кислотные свойства аминокислот NH2 – R – COOH + NaOH = NH2 – R – COONa
- 10. Основные свойства аминокислот COOH – R – NH2 + HCl = COOH – R – NH3
- 12. Скачать презентацию








 Метилэтилкетон. Его применение и процесс получения
Метилэтилкетон. Его применение и процесс получения Презентация на тему В мире полимеров
Презентация на тему В мире полимеров  Сферы применения CaCO3
Сферы применения CaCO3 Арены. Бензол
Арены. Бензол Пути использования активной уксусной кислоты
Пути использования активной уксусной кислоты Органическая химия
Органическая химия Катализаторы и катализ
Катализаторы и катализ Скорость химической реакции
Скорость химической реакции Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы
Ферменттер.Ферменттердің құрылымы.Биохимиялық маңызы реакцмм алканов новое (1)
реакцмм алканов новое (1) Химическая реакция
Химическая реакция Сода: мифы и реальность
Сода: мифы и реальность Силикатная промышленность
Силикатная промышленность Валентность
Валентность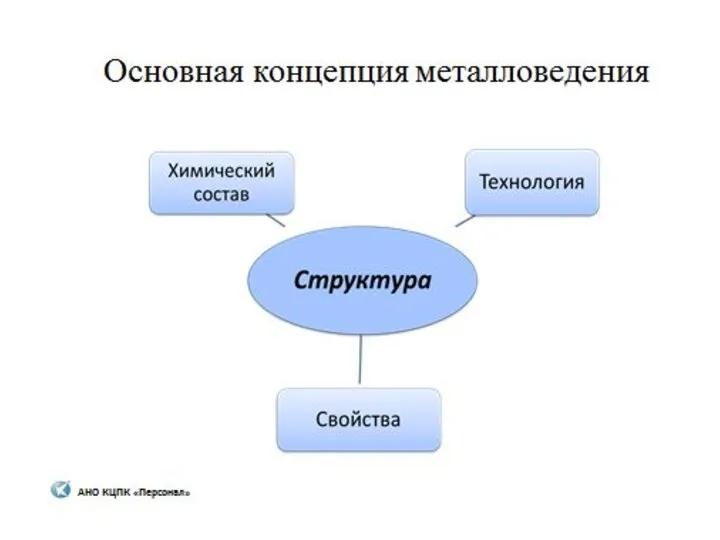 Металловедение
Металловедение Углеводороды. Характеристика
Углеводороды. Характеристика Кремний. Технический кремний
Кремний. Технический кремний бирюза
бирюза Углеводы
Углеводы Ионо-дисперсное состояние микрокомпонентов в растворах
Ионо-дисперсное состояние микрокомпонентов в растворах Скорость химической реакции. Химическое равновесие
Скорость химической реакции. Химическое равновесие Природные источники углеводородов
Природные источники углеводородов Получение и химические свойства оксидов
Получение и химические свойства оксидов Признаки химических реакций
Признаки химических реакций Презентация на тему Растворы (11 класс)
Презентация на тему Растворы (11 класс)  Оксиды. Классификация и химические свойства
Оксиды. Классификация и химические свойства Относительная атомная масса Урок 8 класс Учитель химии Чиркунова Л.А.
Относительная атомная масса Урок 8 класс Учитель химии Чиркунова Л.А. Мастер - класс: Окислительно-восстановительные реакции
Мастер - класс: Окислительно-восстановительные реакции