Слайд 2 Едва ли найдётся другое, искусственно добываемое, вещество, столь часто применяемое в

технике, как серная кислота. Там, где техническая деятельность развита, там потребляется и много серной кислоты.
Д. И. Менделеев
Слайд 3Реакции разбавленной серной кислоты с активными металлами
2Li + H2 SO4 = Li2SO4

+ H2 ↑
Li 0 - 1 e → Li+ *2 восстановитель
2H + + 2e → H2 0 окислитель
Ca + H2 SO4 = CaSO4 + H2 ↑
Ca 0 - 2 e → Ca 2 восстановитель
2H + + 2e → H2 0 окислитель
Слайд 4Реакции разбавленной серной кислоты с металлами средней активности
Zn + H2SO4 =

ZnSO4 + H2 ↑
Zn0 - 2e → Zn 2+ восстановитель
2H+ + 2e → H2 окислитель
Слайд 5Реакции разбавленной серной кислоты с алюминием и железом
2Al + 3H2 SO4 =

Al2(SO4)3+3H2 ↑
Al0 – 3e →Al+3 *2 восстановитель
2H+ + 2e → H2 *3 окислитель
Fe+ H2SO4 = FeSO4 + H2↑
Fe0 -2e →Fe+2 *1 восстановитель
2H+ + 2e → H2 *1 окислитель
Слайд 6Реакции разбавленной серной кислоты с малоактивными металлами
Cu + H2SO4 - не взаимодействует

Слайд 7Реакции концентрированной серной кислоты с активными металлами
8Na + 5H2 SO4 (k) =

H2S + 4Na2SO4 + 4H2O
Na 0 - 1 e → Na+ *8 восстановитель
S+6 +8e →S-2 *1 окислитель
Слайд 8Реакции концентрированной серной кислоты с металлами средней активности
Zn + 2H2 SO4 =

ZnSO4 + 2H2O + SO2
Zn 0 - 2 e → Zn+ 2 восстановитель
S+6 + 2 e → S+4 окислитель
4Zn + 5H2 SO4 = 4ZnSO4 + 4H2O + H2S
Zn 0 - 2 e → Zn+ 2 *4 восстановитель
S+6 + 8 e → S-2 *1 окислитель
3Zn + 4H2 SO4 = 3ZnSO4 + 4 H2O + S
Zn 0 - 2 e → Zn+ 2 *3 восстановитель
S+6 + 6 e → S0 *1 окислитель
Слайд 9Реакции концентрированной серной кислоты с алюминием и железом
На холоде концентрированная серная кислота

пассивирует многие металлы, в том числе РЬ, Cr, Ni, сталь, чугун.При нагревании реакционной смеси происходит химическая реакция:
8Al+15 H2SO4 =4 Al2(SO4)3+3H2S↑ +12H2O
Al0 – 3e →Al+3 *8 восстановитель
S+6 +8e →S-2 *3 окислитель
8Fe+15 H2 SO4 =4 Fe2(SO4)3+3H2 S↑ +12H2O
Fe0 – 3e →Fe+3 *8 восстановитель
S+6 +8e →S-2 *3 окислитель
Слайд 10Реакции концентрированной серной кислоты с малоактивными металлами
Cu + 2H2 SO4 = CuSO4

+ 2H2O + SO2
Cu 0 - 2 e → Cu+ 2 восстановитель
S+6 + 2 e → S+4 окислитель
Слайд 11Реакции концентрированной серной кислоты с неметаллами
S + 2H2 SO4 = 2H2O +

3SO2
S 0 - 4 e → S+4 восстановитель
S +6 + 2 e → S+4 *2 окислитель
2P + 5H2 SO4 = 2H3PO4 + 5SO2 + 2H2O
P 0 - 5 e → P 5+ *2 восстановитель
S 6+ +2e → S+4 *5 окислитель
Слайд 12Взаимодействие концентрированной серной кислоты с органическими веществами
С12Н22О11 + H2 SO4 =
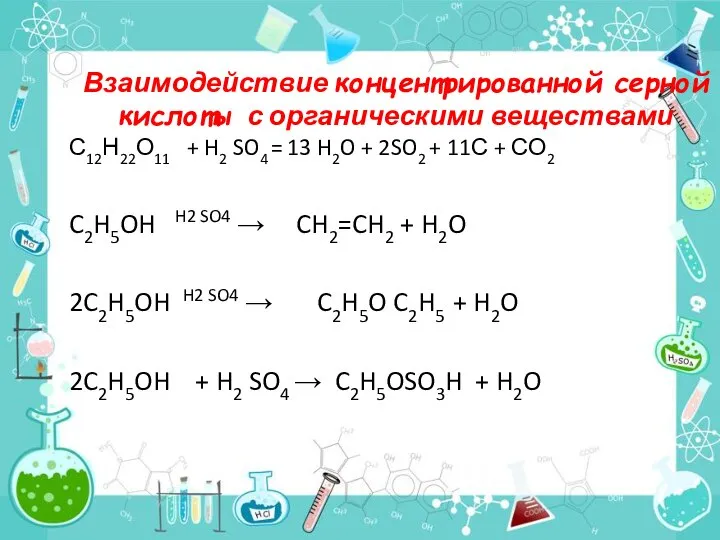
13 H2O + 2SO2 + 11С + СО2
C2H5OH H2 SO4 → CH2=CH2 + H2O
2C2H5OH H2 SO4 → C2H5O C2H5 + H2O
2C2H5OH + H2 SO4 → C2H5OSO3H + H2O











 Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Квантовая химия
Квантовая химия Алкены Бутен
Алкены Бутен Металлы
Металлы Химический диктант по органической химии. 9 класс
Химический диктант по органической химии. 9 класс Химические реакции. Классификация
Химические реакции. Классификация Знакомство с химией
Знакомство с химией Применение каучука
Применение каучука Неорганический мозговой штурм
Неорганический мозговой штурм Практическая работа: Очистка загрязнённой поваренной соли
Практическая работа: Очистка загрязнённой поваренной соли Буферные системы
Буферные системы Cеминар 6 -Алканы-2
Cеминар 6 -Алканы-2 Химические реакции
Химические реакции Электроосмос. Практическое применение электроосмоса
Электроосмос. Практическое применение электроосмоса Магматические горные породы
Магматические горные породы 1_
1_ Физические и химические свойства металлов
Физические и химические свойства металлов Строение электронных оболочек атома
Строение электронных оболочек атома Железо
Железо Производные салициловой, пара-аминобензойной кислот, применяемые в медицине
Производные салициловой, пара-аминобензойной кислот, применяемые в медицине коррозия металлов
коррозия металлов Индикаторная бумага
Индикаторная бумага Тренажер - Валентность. 8 класс
Тренажер - Валентность. 8 класс Потенциометрический анализ, титрование
Потенциометрический анализ, титрование Алкины
Алкины Лучший тест для подготовки к ЕГЭ по химии
Лучший тест для подготовки к ЕГЭ по химии Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ
Тривиальные названия веществ, наиболее часто встречаемых в ЕГЭ Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)
Блок колонн на установке замедленного коксования производительностью 730000 тонн/год гудрона (поз.к-1, кх-1)