Содержание
- 2. Ważne! Podczas rozwiązywania zadań, w których mamy do czynienia ze zmianą stężenia, warto oznaczyć cyfrą „1”
- 8. W celu obliczenia proporcji, w jakich należy zmieszać roztwór bardziej stężony w rozpuszczalnikiem albo z roztworem
- 9. Przykład 3 Ile gramów wody należy dodać do 20g 30% roztworu KOH, aby otrzymać roztwór 12%?
- 11. Przeliczanie stężeń
- 15. Скачать презентацию
Слайд 2Ważne! Podczas rozwiązywania zadań, w których mamy do czynienia ze zmianą stężenia,
Ważne! Podczas rozwiązywania zadań, w których mamy do czynienia ze zmianą stężenia,

Do już istniejących gotowych roztworów bardzo często dodajemy wody. Rozcieńczamy preparat kosmetyczny, np. w celu lepszej aplikacji na skórę – możemy m.in. Sporządzić roztwór z esencji do przemywania skóry.
Otrzymany roztwór ma nowe stężenie, przy obliczaniu którego należy uwzględnić to, że posługujemy się mieszaniną: czystą substancją zmieszaną z rozpuszczalnikiem.
Слайд 8W celu obliczenia proporcji, w jakich należy zmieszać roztwór bardziej stężony w
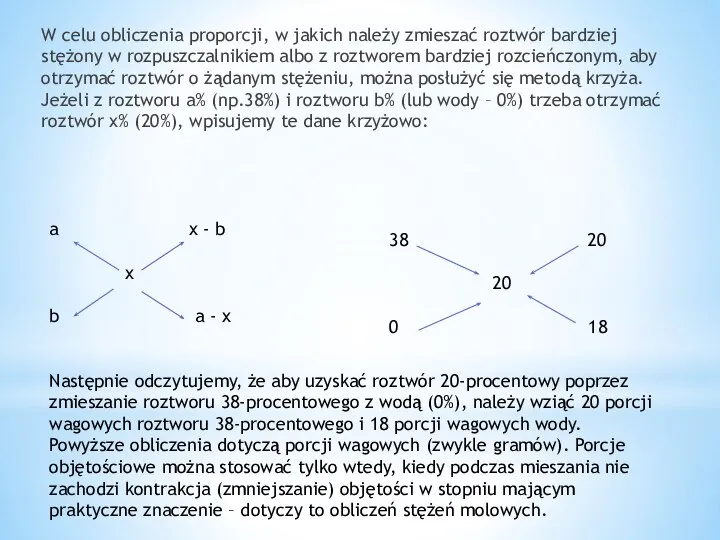
W celu obliczenia proporcji, w jakich należy zmieszać roztwór bardziej stężony w
a x - b
x
b a - x
38 20
20
0 18
Następnie odczytujemy, że aby uzyskać roztwór 20-procentowy poprzez zmieszanie roztworu 38-procentowego z wodą (0%), należy wziąć 20 porcji wagowych roztworu 38-procentowego i 18 porcji wagowych wody. Powyższe obliczenia dotyczą porcji wagowych (zwykle gramów). Porcje objętościowe można stosować tylko wtedy, kiedy podczas mieszania nie zachodzi kontrakcja (zmniejszanie) objętości w stopniu mającym praktyczne znaczenie – dotyczy to obliczeń stężeń molowych.
Слайд 9Przykład 3
Ile gramów wody należy dodać do 20g 30% roztworu KOH,
Przykład 3
Ile gramów wody należy dodać do 20g 30% roztworu KOH,

Obliczenia:
Posługując się krzyżową regułą mieszania, widzimy, że trzeba zmieszać:
roztwór 30% 12 części masowych 30% roztworu
roztwór 12%
roztwór 0% 18 części masowych wody
z z proporcji:
Na 12g roztworu KOH potrzeba 18 g wody
Na 20g roztworu KOH potrzeba X g wody
Слайд 11Przeliczanie stężeń
Przeliczanie stężeń









 Металлы в природе. Общие способы их получения
Металлы в природе. Общие способы их получения Классификация органических соединений
Классификация органических соединений Степень окисления в соединениях
Степень окисления в соединениях Углеводороды
Углеводороды Periodická soustava prvků
Periodická soustava prvků Выход продуктов пиролиза бензина
Выход продуктов пиролиза бензина Исследование концентрированных заквасок для сметаны
Исследование концентрированных заквасок для сметаны Осмотическое давление
Осмотическое давление Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Составление формул оксидов, оснований, солей
Составление формул оксидов, оснований, солей Алкены. Этилен C2H4
Алкены. Этилен C2H4 Метил-трет-бутиловый эфир
Метил-трет-бутиловый эфир Элемент магний
Элемент магний Ovr-1
Ovr-1 Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы
Предельные углеводороды. Алканы, насыщенные углеводороды, парафины, циклоалканы 10_Valentnost_khimicheskikh_elementov
10_Valentnost_khimicheskikh_elementov Применение центрифугирования
Применение центрифугирования Жиры. Классификация жиров
Жиры. Классификация жиров Презентация на тему Металлы в периодической системе
Презентация на тему Металлы в периодической системе  Валентность
Валентность Строение веществ
Строение веществ Углеводороды. 9 класс
Углеводороды. 9 класс Ароматические углеводороды
Ароматические углеводороды Химическая связь. Лекция №3
Химическая связь. Лекция №3 Метод молекулярных орбиталей для координационных соединений
Метод молекулярных орбиталей для координационных соединений 10-2 основные положения теории Бутлерова
10-2 основные положения теории Бутлерова Общая характеристика элементов А-группы
Общая характеристика элементов А-группы Путешествие по городу химиков
Путешествие по городу химиков