Содержание
- 2. Окислительно – восстановительные реакции … – реакции, протекающие с изменением степени окисления элементов.
- 3. Два антипода парою ходят, Первый – теряет; второй - находит, Ролью меняясь при этом порой… Кто
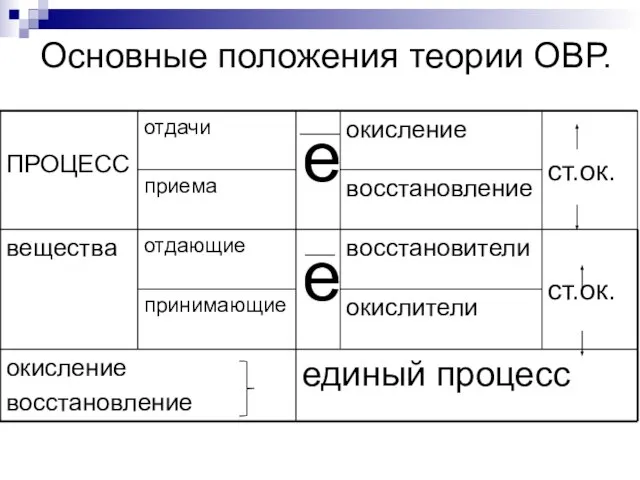
- 4. Основные положения теории ОВР.
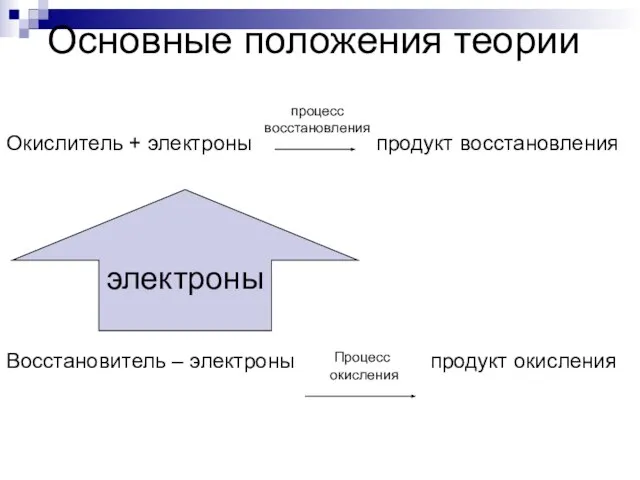
- 5. Окислитель + электроны продукт восстановления Восстановитель – электроны продукт окисления процесс восстановления электроны Процесс окисления Основные
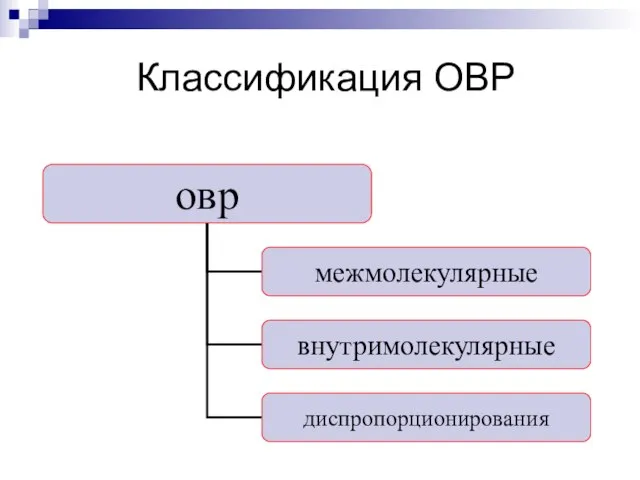
- 6. Классификация ОВР
- 7. Алгоритм составления ОВР Определить степени окисления элементов в соединениях, участвующих в реакции. Выявить элемент, степень окисления
- 8. Число отданных и принятых электронов должно быть одинаковым. Если это не так, то составить электронный баланс:
- 9. Алгоритм определения степеней окисления
- 10. Восстановитель Калий Галлий
- 11. Э Э n+ Атомы металлов (I и II гр., Al, Fe, Zn…). Отрицательно заряженные ионы неметаллов
- 12. Азот Фтор Окислитель
- 13. Окислитель Э Э n- Атомы элементов VI–VII групп (О2, Сl2…). Ионы металлов в высоких степенях окисления
- 14. Степень окисления – Условный заряд атомов химического элемента в соединении, вычисленный на основе предположения, что все
- 16. Сера (-2,0,+2,+4,+6) Железо ( +2, +3)
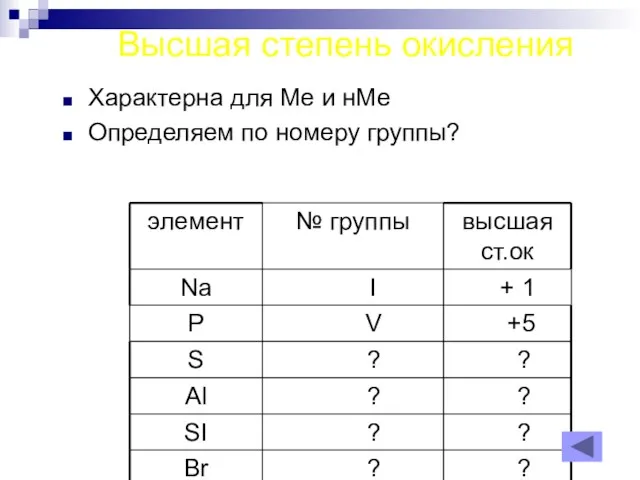
- 17. Высшая степень окисления Характерна для Ме и нМе Определяем по номеру группы?
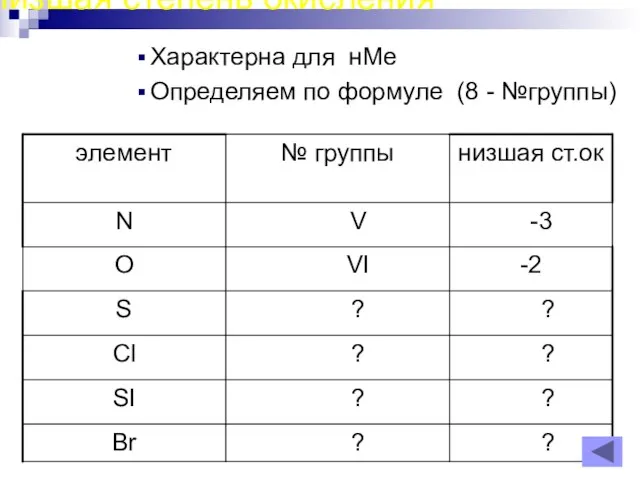
- 18. Низшая степень окисления Характерна для нМе Определяем по формуле (8 - №группы)
- 19. Нулевая ( 0) Все простые вещества Бром Литий Йод
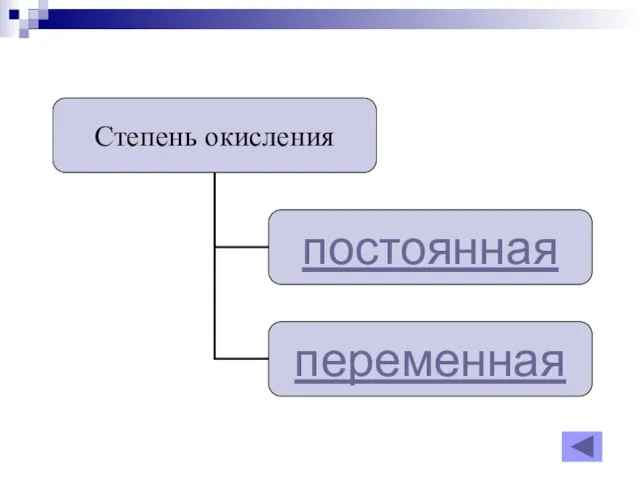
- 20. постоянная
- 21. Тест для 8 класса Тема: «Окислительно – восстановительные реакции»
- 22. Инструкция по выполнению теста Внимательно прочитайте задание и выберите правильный ответ – нажмите справа на нужную
- 23. Степень окисления серы K2SO3 в равна +3 +2 +6 +4
- 24. Окислительно - восстановительная реакция CaO+Co2=CaCO3 NaOH+HCl=NaHCl+H2O Fe+CuSO4=FeSO4+Cu Na3SiO3+2HCl=2NaCl+H2SiO3
- 25. Окислитель Принимает электроны Окисляется Отдаёт электроны Не изменяет степень окисления
- 26. Магний имеет минимальное значение степени окисления +2 -2 0 +1
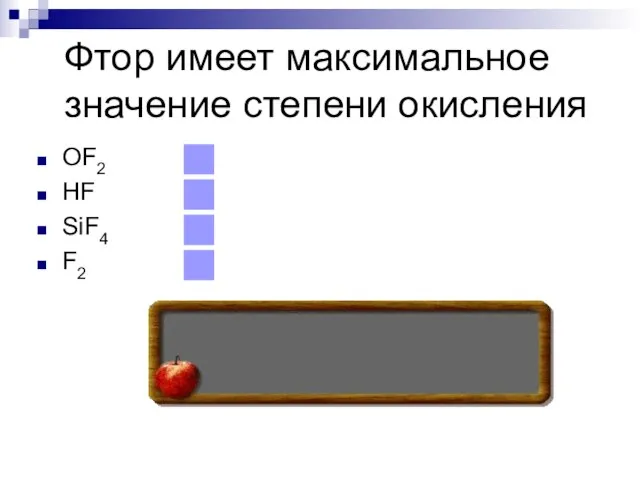
- 27. Фтор имеет максимальное значение степени окисления OF2 HF SiF4 F2
- 28. Конец тестирования Молодец! Справились верно с 5 заданиями Отличная работа!
- 29. Вы ответили неправильно! Прочитайте параграф 43 ещё раз. Выполните тестовое задание снова. Закончить тестирование! Вернуться на
- 31. Скачать презентацию





















 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества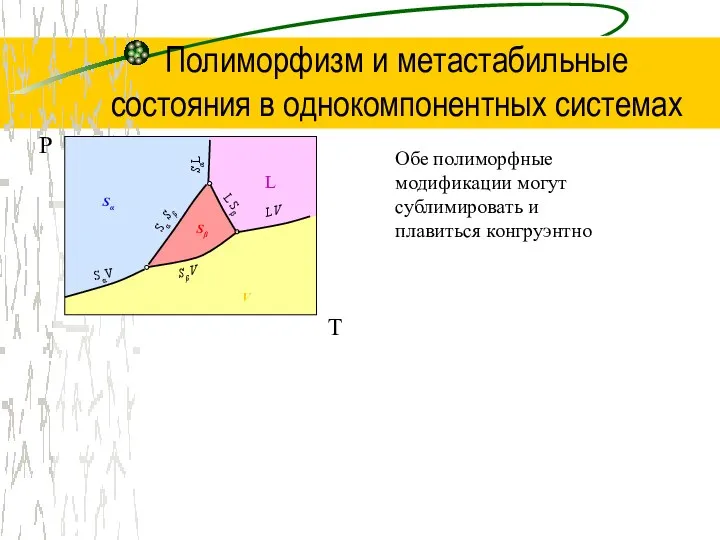 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі