Слайд 2ЛЕКЦИЯ №7
ДИСПЕРСНЫЕ СИСТЕМЫ
ОП. 05 Химия
1 курс 1 семестр
Составитель: преподаватель
Кобзева Марина

Валерьевна
Ставрополь, 2020г
Слайд 3 Дисперсная система — это система, образованная из двух или более фаз (тел),

которые совершенно или практически не смешиваются и не реагируют друг с другом химически.
Первое из веществ (дисперсная фаза) мелко распределено во втором (дисперсионная среда). Если фаз несколько, их можно отделить друг от друга физическим способом (центрифугировать, сепарировать и т. д.).
Обычно дисперсные системы — это коллоидные растворы, золи.
Слайд 4Основные типы дисперсных систем.
По дисперсности, т. е. размеру частиц дисперсной фазы

или отношению общей площади межфазной поверхности к объему (или массе) дисперсной фазы (удельная поверхности). Дисперсные системы условно делят на грубодисперсные и тонкодисперсные (коллоидные системы).
Слайд 5 От степени дисперсности зависят свойства дисперсных систем, в частности их устойчивость. Грубодисперсные

системы являются неустойчивыми и со временем разделяются на дисперсную фазу и дисперсную среду. Коллоиднодисперсные системы значительно более устойчивы.
В природе и технике часто встречаются дисперсные системы, в которых одно вещество равномерно распределено в виде частиц внутри другого вещества
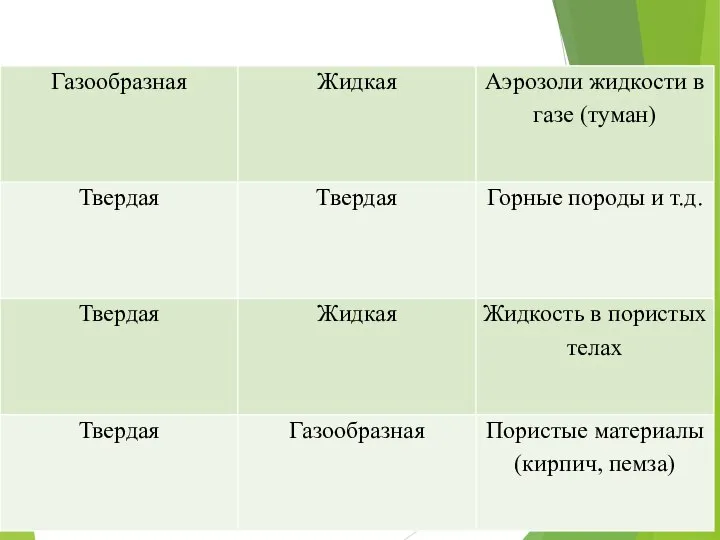
Слайд 6В зависимости от агрегатного состояния дисперсионной среды и дисперсной фазы выделяют основные

виды дисперсных систем
Слайд 8КОЛЛОИДНЫЕ СИСТЕМЫ
Коллоидные растворы - это высокодисперсные двухфазные системы, состоящие из дисперсионной среды

и дисперсной фазы, причем линейные размеры частиц последней лежат в пределах от 1 до 100 нм.
Как видно, коллоидные растворы по размерам частиц являются промежуточными между истинными растворами и суспензиями и эмульсиями.
Коллоидные частицы обычно состоят из большого числа молекул или ионов. Коллоидные частицы называют мицеллами.
Слайд 9 Строение мицеллы рассмотрим на примере образования коллоидного раствора йодида серебра, получаемого при

взаимодействии очень разбавленных растворов нитрата серебра и йодида калия:
AgNO3+KI = AgI↓+KNO3
Ag++No3- +K++I-=AgI↓+K++NO3-
Слайд 10 Нерастворимые молекулы йодида серебра образуют ядро коллоидной частицы. Вещество ядра, имеющее кристаллическую

или аморфную структуру, нерастворимо в дисперсионной среде и состоит из нескольких тысяч нейтральных молекул или атомов.
Полученное ядро адсорбирует на своей поверхности те или иные ионы, имеющиеся в растворе. Если коллоидный раствор получают при избытке йодида калия, то адсорбируются ионы йода.
Они достраивают кристаллическую решетку ядра, прочно входят в его структуру, образуя адсорбционный слой, и придают ядру отрицательный заряд.
Слайд 11 Коллоидные растворы иначе называют золями. Их получают дисперсионными и кондесационными методами.
Диспергирование

чаще всего производят при помощи особых «коллоидных мельниц».
При конденсационном методе коллоидные частицы образуются за счет объединения атомов или молекул в агрегаты.
При протекании многих химических реакций происходит конденсация и образуются высокодисперсные системы (выпадение осадков, протекание гидролиза, окислительно-восстановительные реакции и т.д.).
1 нм - нанометр (1 нм = 10-9 м).
Слайд 12 В отличие от истинных растворов для золей характерен эффект Тиндаля, т. е.

рассеяние света коллоидными частицами.
При пропускании через золь пучка света появляется светлый конус, видимый в затемненном помещении .
Так можно распознать, является данный раствор коллоидным или истинным.
Слайд 13 Одним из важных свойств золей является то, что их частицы имеют электрические

заряды одного знака.
Благодаря этому они не соединяются в более крупные частицы и не осаждаются. При этом частицы одних золей, например металлов, сульфидов, кремниевой и оловянной кислот, имеют отрицательный заряд, других, например гидроксидов, оксидов металлов, — положительный заряд.
Возникновение заряда объясняется адсорбцией коллоидными частицами ионов из раствора
Слайд 14 Для осаждения золя необходимо, чтобы его частицы соединились в более крупные агрегаты.

Соединение частиц в более крупные агрегаты называется коагуляцией, а осаждение их под влиянием силы тяжести - седиментацией.
Обычно коагуляция происходит при прибавлении к золю: 1) электролита, 2) другого золя, частицы которого имеют противоположный заряд, и 3) при нагревании
Слайд 15 Примером сложной дисперсионной системы является молоко, основные составные части которого – вода,

жир, козеин и молочный сахар.
Жир находится в виде эмульсии и при стоянии молока постепенно поднимается к верху (сливки).
Козеин (белок) содержится в виде раствора, похожего по свойствам на коллоидный, и самопроизвольно не выделяется, но легко может быть осажден (в виде творога) при подкислении молока, например, уксусом.
Слайд 16 В естественных условиях выделение козеина происходит при скисании молока. Молочный сахар находится

в виде молекулярного раствора и выделяется лишь при испарении воды.
Коллоидные растворы широко применяются в различных технологических процессах: мыловаренной, бумажной, текстильной промышленности и т.д.
Коллодиные растворы играют большую роль в жизнедеятельности организмов. Протоплазма живых клеток, кровь, сок растений – это коллоидные растворы (золи).














 Атом
Атом Презентация 1
Презентация 1 Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву
Виды нагрева и материалы резистивных нагревателей, их стойкость к температуре, ростовой атмосфере и расплаву Получение аминов
Получение аминов Расчеты по уравнениям химических реакций
Расчеты по уравнениям химических реакций Оксиды, их классификация и химические свойства. 8 класс
Оксиды, их классификация и химические свойства. 8 класс Строение вещества
Строение вещества Виды химической связи. Обобщение и систематизация знаний
Виды химической связи. Обобщение и систематизация знаний Химические реакции
Химические реакции Морфологогия минералов
Морфологогия минералов Природа и типы химических связей
Природа и типы химических связей Презентация на тему Вещества и их свойства
Презентация на тему Вещества и их свойства  ВКР: Определение показателей качества мясной и колбасной продукции различных производителей
ВКР: Определение показателей качества мясной и колбасной продукции различных производителей Презентация на тему Физические и химические явления 8 класс
Презентация на тему Физические и химические явления 8 класс  Изомерия. Виды изомерии
Изомерия. Виды изомерии Презентация на тему Халькогены
Презентация на тему Халькогены  Азотная кислота
Азотная кислота Метелёва И.Е. учитель химии
Метелёва И.Е. учитель химии Решение заданий ОГЭ по химии (1 - 15)
Решение заданий ОГЭ по химии (1 - 15) Химия и производство
Химия и производство Алканы
Алканы Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы
Анализ воды природных источников посёлков Фруктовая и Красная Пойма городского округа Луховицы Салициловая кислота
Салициловая кислота Масляная кислота
Масляная кислота Кумарон - индендық полимерлер
Кумарон - индендық полимерлер Классификация химических реакций
Классификация химических реакций Нефть
Нефть Водородная химическая связь
Водородная химическая связь