Содержание
- 2. Экстракция Экстракция – это сложный физико-химический процесс извлечения металлов из водных растворов протекающий в многокомпонентных двухфазных
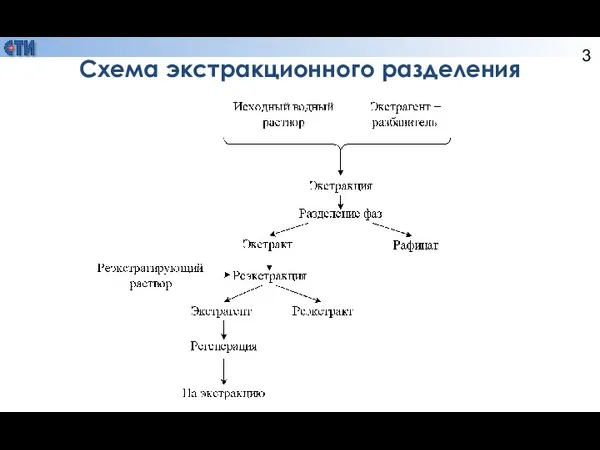
- 3. Схема экстракционного разделения
- 4. Экстрагенты – органические жидкости, способные растворять в себе ионы металлов с образованием прочных комплексных соединений. Разбавители
- 5. Требования к экстрагентам достаточно высокий коэффициент распределения экстрагируемого вещества; селективность по отношению к экстрагируемому веществу; малая
- 6. В условиях фазового равновесия действует правило фаз Гиббса, устанавливающее соотношение между числом степеней свободы F, числом
- 7. Классификация экстрагентов и механизмы экстракции Известно три класса экстрагентов: Нейтральные фосфорорганические экстрагенты (спирты, эфиры, альдегиды, кетоны);
- 8. Фосфорорганические экстрагенты
- 9. Механизмы экстракции различными классами экстрагентов 1) экстракция нейтральными экстрагентами Ln3+ + 3NO3- + 3ТБФ = Ln(NO3)3·3ТБФ
- 10. Для нейтральных фосфорорганических соединений характерно наличие высокого дипольного момента молекул. Значительная электроотрицательность фосфорильного атома кислорода объясняет
- 11. Механизмы экстракции различными классами экстрагентов 2) экстракция кислыми алкилфосфатами идет с образованием очень прочного, хорошо растворимого
- 12. 3) экстракция аминами осуществляется по механизму анионного обмена. Соли ЧАО обладают наибольшей селективностью. В нитратных растворах
- 13. Экстракция аминами протекает в течение нескольких секунд и только тогда, когда водная фаза содержит ионы Н+.
- 14. Равновесие экстракции 1) Экстракция нейтральными экстрагентами Константа равновесия:
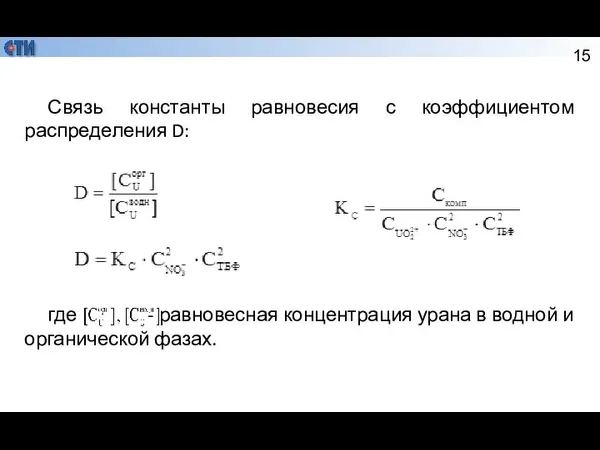
- 15. Связь константы равновесия с коэффициентом распределения D: где - равновесная концентрация урана в водной и органической
- 16. Так как процесс экзотермический, то повышение температуры будет смещать равновесие в сторону исходных веществ и ухудшать
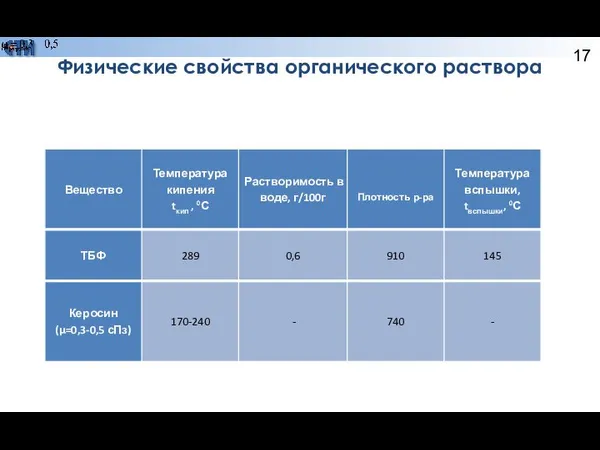
- 17. Физические свойства органического раствора
- 18. Факторы, влияющие на равновесие экстракции аминами Константа равновесия: Коэффициент распределения:
- 19. Факторы, влияющие на равновесие экстракции аминами: 1) константа равновесия – термодинамическая константа, которая отвечает за влияние
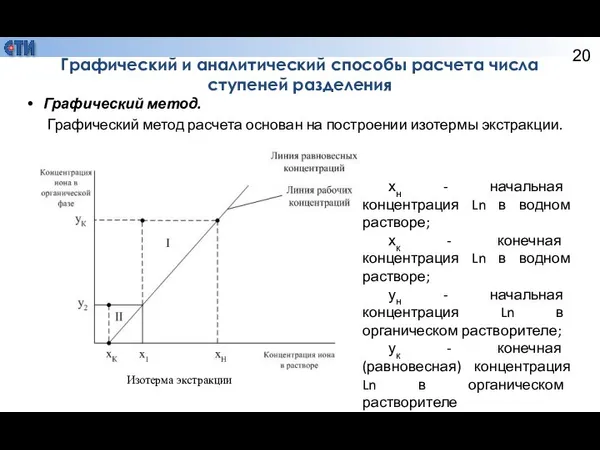
- 20. Графический и аналитический способы расчета числа ступеней разделения Графический метод. Графический метод расчета основан на построении
- 21. Теоретическая ступень – это один акт взаимодействия водной и органической фаз с протеканием химической реакции, в
- 22. Аналитический метод. Если коэффициент распределения величина постоянная, то число теоретических ступеней рассчитывают из уравнения:
- 23. Зная величину коэффициента распределения D и соотношение объемов фаз, найденное из материального баланса процесса, определяют величину
- 24. Кинетика экстракции Процесс экстракционного разделения осуществляется в две стадии: 1) стадия эмульгирования; 2) стадия расслаивания.
- 25. В общем случае скорость процесса зависит от: - градиента концентраций; - температуры; - вязкости водной и
- 26. Расслаивание. Скорость расслаивания тем выше: - чем больше разница плотностей водной и органической фазы, а это
- 27. Переработка лопаритового концентрата Р-р хлоридов после очистки от Th, U и Ra поступает на противоточный экстракционный
- 28. Для нейтрализации HCl используют Na2CO3 Осадок Ce(OH)4 + MnO2 растворяют в HCl и осаждают оксалат церия.
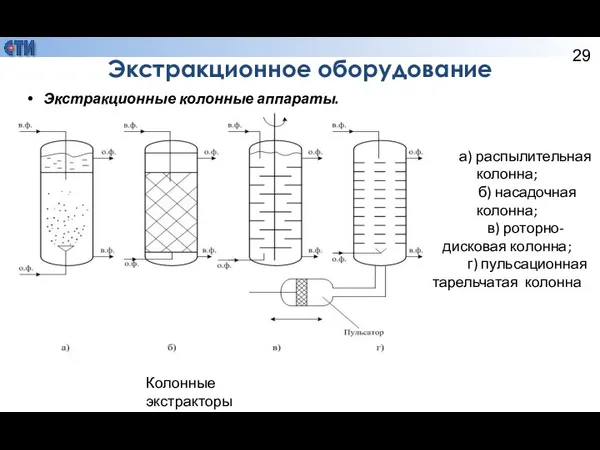
- 29. Экстракционное оборудование Экстракционные колонные аппараты. а) распылительная колонна; б) насадочная колонна; в) роторно-дисковая колонна; г) пульсационная
- 31. Скачать презентацию























 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию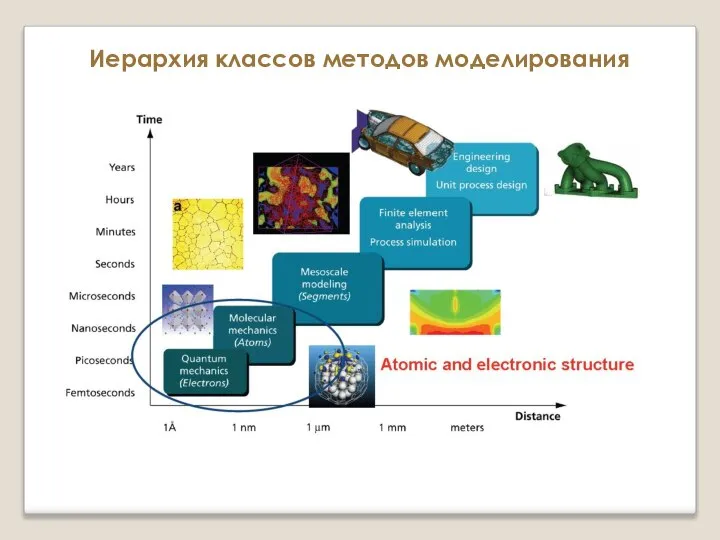 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій