Слайд 2Задание 1
Для выполнения задания используйте следующий перечень веществ: перманганат калия, гидрокарбонат

калия, сульфит натрия, сульфат бария, гидроксид калия. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции с участием выбранных веществ.
Слайд 3Решение
Для начала запишем молекулярные формулы данных веществ: KMnO4, KHCO3, NaSO3, BaSO4, KOH.
Сульфат бария является

нерастворимой солью, поэтому не будет вступать в реакцию с приведенными веществами.
Перманганат калия не вступает в РИО с гидрокарбонатом калия и гидроксидом калия, так как имеют одинаковый катион.
Слайд 4С сульфитом натрия реакция невозможна, так как образуются растворимые соли.
Гидрокарбонат калия и гидроксид

калия тоже имеют общий ион, но реакция между ними возможна с образованием средней соли карбоната калия и будет относиться к РИО.
С сульфитом натрия реакция невозможна, так как образуются растворимые соли.
Сульфит натрия не реагирует с гидроксидом калия по причине образования в ходе реакции растворимых веществ.
Слайд 5Таким образом, вариант ответа только один:
KHCO3+КОН= K2CO3+ Н2O
K+ +HCO3- + K+ +

ОН- = 2K+ + CO32- + Н2O
HCO3- + ОН- = CO32- + Н2O
Слайд 6Задание 2
Для выполнения задания используйте следующий перечень веществ: хлороводород, нитрат серебра(I),

перманганат калия, вода, азотная кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена, приводящая к образованию осадка. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции с участием выбранных веществ.
Слайд 7Решение
Запишем молекулярные формулы данных веществ: HCl, AgNO3, KMnO4, Н2O, HNO3.
Соляная кислота и

азотная кислота между собой не реагируют.
Перманганат калия не с одним из веществ не реагирует, так как нет восстановителей.
Слайд 8Таким образом, вариант ответа только один:
HCl+ AgNO3=AgCl↓+ HNO3
H+ +Cl-+ Ag++NO3- =AgCl↓+ H+

+ NO3-
Ag++NO3- =AgCl↓
Слайд 9Задание 3
Для выполнения задания используйте следующий перечень веществ: серная кислота, сероводород,

карбонат натрия, вода, марганцовая кислота. Допустимо использование водных растворов веществ.
Из предложенного перечня веществ выберите вещества, между которыми возможна реакция ионного обмена, не приводящая к выделению газа. Запишите молекулярное, полное и сокращённое ионное уравнения этой реакции с участием выбранных веществ.
Слайд 10Решение
Для начала запишем молекулярные формулы данных веществ: H2SO4, H2S, Na2CO3, Н2O, HMnO4.
Серная кислота растворимая кислота,

вступает в реакцию с растворимой солью карбоната натрия (в эквивалентных количествах образуется сульфат натрия, в избытке кислоты гидросульфат) с образованием углекислого газа и воды. Не вступает в РИО с кислотами: сероводородом и марганцевой кислотой.
Слайд 11Сероводородная кислота — растворимая кислота, вступает в реакцию с растворимой солью карбоната натрия

(образуется гидросульфид, так как кислота слабая и полностью не диссоциирует) с образованием углекислого газа и воды. Не вступает в РИО с кислотами: серной и марганцевой кислотой.
Марганцовая кислота — растворимая кислота, вступает в реакцию с растворимой солью карбоната натрия с образованием углекислого газа и воды. Не вступает в РИО с кислотами.










 Общая характеристика неметаллов
Общая характеристика неметаллов Изомерия. Классификация органических веществ.
Изомерия. Классификация органических веществ. Химия спирты одноатомные предельные
Химия спирты одноатомные предельные Композитные материалы
Композитные материалы Демокрит его вклад в развитие взглядов на строение вещества
Демокрит его вклад в развитие взглядов на строение вещества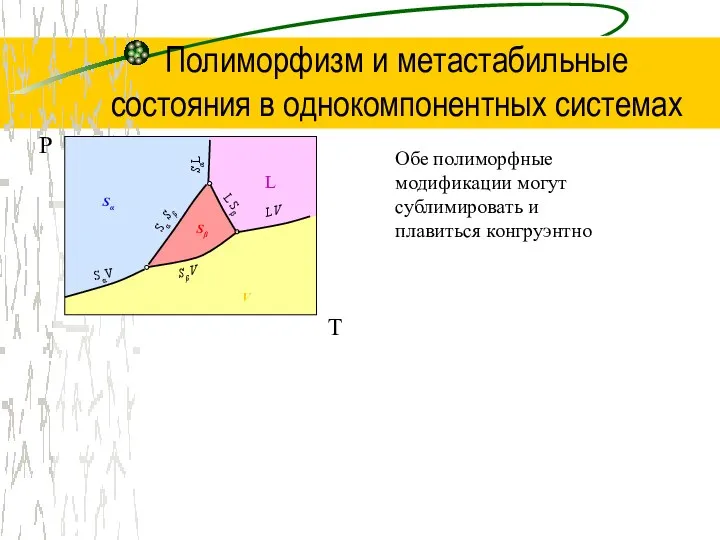 Полиморфизм и метастабильные состояния в однокомпонентных системах
Полиморфизм и метастабильные состояния в однокомпонентных системах Основи масообміну
Основи масообміну Количество вещества. Моль
Количество вещества. Моль Алюміній. Фізичні та хімічні властивості
Алюміній. Фізичні та хімічні властивості Хроматография
Хроматография Углеродистые конструкционные стали
Углеродистые конструкционные стали Жидкокристаллический эластомер как роторный актуатор
Жидкокристаллический эластомер как роторный актуатор Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Свойства растворов электролитов
Свойства растворов электролитов Производство аммиака
Производство аммиака Кислород. Общая характеристика, получение и свойства
Кислород. Общая характеристика, получение и свойства Презентация на тему Металлы
Презентация на тему Металлы  Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи
Количество вещества, число Авогадро, молярная масса, молярный объём, уравнение связи Алкены
Алкены Презентация на тему Электронное и пространственное строение молекулы метана
Презентация на тему Электронное и пространственное строение молекулы метана  Циклоалканы. Физические свойства
Циклоалканы. Физические свойства Кислород
Кислород Синтетические органические соединения
Синтетические органические соединения Турнир Деда Мороза. Викторина по химии
Турнир Деда Мороза. Викторина по химии Презентация на тему Алмазы Индии
Презентация на тему Алмазы Индии  Алкены
Алкены Значимые личности в химии
Значимые личности в химии Стан електронів у атомі
Стан електронів у атомі