Содержание
- 2. Щелочные металлы – элементы IA группы Перечислите известные вам щелочные металлы. Сколько электронов на внешнем энергетическом
- 3. Из истории открытия элементов 19 ноября 1907 года в Лондоне на заседании Королевского химического общества сэр
- 5. 3 января 1959 года В небе появилась комета. Необычная комета – искусственная: из летящей к Луне
- 6. Физические свойства Какое строение характерно для кристаллов щелочных металлов? Как изменяются температуры кипения и плавления? Какой
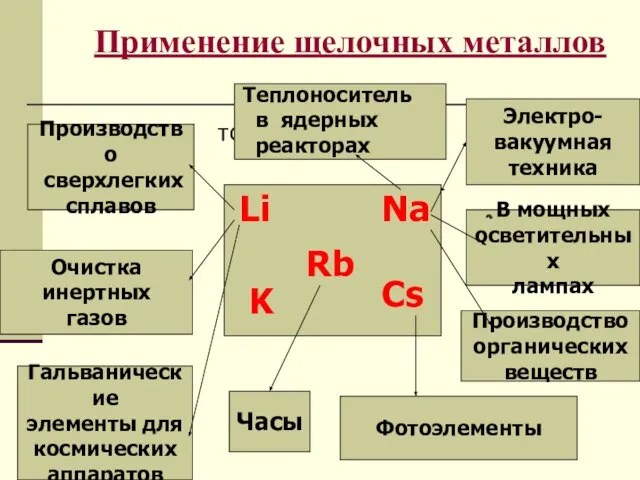
- 7. Применение щелочных металлов тото Электро- вакуумная техника В мощных осветительных лампах Производство органических веществ Производство сверхлегких
- 8. Соединения щелочных металлов В ветхом завете упоминается некое вещество «нетер». Это вещество употребляли как моющее средство.
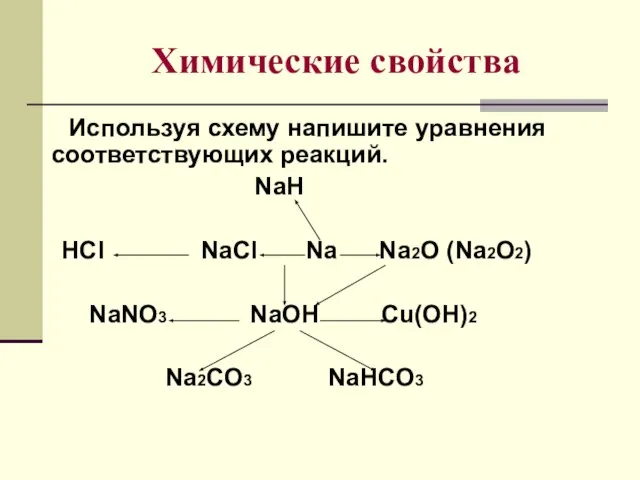
- 9. Химические свойства Используя схему напишите уравнения соответствующих реакций. NaH HCl NaCl Na Na2O (Na2O2) NaNO3 NaOH
- 10. Щелочноземельные металлы-элементы IIA группы Щелочноземельными являются не все элементы IIА группы, а только начиная с кальция
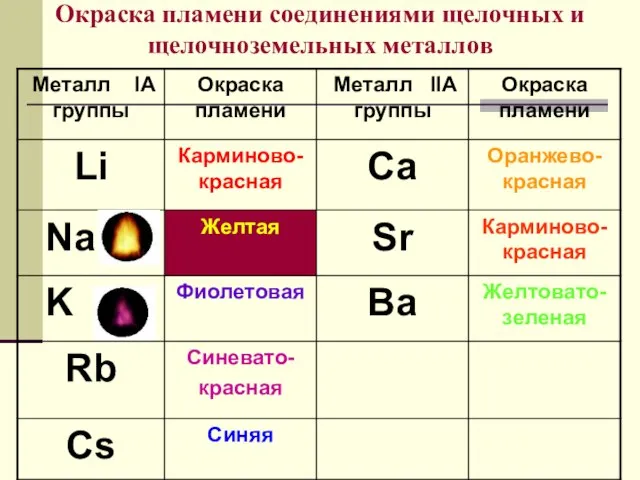
- 11. Окраска пламени соединениями щелочных и щелочноземельных металлов
- 12. Кальций –типичный представитель щелочноземельных металлов Дайте названия соединениям кальция: CaO Ca(OH)2 CaCO3 CaHCO3 Вспомните тривиальные названия
- 13. Жесткость воды
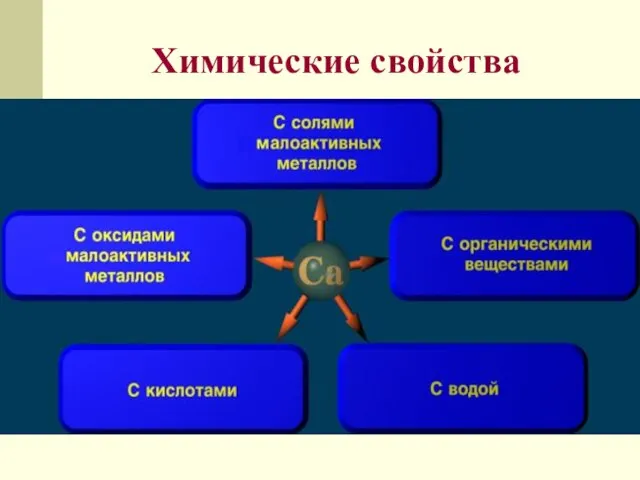
- 14. Химические свойства
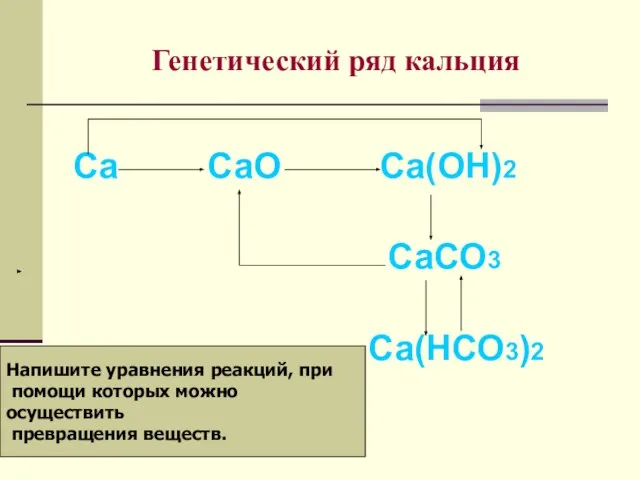
- 15. Генетический ряд кальция Са СаО Са(ОН)2 СаСО3 Са(НСО3)2 Напишите уравнения реакций, при помощи которых можно осуществить
- 16. Кальций в природе Кальциевые горные породы – известняк, мрамор, мел. Вспомните формулу этих горных пород. В
- 17. Мел, известняк, мрамор не растворяются в чистой воде, но растворимы в кислых растворах, даже таких слабых,
- 18. Как называются отложения, свисающие в виде гигантских сосулек со свода пещеры? А растущие навстречу им со
- 19. При воздействии кислотных дождей строения разрушаются. Какие реакции при этом происходят? Известняк и мрамор используют в
- 20. ? ? ? Каково значение щелочных и щелочно-земельных металлов в жизни человека? Как изменяются свойства оксидов
- 22. Скачать презентацию














 kisloty
kisloty Биохимия крови
Биохимия крови 596550
596550 Получение и применение алкадиенов
Получение и применение алкадиенов Молярный объем газов
Молярный объем газов Способы получения металлов
Способы получения металлов Спирт – это жизненная необходимость или страшное зло…
Спирт – это жизненная необходимость или страшное зло… Пространственная изомерия органических соединений
Пространственная изомерия органических соединений Подготовка проб товаров к анализу. Химико-аналитический контроль
Подготовка проб товаров к анализу. Химико-аналитический контроль Полистерол Прохоренко Е.О. 11 Б
Полистерол Прохоренко Е.О. 11 Б Оксид серы (VI) SO3
Оксид серы (VI) SO3 Физико-химические свойства нефтепродуктов
Физико-химические свойства нефтепродуктов Природные источники углеводородов
Природные источники углеводородов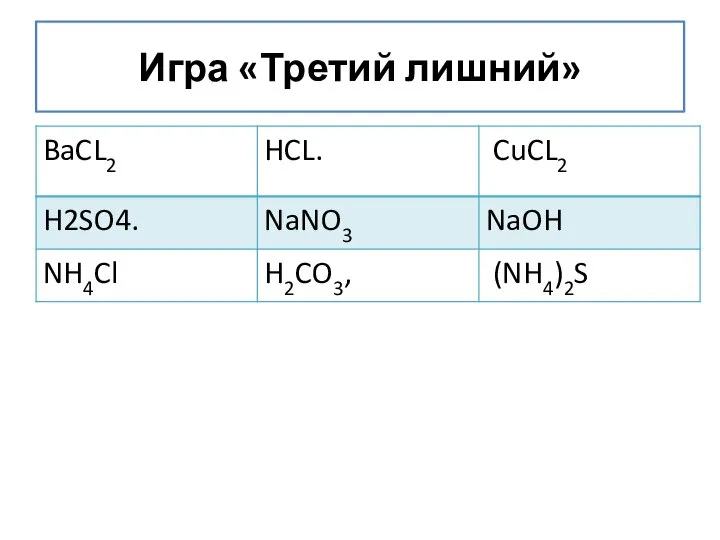 Аммиак. Соли аммония
Аммиак. Соли аммония Получение металлов
Получение металлов Стероиды. Дицетин-холестерин-ацилтрансферазная реакция
Стероиды. Дицетин-холестерин-ацилтрансферазная реакция Презентация на тему: Азотная кислота
Презентация на тему: Азотная кислота Техника безопасности на уроках химии
Техника безопасности на уроках химии Искусственные полимеры
Искусственные полимеры Хлорорганические соединения
Хлорорганические соединения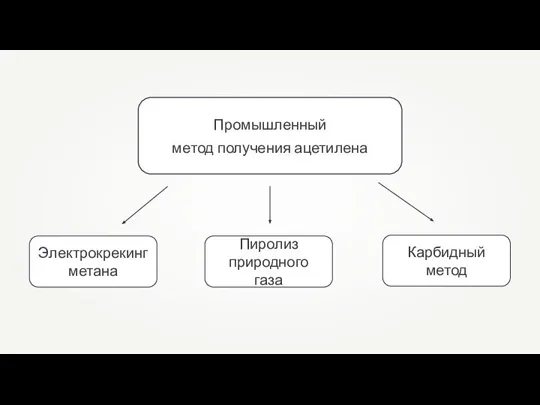 Промышленный метод получения ацетилена
Промышленный метод получения ацетилена Чистые вещества и смеси
Чистые вещества и смеси Дисперсные системы. Гели
Дисперсные системы. Гели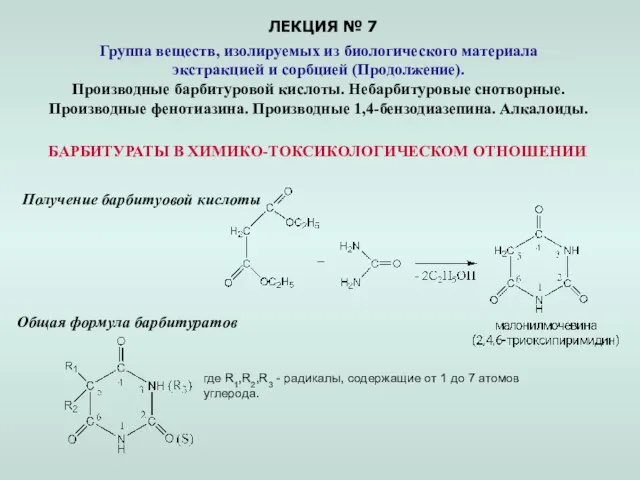 Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"
Презентация по Химии "Группа веществ, изолируемых из биологического материала экстракцией и сорбцией"  Химия и сельское хозяйство
Химия и сельское хозяйство Презентация на тему Скорость химических реакций
Презентация на тему Скорость химических реакций  Буферные системы
Буферные системы Окислительно-восстановительные реакции
Окислительно-восстановительные реакции