Содержание
- 2. Э А=Е Н=Л , О=И ,,, Я Ё=Е
- 3. Электролит
- 4. Цель урока Изучить процесс электролитической диссоциации, объяснить причины электролитической диссоциации.
- 5. Что такое электрический ток? Как называются вещества, которые проводят электрический ток? Приведите примеры. Почему металлы проводят
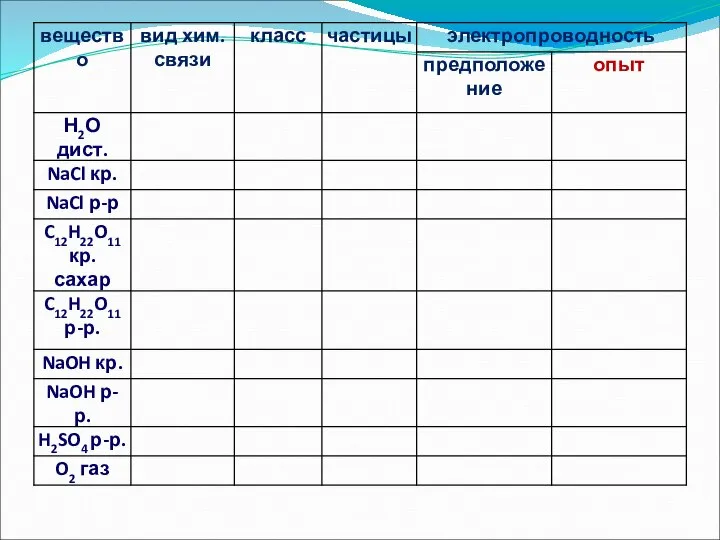
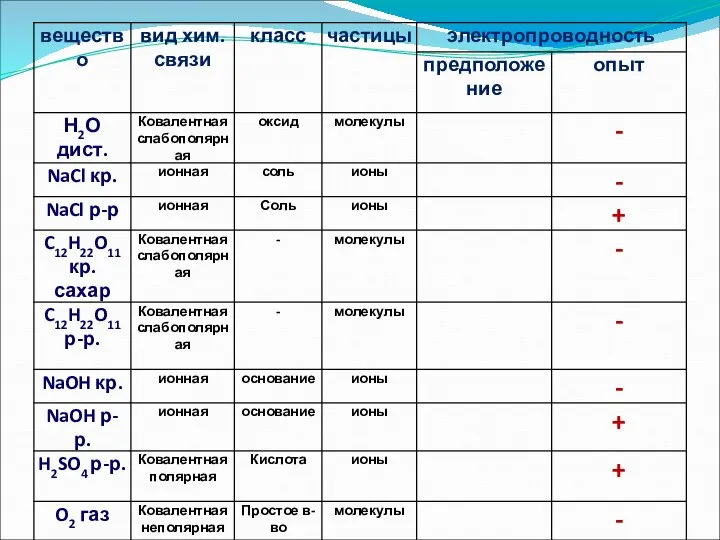
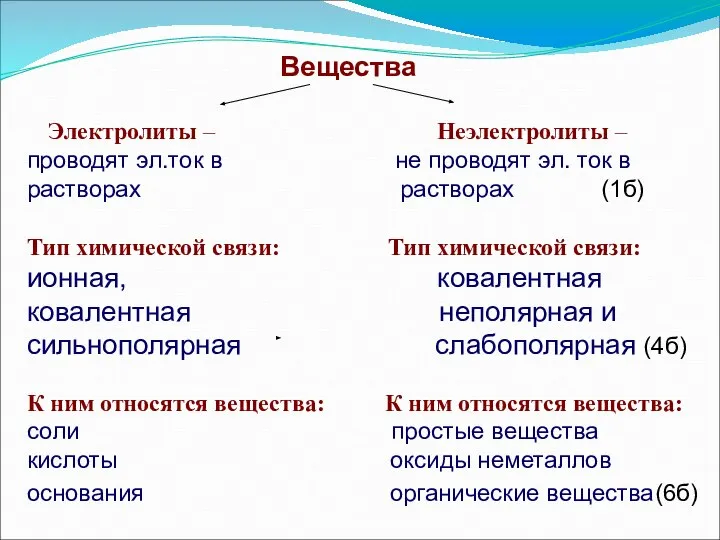
- 8. Вещества Электролиты – Неэлектролиты – проводят эл.ток в не проводят эл. ток в растворах растворах (1б)
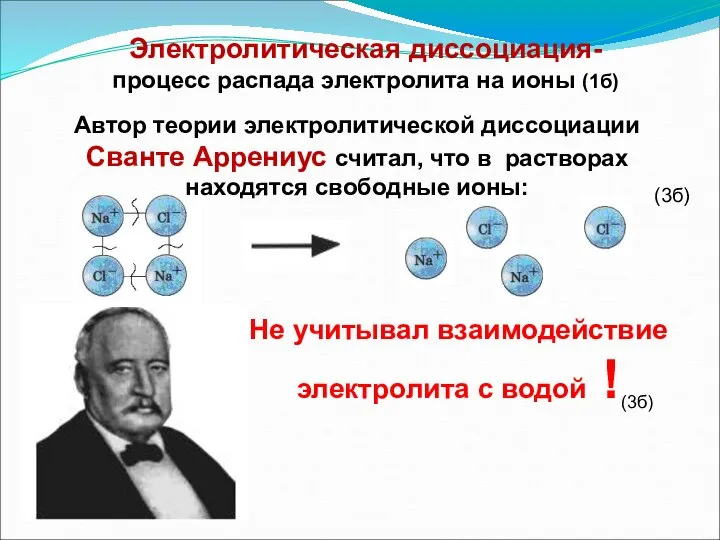
- 9. Автор теории электролитической диссоциации Сванте Аррениус считал, что в растворах находятся свободные ионы: Электролитическая диссоциация- процесс
- 10. Причину диссоциации объяснили И.А. Каблуков, В.А. Кистяковский ─ при растворении электролита происходит химическое взаимодействие растворенного вещества
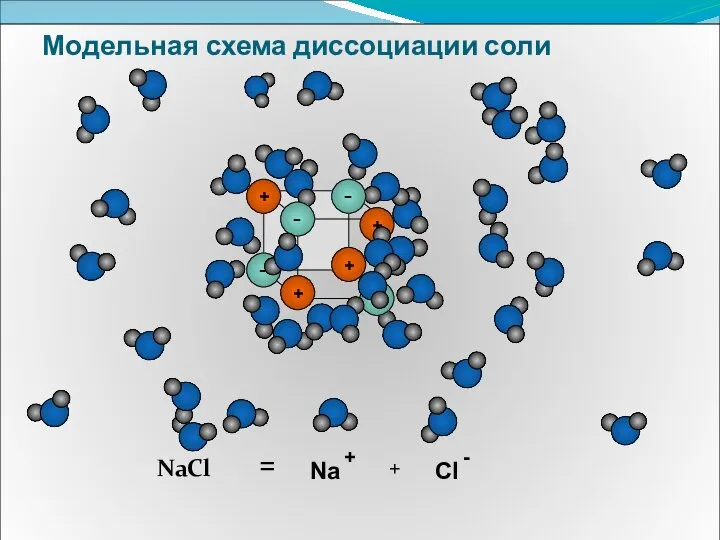
- 11. Модельная схема диссоциации соли NaCl = + Na +
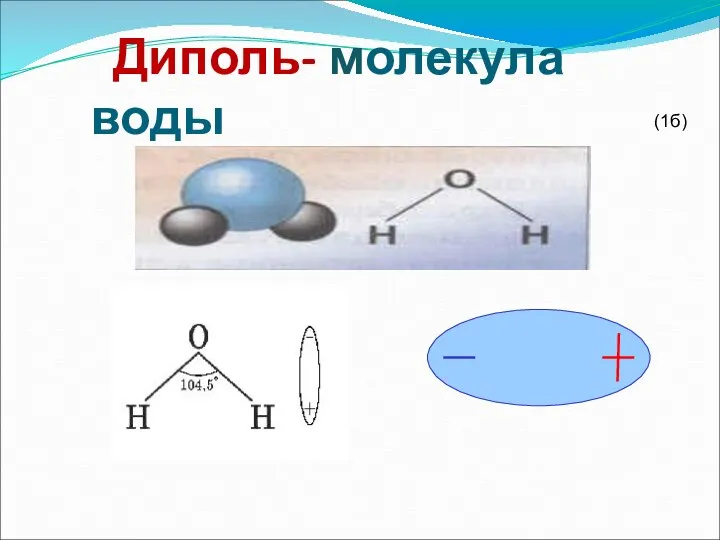
- 12. Диполь- молекула воды (1б)
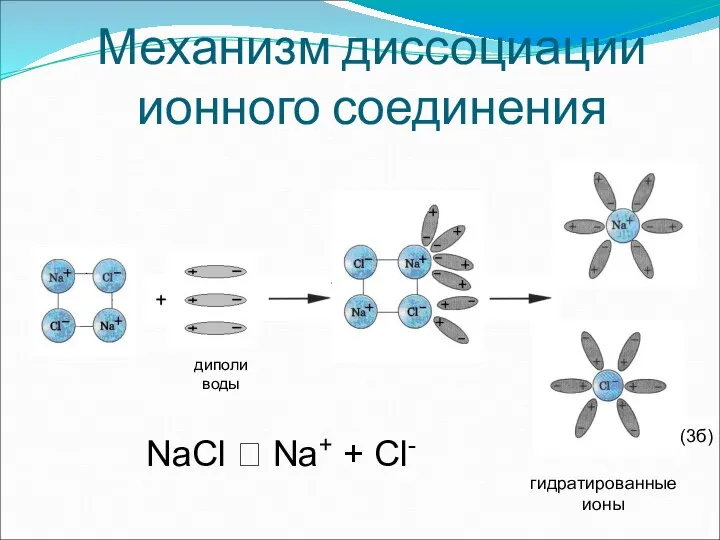
- 13. Механизм диссоциации ионного соединения NaCl ⮀ Na+ + Cl- гидратированные ионы диполи воды (3б)
- 14. Последовательность процессов, происходящих при диссоциации веществ с ионной связью: 1)ориентация молекул; 2)гидратация(взаимодействие); 3)диссоциация(распад) кристалла
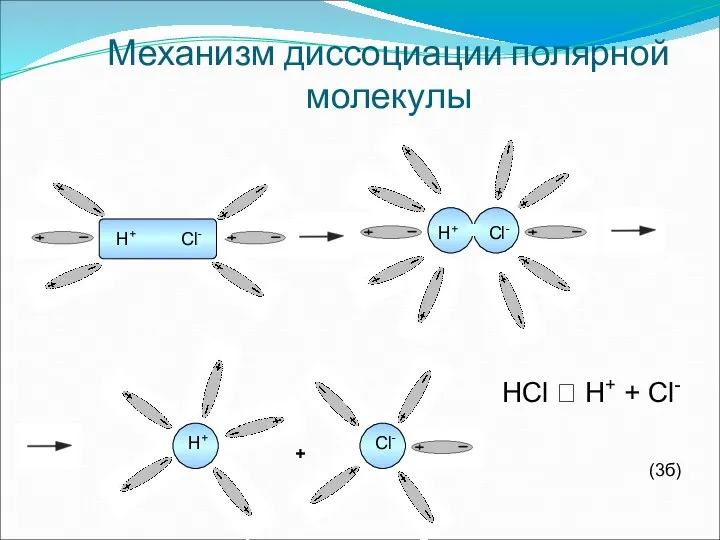
- 15. Механизм диссоциации полярной молекулы H+ Cl- H+ Cl- H+ Cl- + HCl ⮀ H+ + Cl-
- 16. Последовательность процессов, происходящих при диссоциации веществ с ковалентной полярной связью: 1)ориентация молекул; 2)гидратация(взаимодействие) молекул; 3)ионизация молекул(превращение
- 17. Степень диссоциации (α) (1б)
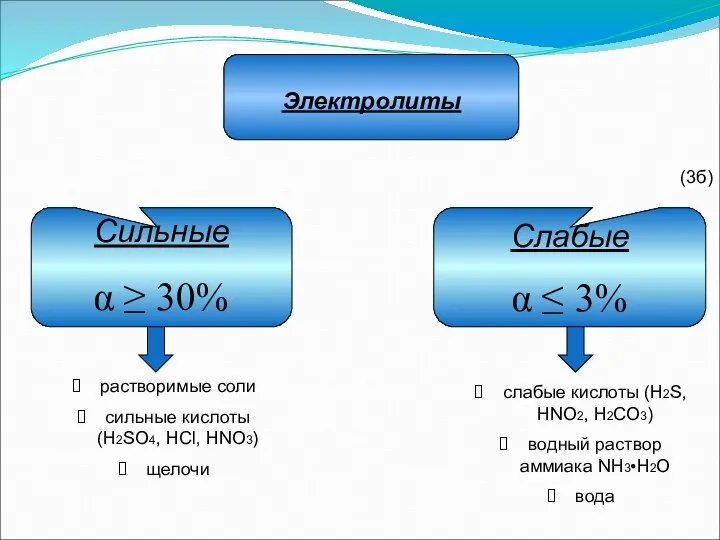
- 18. Сильные α ≥ 30% Слабые α ≤ 3% Электролиты растворимые соли сильные кислоты (H2SO4, HCl, HNO3)
- 21. Установите связь между электролитической диссоциацией и проблемами эксплуатации автомобиля Гололёд - Реагент - Коррозия
- 22. Объясните процесс приготовления пищи с точки зрения электролитической диссоциации
- 23. Задание для группы №1: Впишите недостающие слова: Все вещества по их способности проводить электрический ток в
- 24. Задание для группы №2;3: (2б за каждый правильный) всего12б Покажите выигрышный путь, состоящий из названий веществ
- 25. Задание для группы №4: Соотнесите: 1. (2б за каждый правильный) всего10б А) Электролиты 1) Кислоты Б)
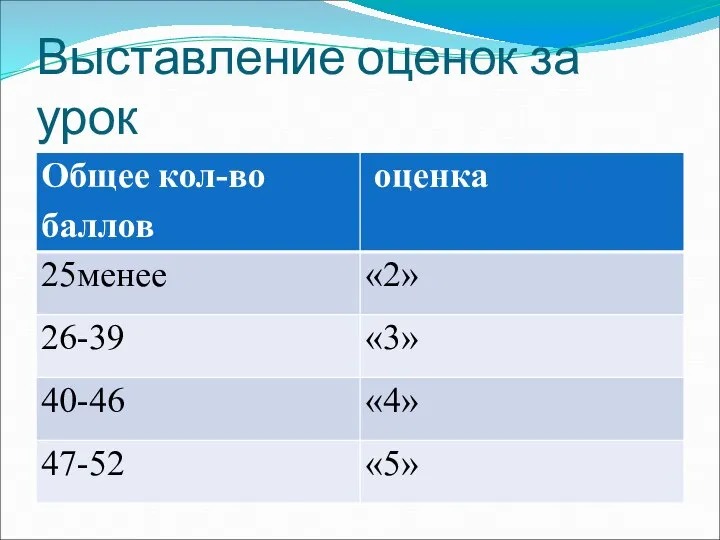
- 26. Выставление оценок за урок
- 27. РЕФЛЕКСИЯ Сегодня я узнал….. Было интересно…… Теперь я могу……… Я приобрел…… Я научился………
- 28. Домашнее задание: Читать Стр.193-197 до слов « В растворах электролитов..» упр.1,5 - «3»; упр.1,5,4 - «4»;
- 30. Скачать презентацию
















 Органическая химия. Теория строения органических веществ
Органическая химия. Теория строения органических веществ Искусственные полимеры
Искусственные полимеры Игра Самый умный химик
Игра Самый умный химик Создание учебно-методических материалов по химии в современной форме (презентации уроков)
Создание учебно-методических материалов по химии в современной форме (презентации уроков) Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических
Повторение по теме: « Химическая связь. Строение вещества». Виды химических связей Типы кристаллических Які існують способи розділення сумішей?
Які існують способи розділення сумішей? Подготовка к ЕГЭ
Подготовка к ЕГЭ Pастворы, используемые в промышленности
Pастворы, используемые в промышленности Хлорорганические соединения
Хлорорганические соединения Алкены. Непредельные углеводороды, олефины
Алкены. Непредельные углеводороды, олефины Карбоновые кислоты
Карбоновые кислоты Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Презентация на тему Углерод
Презентация на тему Углерод  Дисперсные системы и поверхностные явления
Дисперсные системы и поверхностные явления Галогены
Галогены Презентация на тему Метан и его свойства
Презентация на тему Метан и его свойства  Скорость химических реакций
Скорость химических реакций АРЕНЫ
АРЕНЫ Каучук
Каучук Реакции ионного обмена и условия их протекания
Реакции ионного обмена и условия их протекания Основные подходы к формированию и развитию социальных компетенций на уроках химии
Основные подходы к формированию и развитию социальных компетенций на уроках химии Растворение. Растворы. Урок в 8 классе
Растворение. Растворы. Урок в 8 классе Предельные углеводороды
Предельные углеводороды Углеродистые конструкционные стали
Углеродистые конструкционные стали Ароматические углеводороды. Арены
Ароматические углеводороды. Арены Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы
Поляризуемость. Эллипсоид поляризуемости и симметрия молекулы Многоатомные спирты
Многоатомные спирты Презентация на тему Важнейшие классы неорганических соединений
Презентация на тему Важнейшие классы неорганических соединений