Содержание
- 2. Окислительно-восстановительными называют реакции протекающие с изменением степеней окисления элементов, входящих в состав реагирующих веществ. Окислительно-восстановительные реакции
- 3. Окисление, с точки зрения элёктронной теории, — процесс отдачи электронов атомами, молекулами или ионами, например: При
- 4. Восстановление — процесс присоединения электронов атомами, молекулами или ионами: При восстановлении степень окисления элемента понижается.
- 5. Восстановитель — элемент, отдающий электроны (или вещество, содержащее такой элемент). Восстановитель в ходе реакции окисляется. Окислитель
- 6. Помните: Для данного элемента максимально возможная положительная степень окисления, как правило равна номеру группы в Периодической
- 7. Типичные восстановители и окислители К типичным окислителям относятся: галогены, кислород О2, озон О3, пероксиды Н2О2, производные
- 8. Типичные восстановители и окислители К типичным восстановителям могут быть отнесены: простые вещества — металлы (наиболее сильные
- 9. Типичные восстановители и окислители Очевидно, что элемент в высшей степени окисления может проявлять только окислительные свойства,
- 10. Классификация окислительно-восстановительных реакций Реакции межмолекулярного окисления-восстановления. В подобных реакциях восстановитель и окислитель — разные химические элементы,
- 11. Классификация окислительно-восстановительных реакций Реакции диспропорционирования. Так называются реакции, в которых и окислитель, и восстановитель — один
- 12. Классификация окислительно-восстановительных реакций Реакции сопропорционирования. Реакции сопропорционирования являются обратными по отношению к реакциям диспропорционирования и являются
- 14. Скачать презентацию











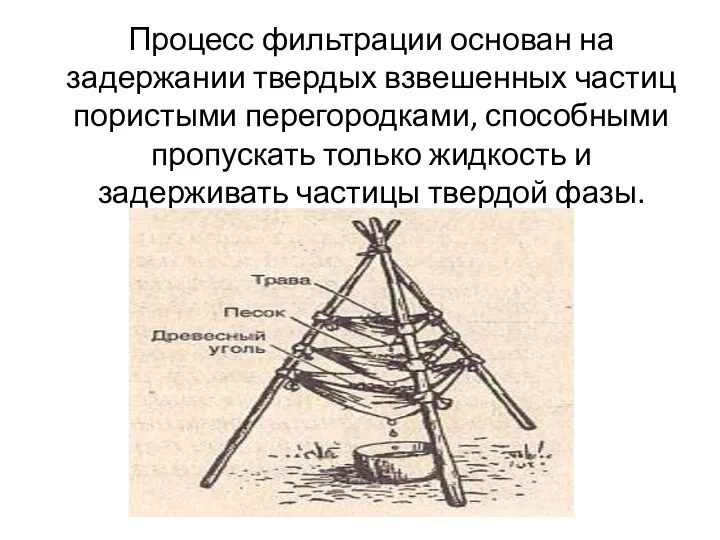 Процесс фильтрации - задержание твердых взвешенных частиц
Процесс фильтрации - задержание твердых взвешенных частиц Интрузивные контакты. Контакты интрузивных и осадочных пород
Интрузивные контакты. Контакты интрузивных и осадочных пород Химическая лаборатория
Химическая лаборатория Презентация на тему Предельные углеводороды
Презентация на тему Предельные углеводороды  Полиморфизм. Аморфные вещества
Полиморфизм. Аморфные вещества Дисахариды и полисахариды
Дисахариды и полисахариды Химия углеводов
Химия углеводов Неметаллы
Неметаллы Электролиз расплавов и растворов электролитов
Электролиз расплавов и растворов электролитов Химические реакции (2)
Химические реакции (2) 9-4
9-4 11_PERMANGANATOMETRIYa_JODOMETRIYa_1
11_PERMANGANATOMETRIYa_JODOMETRIYa_1 Типы химических реакций
Типы химических реакций Классификация, хранение, маркировка химических реактивов
Классификация, хранение, маркировка химических реактивов Изотопы. Области применения изотопов
Изотопы. Области применения изотопов Знакомство с химией
Знакомство с химией Теория строения органических соединений
Теория строения органических соединений Химия Солнца
Химия Солнца А правда ли мыло волшебное?
А правда ли мыло волшебное? Взаимное влияние атомов в молекулах
Взаимное влияние атомов в молекулах Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы
Основы теории сплавов. Типы сплавов (твердые растворы, сплавы-смеси, сплавы- химические соединения. Диаграммы Буферные растворы. Буферная емкость
Буферные растворы. Буферная емкость Сeквенирование нуклеиновых кислот
Сeквенирование нуклеиновых кислот Непредельные углеводороды
Непредельные углеводороды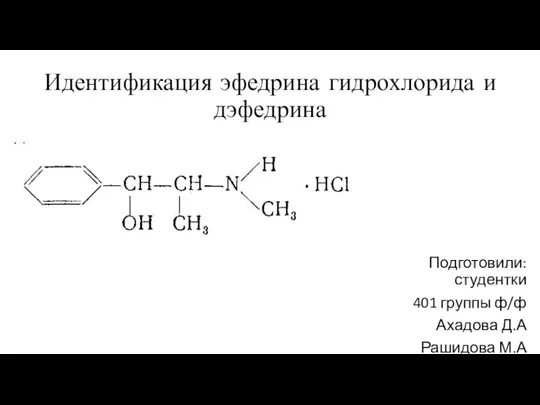 Идентификация эфедрина гидрохлорида и дэфедрина
Идентификация эфедрина гидрохлорида и дэфедрина Определение качества дизельного топлива
Определение качества дизельного топлива Выбор материала для изготовления зубчатых колес
Выбор материала для изготовления зубчатых колес Для чего нужна нефть
Для чего нужна нефть