Содержание
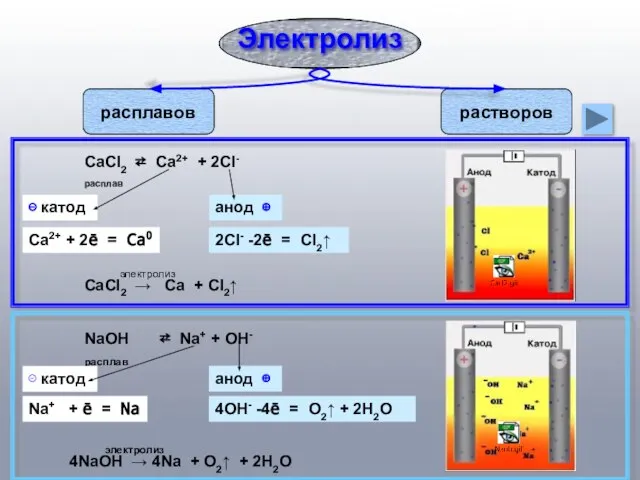
- 2. Электролиз расплавов растворов CaCl2 ⇄ Ca2+ + 2Cl- расплав ⊝ катод анод ⊕ Ca2+ + 2ē
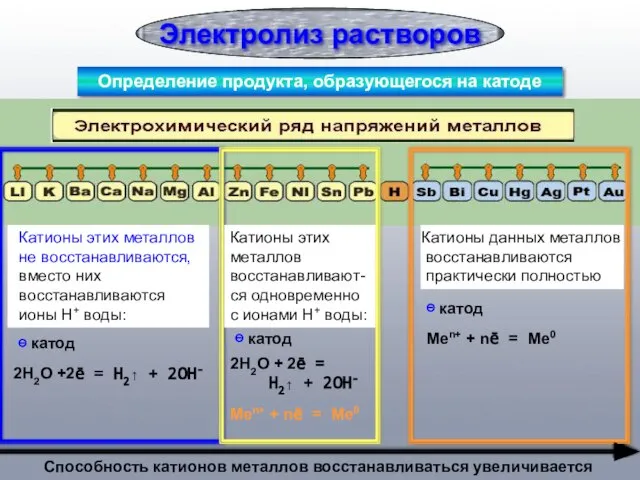
- 3. Электролиз растворов Определение продукта, образующегося на катоде Катионы этих металлов не восстанавливаются, вместо них восстанавливаются ионы
- 4. Электролиз растворов Определение продукта, образующегося на аноде S2- I- Br- Cl- OH- SO42- NO3- CO32- PO43-
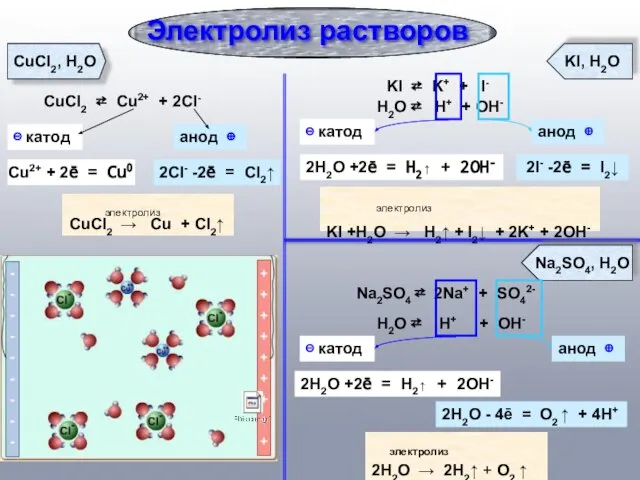
- 5. CuCl2 ⇄ Cu2+ + 2Cl- Электролиз растворов ⊝ катод анод ⊕ Cu2+ + 2ē = Cu0
- 6. Na2SO4 + H2O → Диссоциация: Na2SO4 →2 Na+ + SO42− аноде (+) : SO42−, Н2О: 2
- 7. Ni2+ + 2e− = Ni0 2Н2О + 2e− = Н20 + 2ОН−; NiSO4 + H2O →
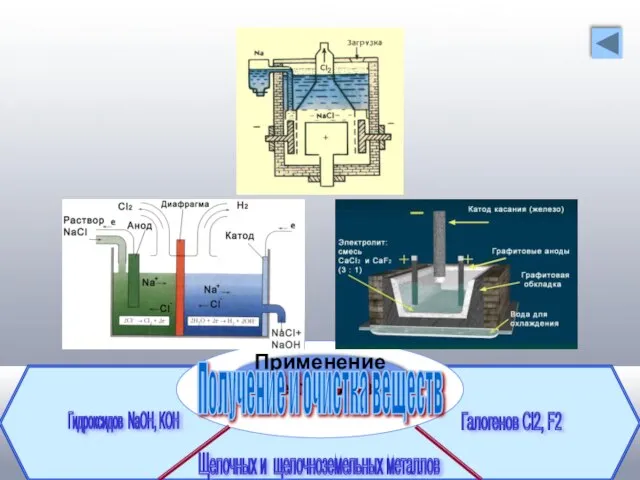
- 8. Применение электролиза Получение и очистка веществ Щелочных и щелочноземельных металлов Гидроксидов NaOH, KOH Галогенов Cl2, F2
- 10. Скачать презентацию



 Презентация на тему Полисахариды
Презентация на тему Полисахариды  Уксусная кислота
Уксусная кислота Угольная кислота и ее соли
Угольная кислота и ее соли Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления
Инновационное производство синтетических мелкокодисперсных оксидов и оборудования для их изготовления Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли
Презентация на тему Изучение реакции среды в зависимости от типа гидролиза соли  Вода – самое удивительное вещество на Земле
Вода – самое удивительное вещество на Земле Фосфорная кислота и ее свойства
Фосфорная кислота и ее свойства Кристаллические решетки, вид связи и свойства веществ
Кристаллические решетки, вид связи и свойства веществ Презентация на тему Значение Периодического закона Д.И.Менделеева
Презентация на тему Значение Периодического закона Д.И.Менделеева  Reshenie_zadach
Reshenie_zadach Презентация на тему Растворение. Растворы (8 класс)
Презентация на тему Растворение. Растворы (8 класс)  Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории
Практическая работа. Решение экспериментальных задач по неорганической химии с использованием виртуальной лаборатории Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами
Возможности окрашивания поверхности стекла путем высокотемпературной ионообменной обработки с выбранными реагентами Углеводороды
Углеводороды Химическая идентификация основных классов биомолекул
Химическая идентификация основных классов биомолекул Многообразие органических веществ
Многообразие органических веществ Ароматические вещества и их значение для человека
Ароматические вещества и их значение для человека Ионные уравнения. Кислоты, их классификация. 8 класс
Ионные уравнения. Кислоты, их классификация. 8 класс Характеристика 1-й аналитической группы анионов
Характеристика 1-й аналитической группы анионов Интерактивная интеллектуальная игра. Юный химик
Интерактивная интеллектуальная игра. Юный химик Драгоценные камни
Драгоценные камни Электролитическая диссоциация
Электролитическая диссоциация Техника безопасности на уроках химии
Техника безопасности на уроках химии Атомның электрондық құрылысы
Атомның электрондық құрылысы Очистка хозяйственных и сточных вод от азота аммонийного с помощью нитрифицирующих бактерий
Очистка хозяйственных и сточных вод от азота аммонийного с помощью нитрифицирующих бактерий Обобщение знаний по курсу органической химии
Обобщение знаний по курсу органической химии Растворы, растворимость
Растворы, растворимость Презентация на тему День Земли, Воды и Чистого воздуха
Презентация на тему День Земли, Воды и Чистого воздуха