Содержание
- 2. «Считай несчастным тот день или тот час, в который ты не усвоил ничего нового и ничего
- 3. «Выбери правильный ответ» (тела) С - железо К -стакан Д -ваза Е - стекло О -
- 4. Л - горение костра В - дробление сахара А - протухание яйца Д - испарение воды
- 5. Секретная лаборатория. 2. Угадай элемент по подсказке 1. Его содержание в водах Мирового океана составляет примерно
- 6. Секретная лаборатория. 2. Угадай элемент по подсказке 1.За 350 лет до нашей эры Аристотель в своих
- 7. Секретная лаборатория. 2. Угадай элемент по подсказке 1. Известен с глубокой древности. 2. Назван по имени
- 8. Секретная лаборатория. 2. Угадай элемент по подсказке 1. В организме человека его содержится около 3 грамм
- 9. Секретная лаборатория. 3. Выбрать формулу, составленную с учётом валентности. 1) Zn2O, 2)H2O, 3)Al2O, 4)K3O.
- 10. Секретная лаборатория. 4. Сумма всех валентностей даст точную массу этого вещества Al2O3, P2O5, MnO2, Cl2O7, SO3,
- 11. Секретная лаборатория. 5. Исключите лишнее 1)BaO 2) HCl 3) Zn 4) H2O
- 12. Секретная лаборатория. 6. Вычислив сумму относительных молекулярных масс верно, вы получите год открытия периодического закона Д.И.
- 13. Секретная лаборатория. 7. Выберите свойство, которое не относится к химическим изменение цвета; запах; агрегатное состояние; выделение
- 14. 8. Кейс Паша заболел и его положили в больницу. Когда Паша выздоровел, оказалось, что он пропустил
- 15. Типы химических реакций В реакциях соединения из нескольких исходных веществ образуется одно сложное вещество. 2Mg +
- 16. 8. Кейс
- 17. 8. Кейс
- 18. 8. Кейс Находясь долгое время на воздухе. Медь покрывается плёнкой малахита, образующегося по реакции 2Cu +
- 19. 9. Сумма коэффициентов в уравнении 2Fe + 3Cl2 = 2FeCl3 10. Вычислить массовую долю кислорода в
- 20. Синквейн 1. 2. 3. 4. 5.
- 22. Скачать презентацию



















 Азотная кислота
Азотная кислота Окислительно-восстановительные реакции (ОВР)
Окислительно-восстановительные реакции (ОВР) Игра Что? Где? Когда?. Химия
Игра Что? Где? Когда?. Химия Обратимость химических реакций. Химическое равновесие
Обратимость химических реакций. Химическое равновесие Индиго-краситель
Индиго-краситель Растительные источники жиров и жирных масел
Растительные источники жиров и жирных масел Макро- и микромир
Макро- и микромир Коррозия металлов
Коррозия металлов Сказка о братьях карбонатах
Сказка о братьях карбонатах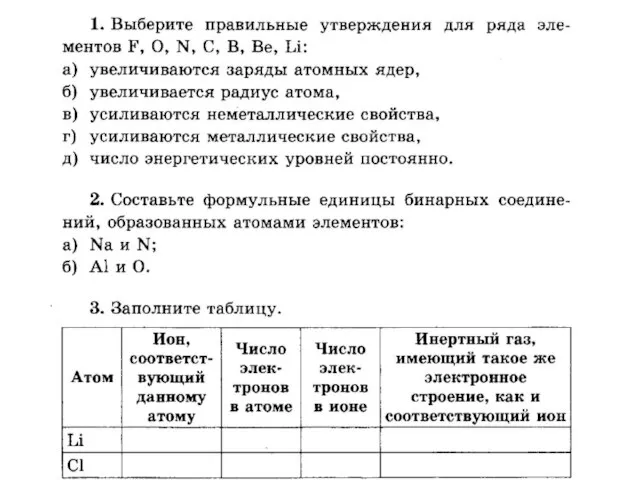 Взаимодействие атомов элементов-неметаллов между собой
Взаимодействие атомов элементов-неметаллов между собой Полиамиды (ПА)
Полиамиды (ПА) Фосфориты. Добыча фосфоритов
Фосфориты. Добыча фосфоритов Способы выражения концентраций растворов
Способы выражения концентраций растворов Кислородсодержащие органические соединения
Кислородсодержащие органические соединения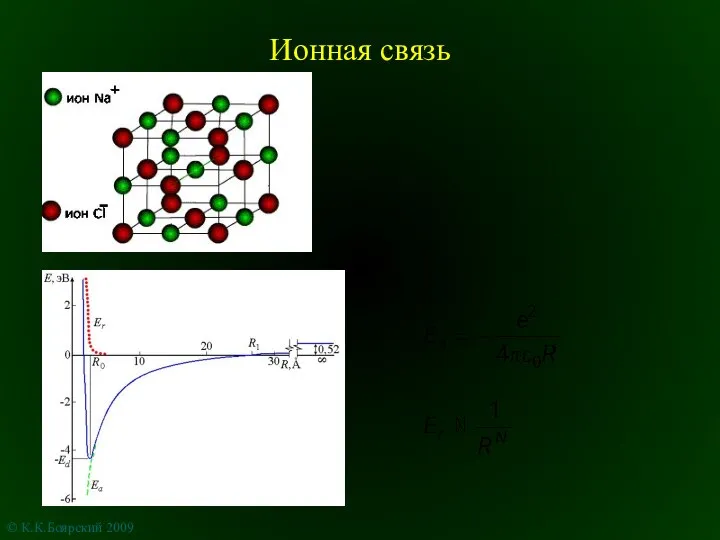 Ионная связь
Ионная связь Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Карбоновые кислоты, их строение, номенклатура, получение и свойства
Карбоновые кислоты, их строение, номенклатура, получение и свойства Уравнение состояния идеального газа
Уравнение состояния идеального газа Шаблон для презентации по химии
Шаблон для презентации по химии Перициклические реакции
Перициклические реакции Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу
Оңай балқитын флюстерді қолдана отырып хромкенді шекемтастар алу мүмкіндігін зерттеу Катализ в нефтепереработке
Катализ в нефтепереработке Органические галогениды. (Лекция 7)
Органические галогениды. (Лекция 7) Составление уравнений окислительно-восстановительных реакций
Составление уравнений окислительно-восстановительных реакций Жиры
Жиры Скорость химических реакций
Скорость химических реакций 1666603286718__4v20ts
1666603286718__4v20ts Основы МКТ
Основы МКТ