Содержание
- 2. четвертый по распространенности в земной коре, второй среди металлов Fe элемент № 26 в периодической системе
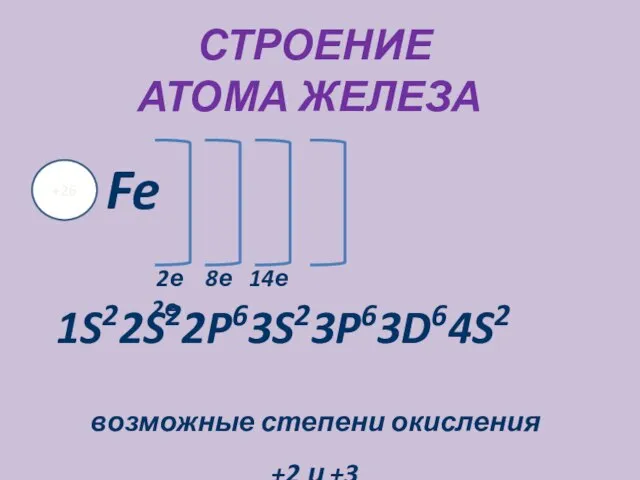
- 3. СТРОЕНИЕ АТОМА ЖЕЛЕЗА +26 Fe 2е 8е 14е 2е 1S22S22P63S23P63D64S2 возможные степени окисления +2 и +3
- 4. Железо в природе В земной коре на долю железа приходится около 4,1% массы земной коры (4-е
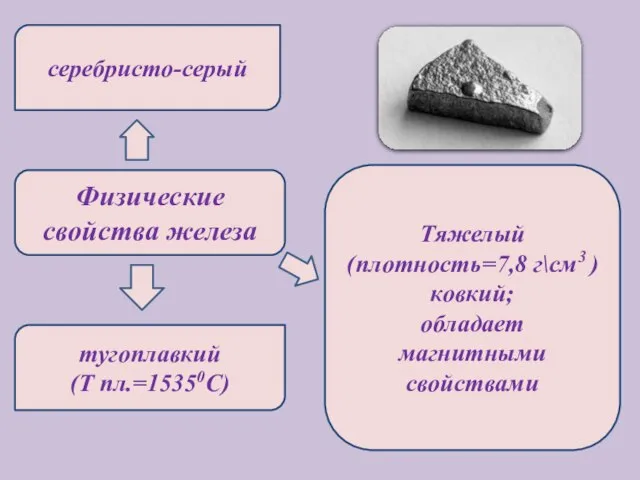
- 5. Физические свойства железа серебристо-серый тугоплавкий (Т пл.=15350C) Тяжелый (плотность=7,8 г\см3 ) ковкий; обладает магнитными свойствами
- 6. Химические свойства Реакции с простыми веществами Железо сгорает в кислороде при нагревании: 4Fe +3O2=2Fe2O3 Реагирует с
- 7. Химические свойства Реакции со сложными веществами С кислотами: А) с соляной кислотой 2HCL + Fe =
- 8. 4Fe + 2Н2О + ЗО2 = 2(Fe2O3•Н2О) Железо разрушается под действием окружающей среды, т.е. подвергается коррозии
- 10. Скачать презентацию





 Химия как наука. Краткая история развития химии. Значение химии
Химия как наука. Краткая история развития химии. Значение химии Выбраковка результатов химического анализа
Выбраковка результатов химического анализа Химические реакции. Вещество
Химические реакции. Вещество Формальдегид. Карбоновые кислоты
Формальдегид. Карбоновые кислоты Алкены. Ҳимические свойства алкенов
Алкены. Ҳимические свойства алкенов Химическая связь и ее типы
Химическая связь и ее типы Производство аммиака
Производство аммиака Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах
Презентация на тему Обобщение знание и умений и предельных и непредельных углеводородах  Определение степеней окисления и расстановка коэффициентов в ОВР
Определение степеней окисления и расстановка коэффициентов в ОВР Общие знания по курсу неорганической химии
Общие знания по курсу неорганической химии Задачи. Периодическая система. Строение атома. Повторение
Задачи. Периодическая система. Строение атома. Повторение Синтез и реакции пиридазина
Синтез и реакции пиридазина Моющие и чистящие средства
Моющие и чистящие средства Алкадиены. Каучук
Алкадиены. Каучук Приёмы работы с текстом на уроках химии
Приёмы работы с текстом на уроках химии Химия в косметологии
Химия в косметологии Текстуры руд
Текстуры руд Витамины. (10 класс)
Витамины. (10 класс) Кислоты (часть 2). 8 класс
Кислоты (часть 2). 8 класс Моделирование деформаций углеродных слоёв при функционализации технического углерода
Моделирование деформаций углеродных слоёв при функционализации технического углерода Круговорот азота
Круговорот азота Среды для культивирования эмбрионов-история разработки и составы
Среды для культивирования эмбрионов-история разработки и составы Презентация на тему Природные источники углеводородов (9 класс)
Презентация на тему Природные источники углеводородов (9 класс)  Углеводы. Стереохимия углеводов в проекциях Фишера
Углеводы. Стереохимия углеводов в проекциях Фишера Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты
Карбоновые кислоты и их гетерофункциональные производные: гидрокси- и оксокарбоновые кислоты Синтез латексов
Синтез латексов Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки
Экспериментальное исследование кипения сверхтекучего гелия на цилиндрическом нагревателе внутри пористой оболочки Физические и химические явления 8 класс Учитель химии Кузнецова А.Н.
Физические и химические явления 8 класс Учитель химии Кузнецова А.Н.