Содержание
- 2. 1. История открытия галогенов 2. Положение в Периодической системе 3. Химические свойства 4. Применение 5.Проверка знаний
- 3. Фтор История открытия галогенов Хлор Бром Йод Астат
- 4. В 1886 году французский химик А. Муассан, используя электролиз жидкого фтороводорода, охлажденного до температуры –23°C (в
- 5. В 1774 году шведский ученый К. Шееле открыл хлор, который принял за сложное вещество и назвал
- 6. В 1825 году французский химик А.Ж.Балар при изучении маточных рассолов выделил темно-бурую жидкость, который он назвал
- 7. В 1811 году французский химик Бернар Куртуа открыл иод путём перегонки маточных растворов от своего азотнокислого
- 8. В 1869 г Д.И.Мендеелеев предсказал его существование и возможность открытия в будущем (как «эка-иод»). Впервые астат
- 9. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 10. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 11. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 12. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 13. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
- 14. Периодическая система химических элементов Д.И.Менделеева Группы элементов I III II VIII IV V VI VII II
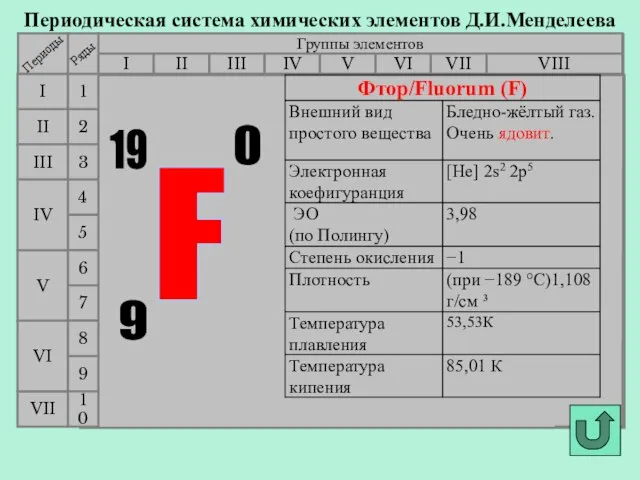
- 15. Химические свойства 45 F2 -наиболее реакционноспособен , реакции идут на холоде, при нагревании – даже с
- 16. Химические свойства Cl2 - сильно реакционноспособен (искл. C, O2, N2 и некот. др.) С простыми веществами:
- 17. Химические свойства Br2 - реакционноспособен С простыми веществами: С металлами С неметаллами Al + Br2 →
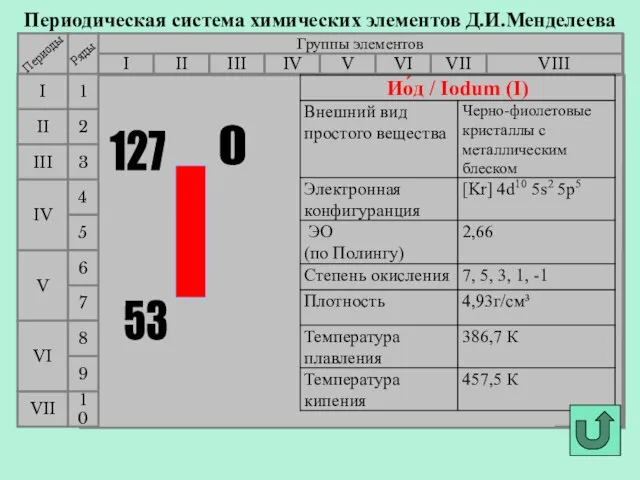
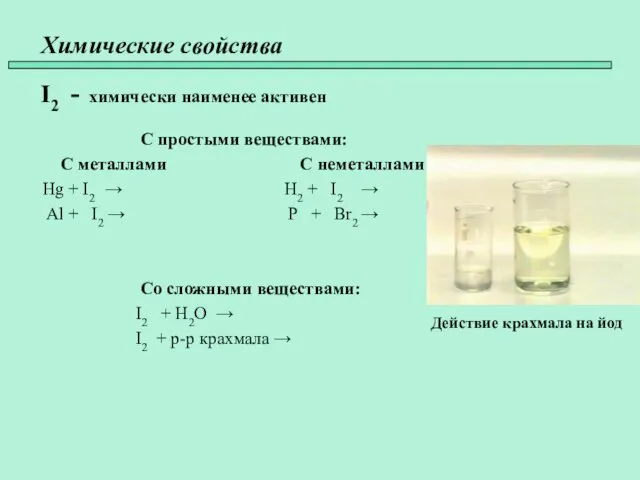
- 18. Химические свойства I2 - химически наименее активен С простыми веществами: С металлами С неметаллами Hg +
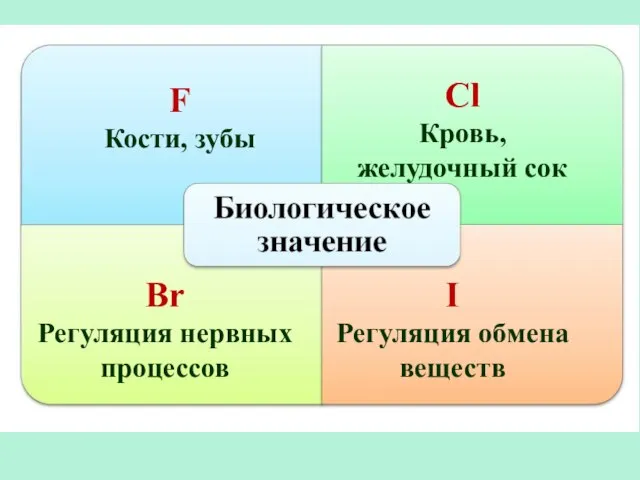
- 19. F Кости, зубы Сl Кровь, желудочный сок Br Регуляция нервных процессов I Регуляция обмена веществ
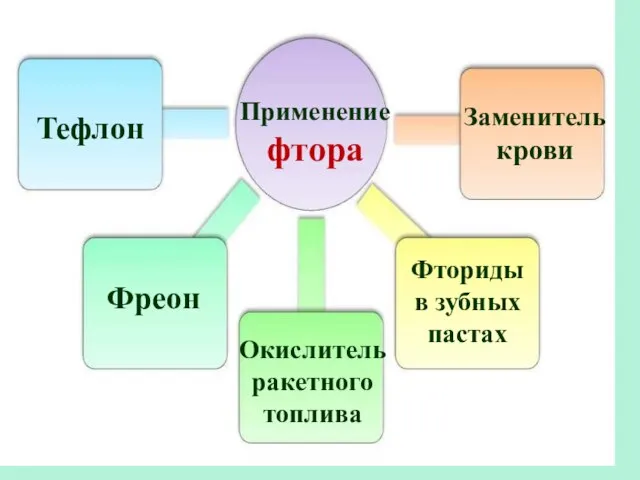
- 20. Применение фтора Тефлон Фреон Окислитель ракетного топлива Заменитель крови Фториды в зубных пастах
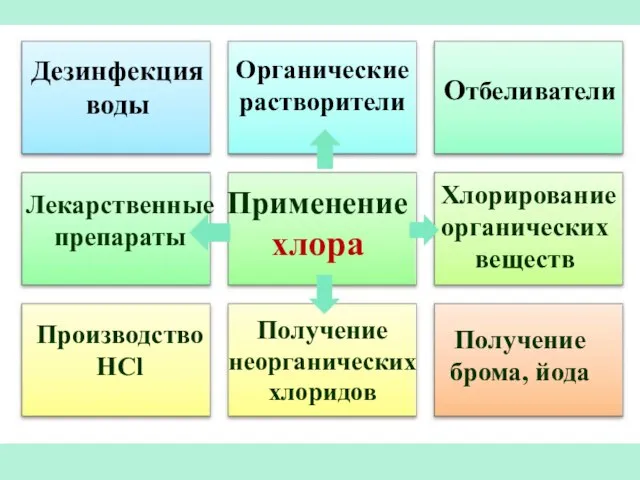
- 21. Применение хлора Отбеливатели Производство HCl Получение брома, йода Дезинфекция воды Органические растворители Лекарственные препараты Хлорирование органических
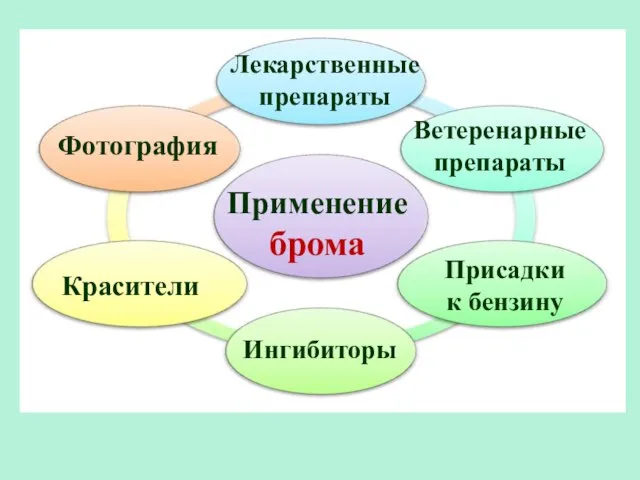
- 22. Применение брома Лекарственные препараты Красители Фотография Ветеренарные препараты Ингибиторы Присадки к бензину
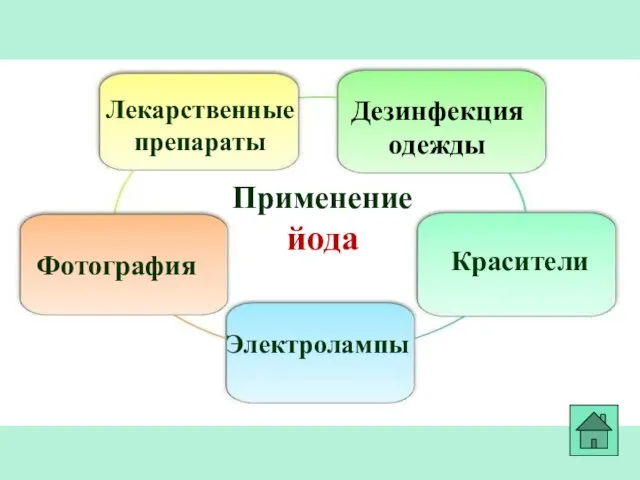
- 23. Применение йода Лекарственные препараты Фотография Красители Дезинфекция одежды Электролампы
- 24. Физические свойства галогенов Заполни пропуски Фтор - , в воде , так как интенсивно с ней
- 25. Химические свойства галогенов Поставь коэффициенты Na + Cl2 = NaCl S + F2 = SF6 Fe
- 26. Химические свойства галогенов Найди соответствие между исходными веществами и продуктами реакций Xe + 2F2 = H2
- 27. § 22, упр.4 Домашнее задание
- 28. Спасибо за урок! Благодарю за сотрудничество.
- 30. Скачать презентацию



















 Химическая география чудес природы
Химическая география чудес природы Эмульсия. Основные типы эмульсий
Эмульсия. Основные типы эмульсий Презентация на тему "Водород"
Презентация на тему "Водород" Растворы
Растворы алотропні модифікації неметалів
алотропні модифікації неметалів Кислород. Физические и химические свойства. Получение
Кислород. Физические и химические свойства. Получение Гетероциклические соединения
Гетероциклические соединения Предельные углеводороды (алканы)
Предельные углеводороды (алканы) Синтез латексов
Синтез латексов Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс
Спирты. Классификация, номенклатура, изомерия, получение и применение. 10 класс Строение атома
Строение атома Substanță chimică
Substanță chimică Гемоглобин. Структура и свойства молекулы гемоглобина
Гемоглобин. Структура и свойства молекулы гемоглобина Задача на химическое равновесие
Задача на химическое равновесие Простые и сложные вещества
Простые и сложные вещества Спирты. К кроссворду
Спирты. К кроссворду Строение вещества. Эксперименты
Строение вещества. Эксперименты Молибден. Получение молибдена
Молибден. Получение молибдена Синтетические душистые вещества
Синтетические душистые вещества 10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1)
10_KhimiaKlassifikatsia_organicheskikh_soedieniy (1) Белки
Белки Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем
Термодинамика. Основные понятия и законы. Особенности термодинамики живых систем Классификация химических реакций (11 класс)
Классификация химических реакций (11 класс) химия
химия Карбоновые кислоты
Карбоновые кислоты Изотопы. Области применения изотопов
Изотопы. Области применения изотопов Презентация на тему Азотная кислота и её соли
Презентация на тему Азотная кислота и её соли  Марганец. Калий
Марганец. Калий