Содержание
- 2. Тест по теме «Ионная и ковалентная химическая связь» 1.Химическая связь в соединении хлора с элементом, в
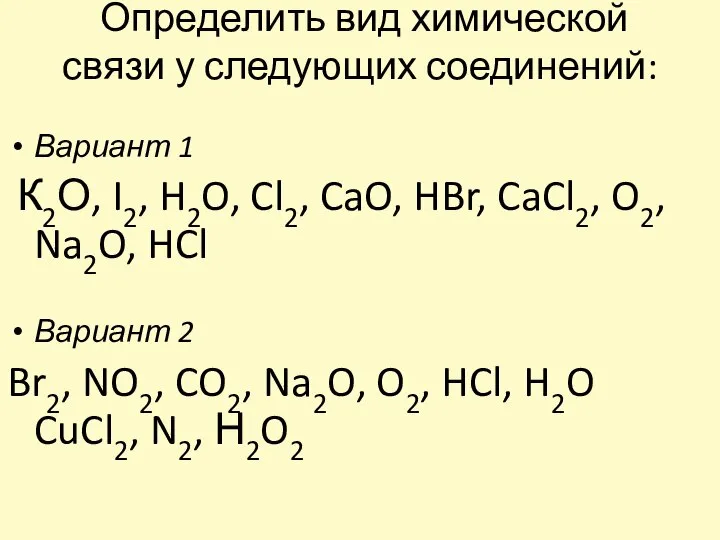
- 3. Определить вид химической связи у следующих соединений: Вариант 1 К2О, I2, H2O, Cl2, CaO, HBr, CaCl2,
- 4. Определите элементы, ставшие не в ту «очередь»: Ca Fe P K Al Mg Na Почему?
- 7. Атомы металлов легко отдают валентные электроны и превращаются в положительные заряженные ионы: Ме0 – n ē
- 8. Свободные электроны, оторвавшиеся от атома, перемещаются между положительными ионами металлов. Между ними возникает металлическая связь, т.
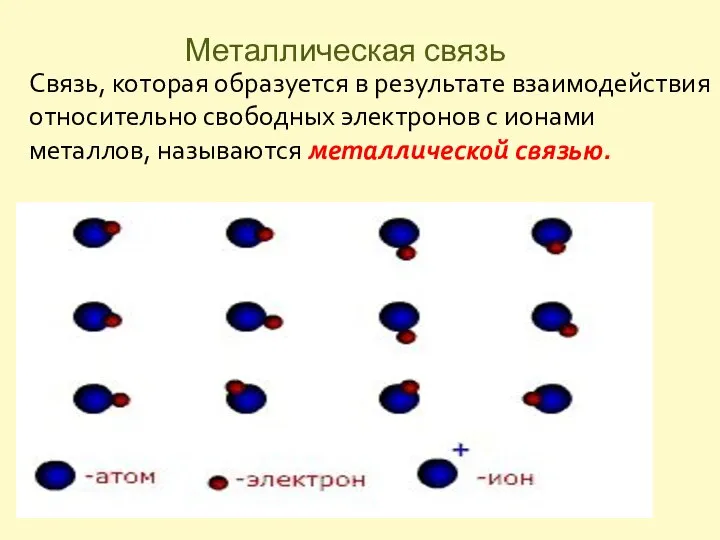
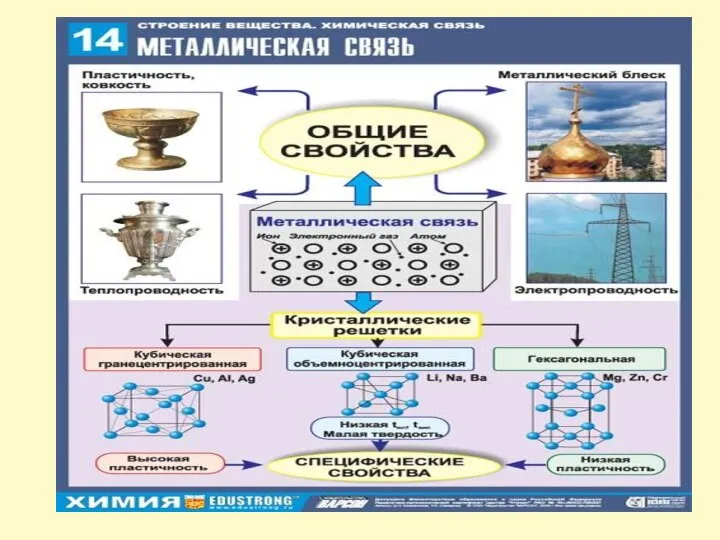
- 9. Металлическая связь Связь, которая образуется в результате взаимодействия относительно свободных электронов с ионами металлов, называются металлической
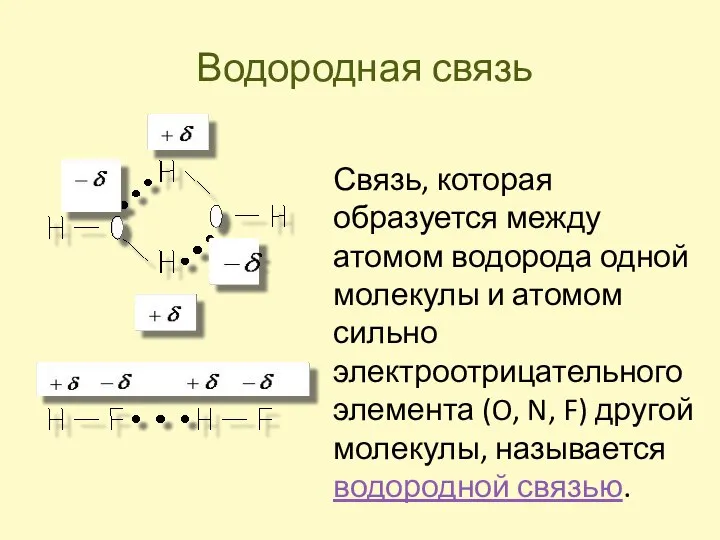
- 11. Водородная связь Связь, которая образуется между атомом водорода одной молекулы и атомом сильно электроотрицательного элемента (O,
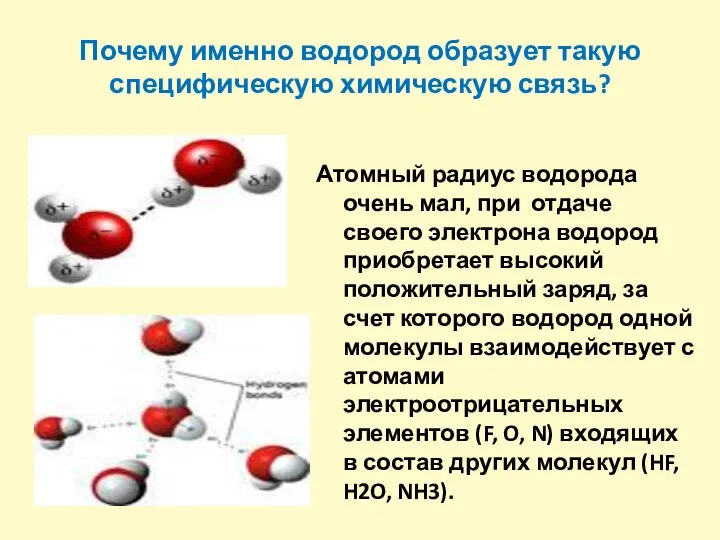
- 12. Почему именно водород образует такую специфическую химическую связь? Атомный радиус водорода очень мал, при отдаче своего
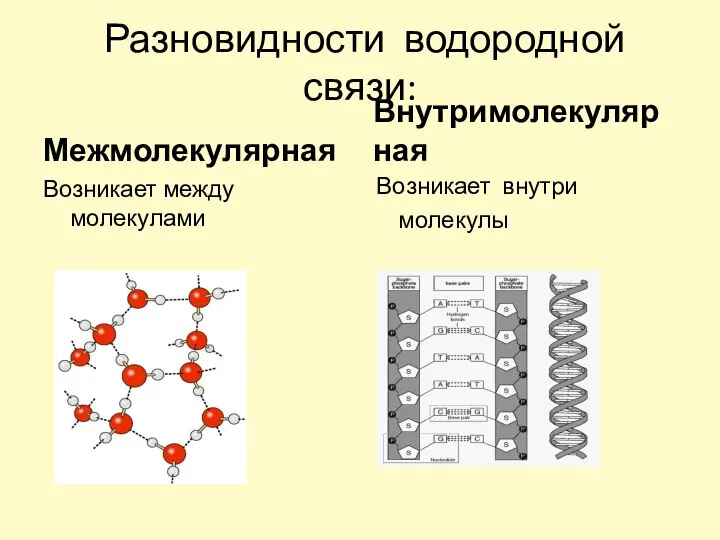
- 13. Разновидности водородной связи: Межмолекулярная Возникает между молекулами Внутримолекулярная Возникает внутри молекулы
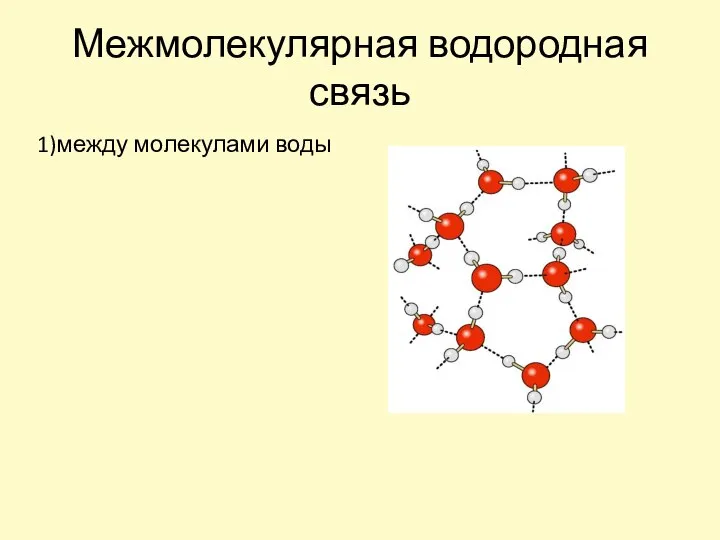
- 14. Межмолекулярная водородная связь 1)между молекулами воды
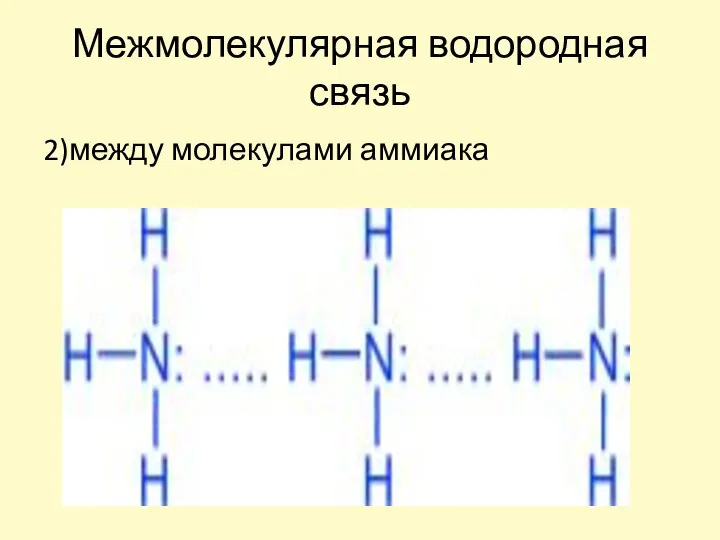
- 15. Межмолекулярная водородная связь 2)между молекулами аммиака
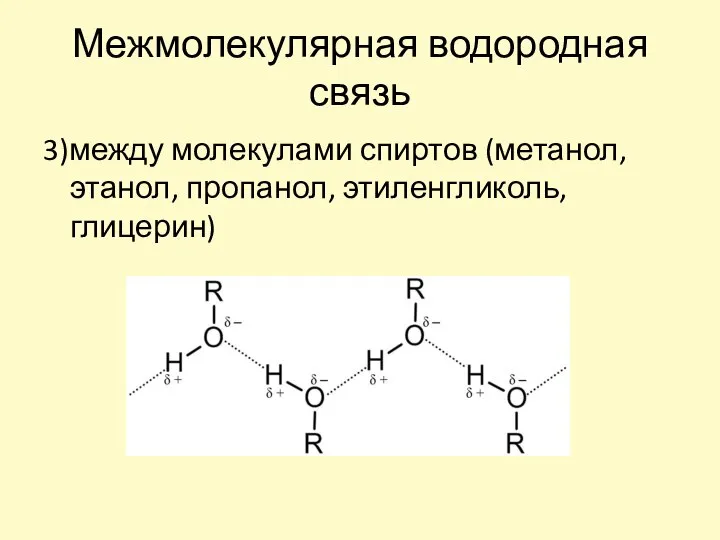
- 16. Межмолекулярная водородная связь 3)между молекулами спиртов (метанол, этанол, пропанол, этиленгликоль, глицерин)
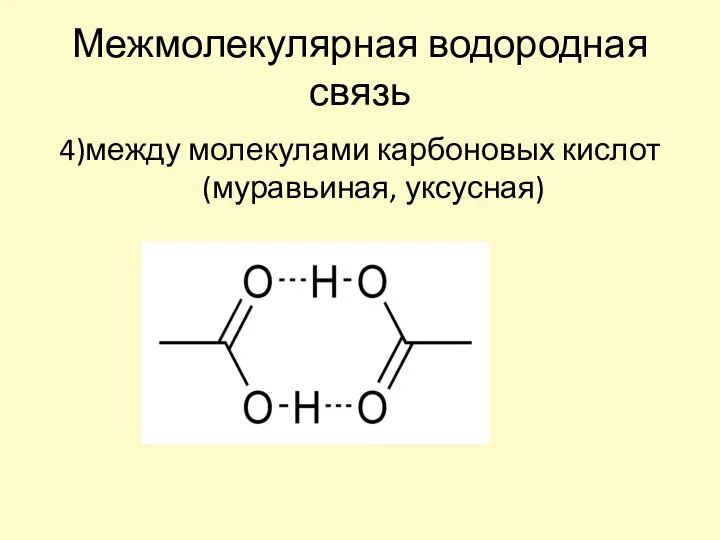
- 17. Межмолекулярная водородная связь 4)между молекулами карбоновых кислот (муравьиная, уксусная)
- 18. Межмолекулярная водородная связь 5)Между молекулами фтороводорода Н – Fδ- … δ+ H – F δ- …
- 19. Особые свойства веществ, образованных межмолекулярной водородной связью 1)вещества с низкой молекулярной массой – жидкости или легко
- 20. Особые свойства веществ, образованных межмолекулярной водородной связью 2)некоторые спирты и кислоты неограниченно растворимы в воде
- 21. Особые свойства веществ, образованных межмолекулярной водородной связью 3)способствуют образованию кристаллов в виде снежинок или измороси
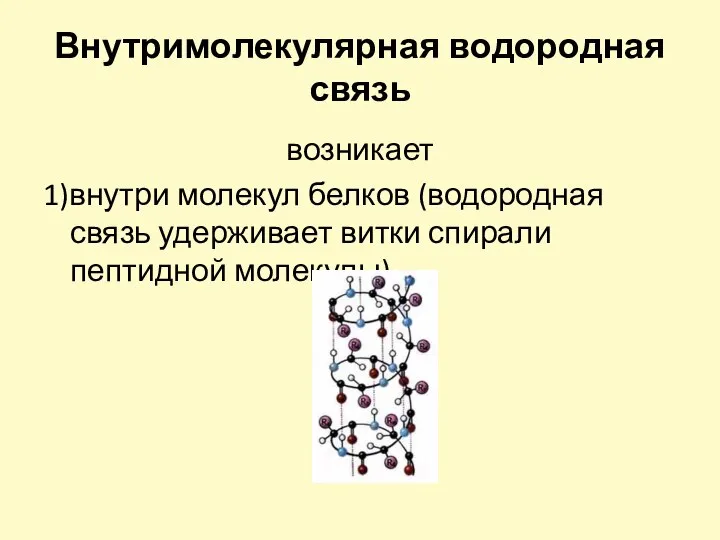
- 22. Внутримолекулярная водородная связь возникает 1)внутри молекул белков (водородная связь удерживает витки спирали пептидной молекулы)
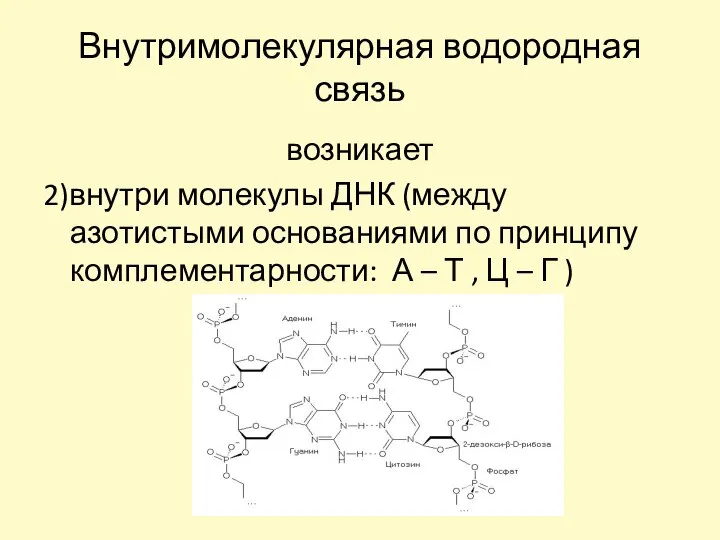
- 23. Внутримолекулярная водородная связь возникает 2)внутри молекулы ДНК (между азотистыми основаниями по принципу комплементарности: А – Т
- 24. Значение внутримолекулярной связи Способствует образованию молекул белков, ДНК и РНК и определяет их функционирование.
- 25. Факторы, разрушающие водородную связь в белковой молекуле (денатурирующие факторы) Электромагнитное излучение Вибрации Высокие температуры Химические вещества
- 26. 1) Для какого вещества характерна водородная связь: а) C₂H₆ б) C₂H₅OH в) CH₃-O-CH₃ г) CH₃COOCH₃ 2)
- 27. 4). Вещество, между молекулами которого существует водородная связь: а) этанол б) метан в) водород г) бензол
- 28. Дом. задание: Задача № 1. В растворе массой 100 г содержится хлорид бария массой 20 г.
- 29. В растворе массой 100 г содержится хлорид бария массой 20 г. Какова массовая доля хлорида бария
- 31. Скачать презентацию















 Вывод и обсуждение
Вывод и обсуждение Структура материалов. Введение в науку о материалах
Структура материалов. Введение в науку о материалах Спирты и фенолы. (Лекция 6.1)
Спирты и фенолы. (Лекция 6.1) Массовая доля растворённого вещества
Массовая доля растворённого вещества Вещества простые и сложные
Вещества простые и сложные Презентация на тему Неметаллы
Презентация на тему Неметаллы  Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород
Преобразование уравнения Нернста. Коэффициент Кда. Причины различия в значениях Кда для различных пород Удельная теплота сгорания
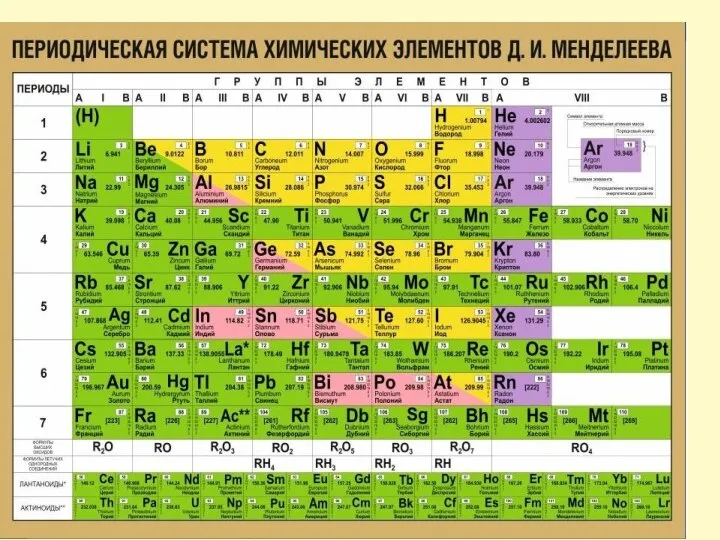
Удельная теплота сгорания Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева
Характеристика химического элемента на основании его положения в Периодической системе Д. И. Менделеева Реакции ионного обмена
Реакции ионного обмена Пластмассы. Классификация
Пластмассы. Классификация Арены. Бензол
Арены. Бензол Очистка поверхности медного сплава
Очистка поверхности медного сплава Презентация на тему Химическая связь
Презентация на тему Химическая связь  Вода
Вода Кремний. Физический свойства. Получение. Применение
Кремний. Физический свойства. Получение. Применение Амфотерные соединения
Амфотерные соединения Основные понятия органической химии
Основные понятия органической химии Амфотерность оксида и гидроксида алюминия
Амфотерность оксида и гидроксида алюминия Изучение геохимических свойств редкоземельных элементов
Изучение геохимических свойств редкоземельных элементов Ниобий. Химические свойства
Ниобий. Химические свойства Реакционная способность химических соединений. Лекция 9
Реакционная способность химических соединений. Лекция 9 Периодическая система Д.И. Менделеева
Периодическая система Д.И. Менделеева Template biosynthesis
Template biosynthesis Физико-химическая механика и реология дисперсных структур. Лекция 15
Физико-химическая механика и реология дисперсных структур. Лекция 15 Комплексное задание по дисциплине основы материаловедения для группы 18
Комплексное задание по дисциплине основы материаловедения для группы 18 Презентация на тему Роль химии в жизни общества
Презентация на тему Роль химии в жизни общества  Осторожно, химия
Осторожно, химия