Содержание
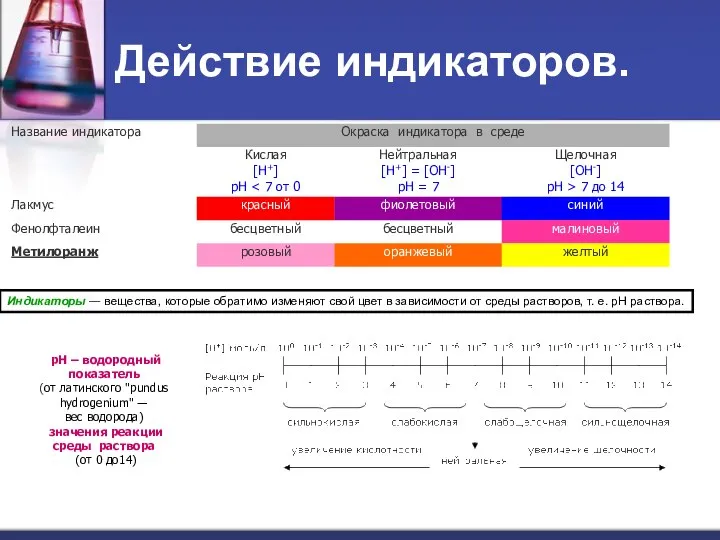
- 2. Действие индикаторов. рН – водородный показатель (от латинского "pundus hydrogenium" ― вес водорода) значения реакции среды
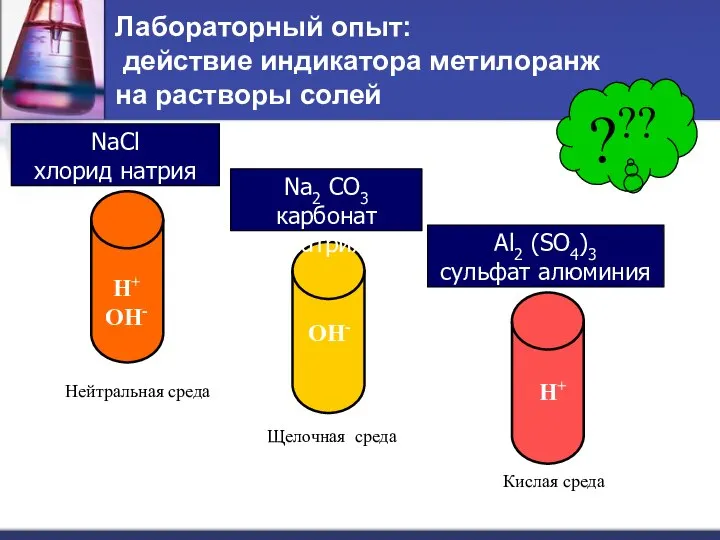
- 3. Лабораторный опыт: действие индикатора метилоранж на растворы солей ??? Na2 CO3 карбонат натрия NaCl хлорид натрия
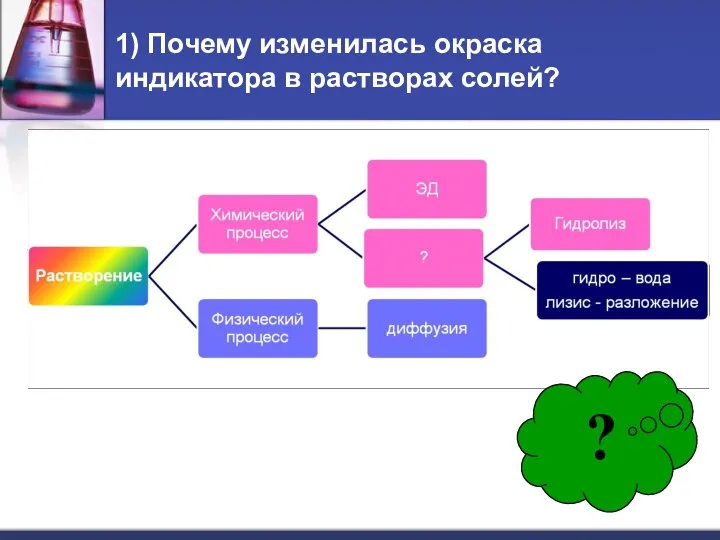
- 4. 1) Почему изменилась окраска индикатора в растворах солей? ?
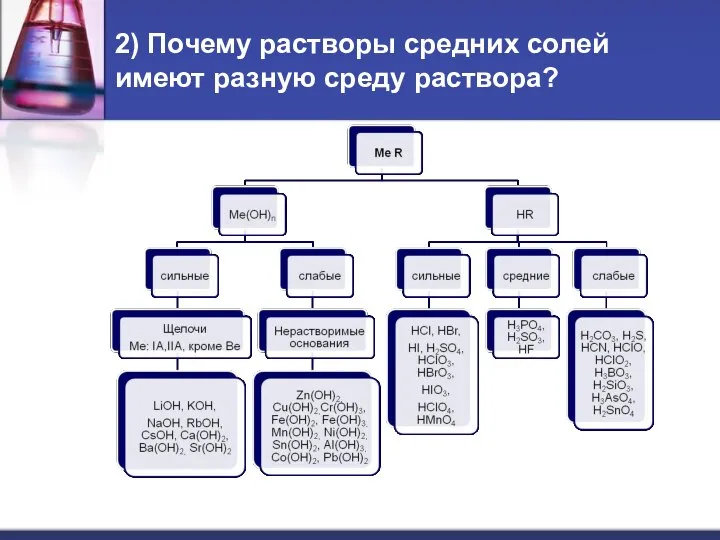
- 5. 2) Почему растворы средних солей имеют разную среду раствора?
- 6. Схема гидролиза сульфата алюминия Al(OH)3 H2SO4 слабое основание сильная кислота [OH]- (что сильней того и больше!)
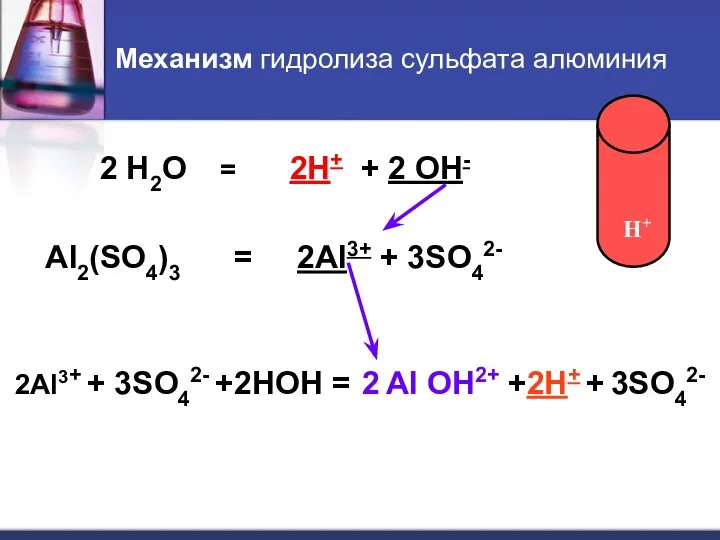
- 7. Механизм гидролиза сульфата алюминия 2 H2O = 2H+ + 2 OH- Al2(SO4)3 = 2Al3+ + 3SO42-
- 8. АЛГОРИТМ СОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ 1. Определяем тип гидролиза. Составляем уравнение ЭД соли: Al2(SO4)3 =
- 9. Сформулируем вывод: Соли, образованные сильн___________ и слаб____________ гидролизируют по ________________ с образованием ___________________ и _______________, обуславливающих
- 10. Сформулируем вывод: Соли, образованные сильной кислотой и слабым основанием гидролизируют по катиону с образованием гидроксокатионов и
- 11. Схема гидролиза карбоната натрия NaOH H2CO3 сильное основание слабая кислота [OH]- > [H]+ (что сильней того
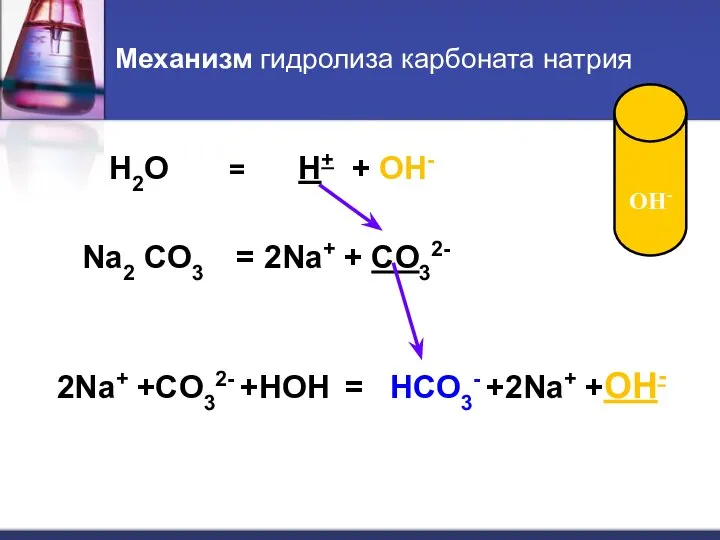
- 12. Механизм гидролиза карбоната натрия H2O = H+ + OH- Na2 CO3 = 2Na+ + CO32- 2Na+
- 13. АЛГОРИТМ СОСТАВЛЕНИЯ УРАВНЕНИЙ РЕАКЦИЙ ГИДРОЛИЗА СОЛЕЙ 1. Определяем тип гидролиза. Составляем уравнение ЭД соли: Na2 CO3
- 14. Сформулируем вывод: Соли, образованные сильн___________ и слаб____________ гидролизируют по ________________ с образованием ___________________ и _______________, обуславливающих
- 15. Сформулируем вывод: Соли, образованные сильным основанием и слабой кислотой гидролизируют по аниону с образованием гидроанионов и
- 16. Схема гидролиза хлорида натрия NaOH HCl сильное основание сильная кислота [OH]- = [H]+ Н е й
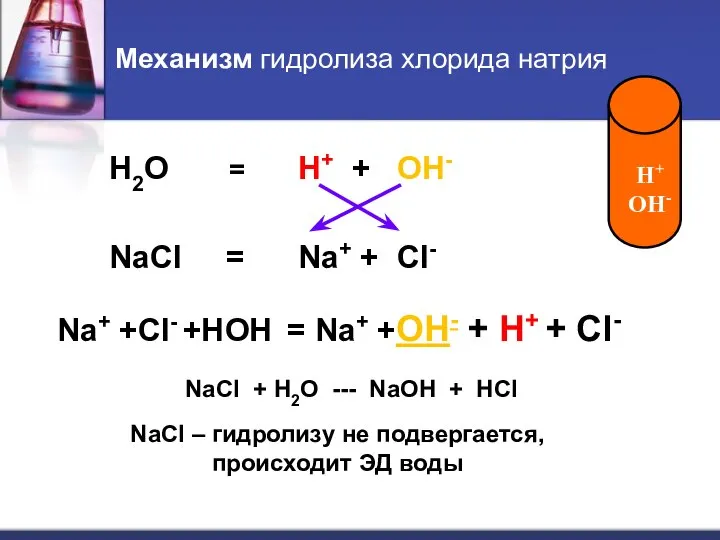
- 17. Механизм гидролиза хлорида натрия H2O = H+ + OH- NaCl = Na+ + Cl- Na+ +Cl-
- 18. Сформулируем вывод: Соли, образованные сильным основанием и сильным кислотой Не гидролизируют. Происходит ЭД воды, обуславливающая нейтральную
- 19. Схема гидролиза сульфида алюминия Al(OH)3 H2S слабое основание слабая кислота [OH]- = [H]+ Н е й
- 20. Сформулируем вывод: Соли, образованные ___________ и ____________ гидролизируют по ________________ с образованием ___________________ и _______________, обуславливающих
- 21. Сформулируем вывод: Соли, образованные слабой кислотой и слабым основанием гидролизируют одновременно по аниону и катиону с
- 22. Сформулируем определение понятия «гидролиз»: К какому типу мы отнесем данные реакции? Какие вещества в них участвуют?
- 23. Закрепление: самостоятельно заполните таблицу на основе эксперимента
- 24. Закрепление: проверка.
- 25. Роль гидролиза в природе: Преобразование земной коры Обеспечение слабощелочной среды морской воды Роль гидролиза в повседневной
- 27. Скачать презентацию
![Схема гидролиза сульфата алюминия Al(OH)3 H2SO4 слабое основание сильная кислота [OH]- (что](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1075223/slide-5.jpg)



![Схема гидролиза карбоната натрия NaOH H2CO3 сильное основание слабая кислота [OH]- >](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1075223/slide-10.jpg)



![Схема гидролиза хлорида натрия NaOH HCl сильное основание сильная кислота [OH]- =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1075223/slide-15.jpg)

![Схема гидролиза сульфида алюминия Al(OH)3 H2S слабое основание слабая кислота [OH]- =](/_ipx/f_webp&q_80&fit_contain&s_1440x1080/imagesDir/jpg/1075223/slide-18.jpg)






 Презентация на тему Соединения серы
Презентация на тему Соединения серы  Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов
Основные законы и понятия химии. Основные классы неорганических соединений. Химический эквивалент. Закон эквивалентов Незаменимая уксусная кислота
Незаменимая уксусная кислота Перегонка. Вклад алхимиков в органическую химию
Перегонка. Вклад алхимиков в органическую химию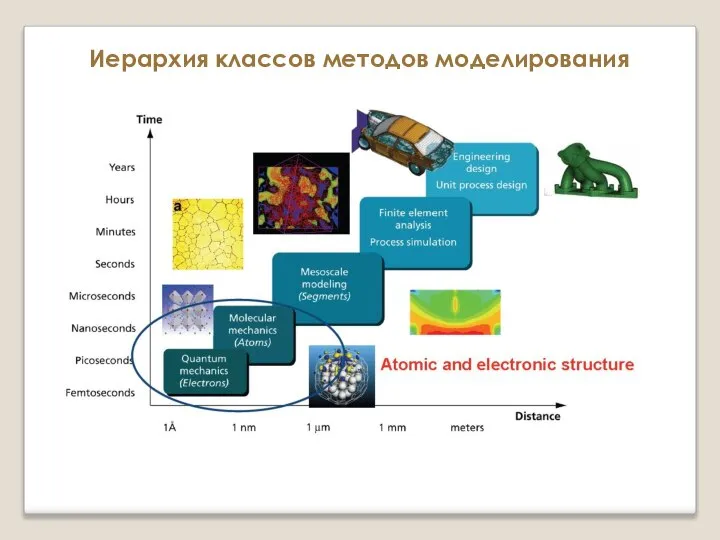 Иерархия классов методов моделирования. Атомистические и микроскопические методы
Иерархия классов методов моделирования. Атомистические и микроскопические методы Магний и кальций
Магний и кальций Сахароза, крахмал, целлюлоза
Сахароза, крахмал, целлюлоза Строение сложного фермента
Строение сложного фермента Хімія у вирішенні промислової проблеми
Хімія у вирішенні промислової проблеми Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент
Вещество и тело. Атом и молекула. Свойства веществ. Простые и сложные вещества. Химический элемент Основи молекулярно-кінетичної теорії
Основи молекулярно-кінетичної теорії Углеводороды. Общие знания
Углеводороды. Общие знания Gelation in aqueous solution of L-cysteine and silver nitrate
Gelation in aqueous solution of L-cysteine and silver nitrate Заполни электронные уровни элементов
Заполни электронные уровни элементов Явление аллотропии
Явление аллотропии Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала
Исследование структуры продуктов аммонолиза мезопористых магниетермических порошков тантала Центробежное осаждение
Центробежное осаждение Характеристика кислорода и серы
Характеристика кислорода и серы Актуальные задачи химии
Актуальные задачи химии Металлы - наши друзья или враги
Металлы - наши друзья или враги Получение, свойства и применение алкенов
Получение, свойства и применение алкенов Классификация силикатов
Классификация силикатов Способы получения металлов
Способы получения металлов Фуллерены
Фуллерены 6. Характеристика элементов на основе положения в периодической системе
6. Характеристика элементов на основе положения в периодической системе Природные источники углеводородов
Природные источники углеводородов علاوي الندوة
علاوي الندوة Цезій
Цезій