Содержание
- 2. «Органическая химия может сейчас кого угодно свести с ума. Она представляется мне дремучим лесом, полным удивительных
- 3. Теория радикалов (30 гг. XIX в Й.Берцелиус, Ю.Либих, Ж.Дюма) В состав органических веществ входят радикалы; Радикалы
- 4. Теория типов (40-50 гг. XIX в. Ш.Жерар, А.Кекуле и др.) Все органические вещества – производные простейших
- 5. К первой половине XIX века в органической химии был накоплен громадный фактический материал, дальнейшее изучение которого
- 6. Предпосылки возникновения теории Развитие и утверждение атомистических представлений (съезд в Карслруэ, 1860г.); Установление понятий валентности (Э.
- 7. Теоретические разработки добутлеровского периода внесли определенный вклад в познание строения органических соединений. Но ни одна из
- 8. Бутлеров Александр Михайлович (1828-1886) Русский химик, академик Петербургской АН (с 1874 г.). Окончил Казанский университет (1849
- 9. Теория строения органических соединений Теория химического строения органических соединений, выдвинутая А. М. Бутлеровым во второй половине
- 10. Основные положения теории строения органических веществ (А.М. Бутлеров 1861 – 1864 гг.) 1. Атомы в молекулах
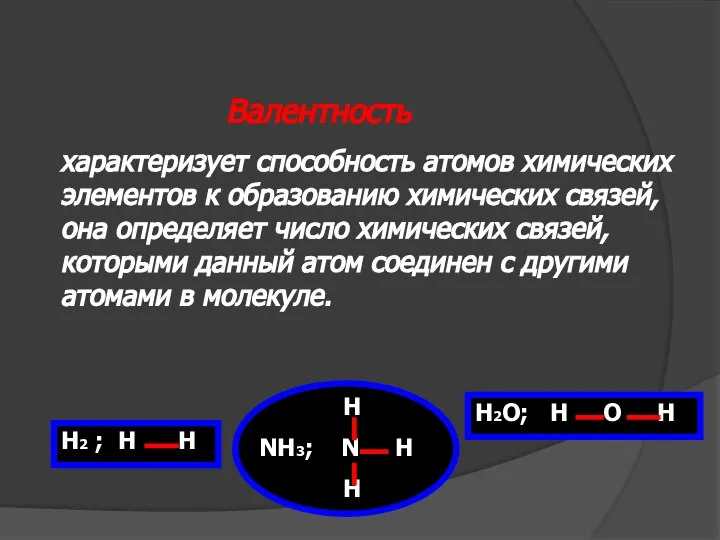
- 11. Валентность характеризует способность атомов химических элементов к образованию химических связей, она определяет число химических связей, которыми
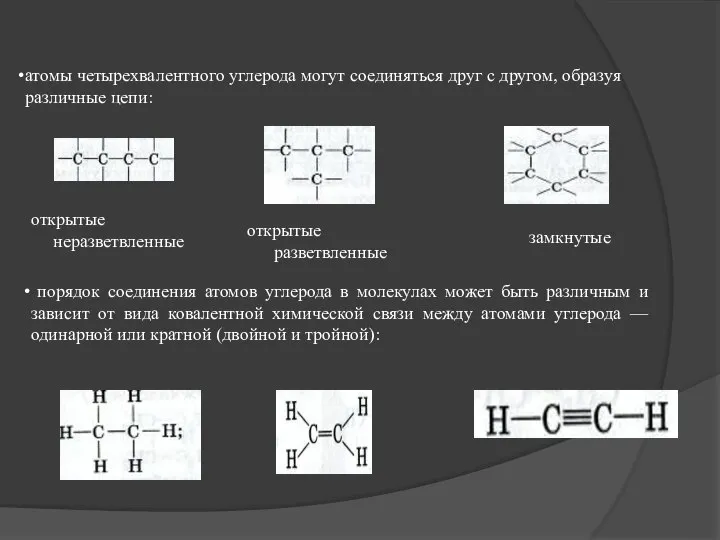
- 12. атомы четырехвалентного углерода могут соединяться друг с другом, образуя различные цепи: открытые неразветвленные замкнутые порядок соединения
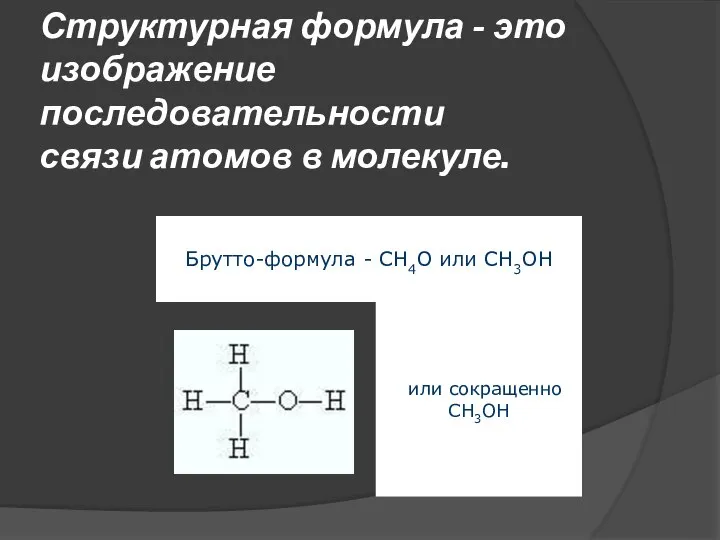
- 13. Структурная формула - это изображение последовательности связи атомов в молекуле.
- 14. 2. Свойства веществ определяются не только их качественным и количественным составом, но и порядком соединения атомов
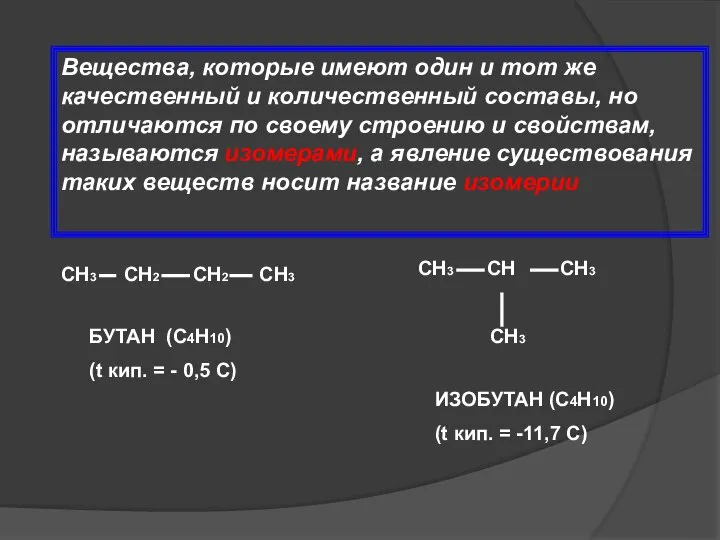
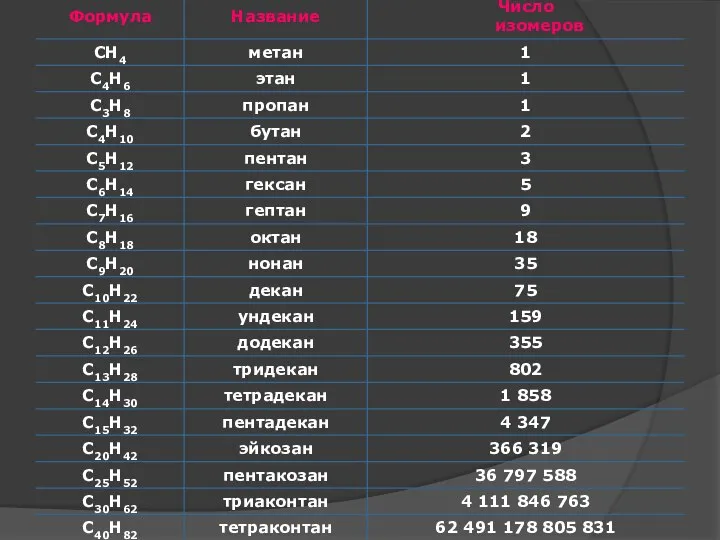
- 15. Вещества, которые имеют один и тот же качественный и количественный составы, но отличаются по своему строению
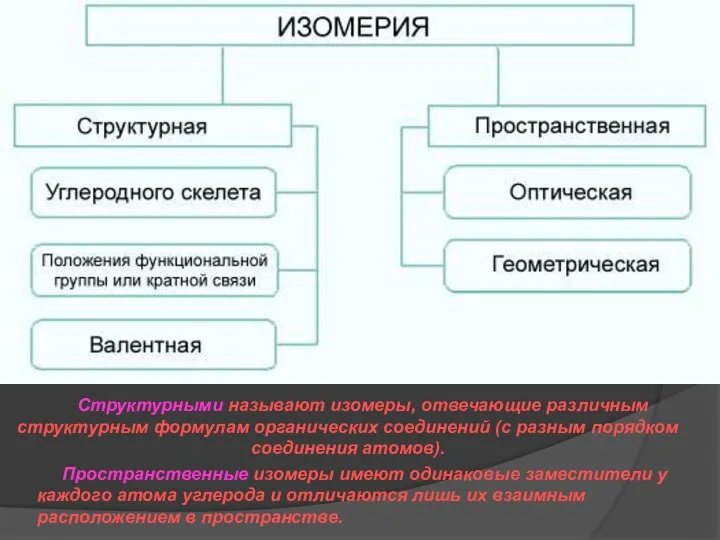
- 17. Структурными называют изомеры, отвечающие различным структурным формулам органических соединений (с разным порядком соединения атомов). Пространственные изомеры
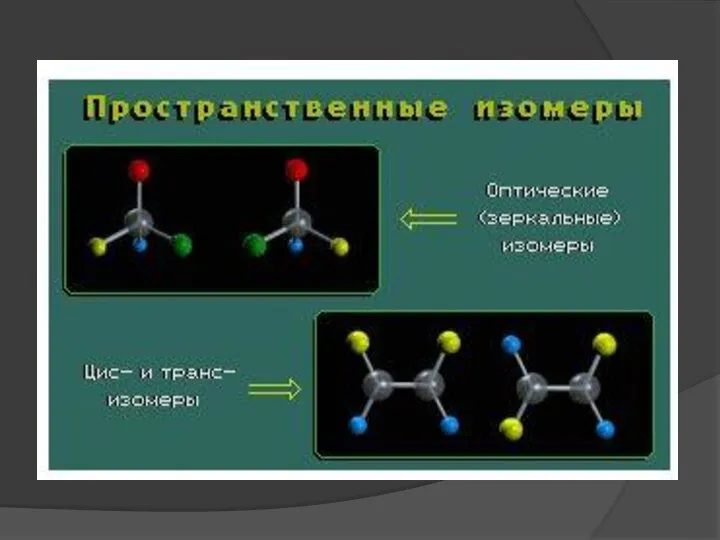
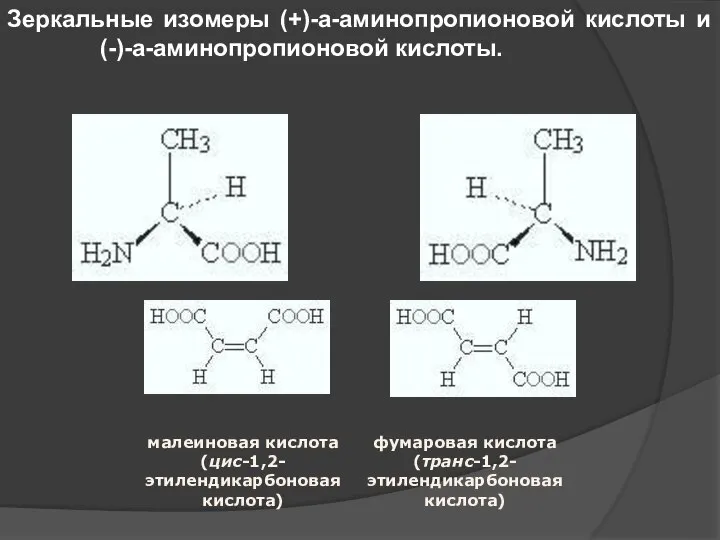
- 18. Пространственные изомеры (стереоизомеры). Стереоизомеры можно разделить на два типа: геометрические изомеры и оптические изомеры. Геометрическая изомерия
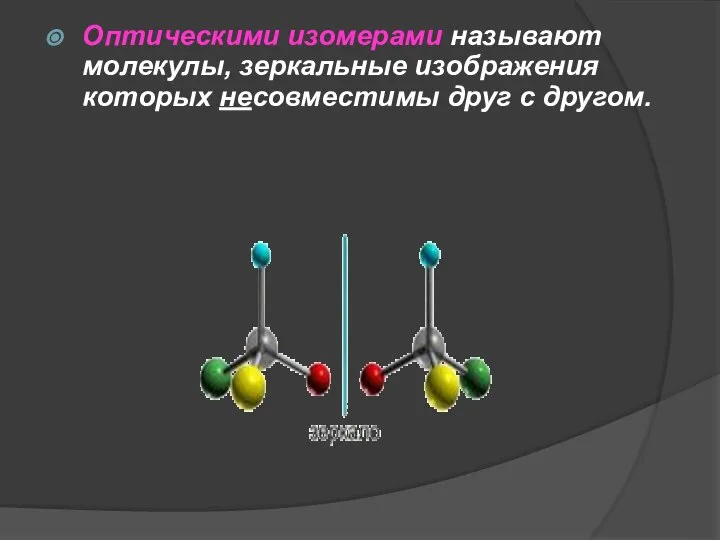
- 19. Оптическими изомерами называют молекулы, зеркальные изображения которых несовместимы друг с другом.
- 22. Зеркальные изомеры (+)-a-аминопропионовой кислоты и (-)-a-аминопропионовой кислоты.
- 23. Итак, изомерия – одно из наиболее своеобразных проявлений специфики и особенности органической химии.
- 24. 3. Свойства органических соединений зависят от взаимного влияния атомов и групп атомов в молекуле друг на
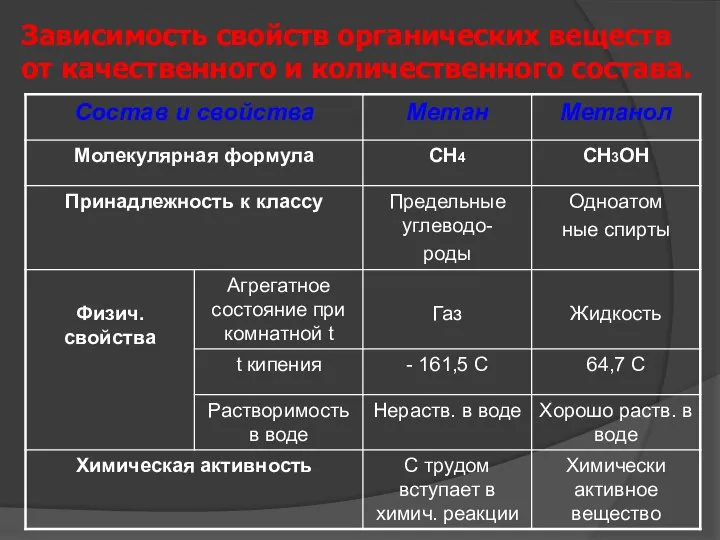
- 25. Зависимость свойств органических веществ от качественного и количественного состава.
- 27. Скачать презентацию














 Пиримидин. Пиримидиновые основания
Пиримидин. Пиримидиновые основания Метаболизм азота
Метаболизм азота Презентация на тему Игра по химии «Остров Периодическая Система»
Презентация на тему Игра по химии «Остров Периодическая Система»  Чистые вещества и смеси, их разделение
Чистые вещества и смеси, их разделение Полисахариды. Крахмал и целлюлоза
Полисахариды. Крахмал и целлюлоза Полезные кирпичи окружающего мира
Полезные кирпичи окружающего мира Значение периодического закона для современной науки и техники (связь химии с экономикой и экологией) Учитель химии МОУ лицея
Значение периодического закона для современной науки и техники (связь химии с экономикой и экологией) Учитель химии МОУ лицея  Коллоидные системы
Коллоидные системы Химические реакции. Реакции по фазовому составу
Химические реакции. Реакции по фазовому составу Характеристика азота как химического элемента и простого вещества
Характеристика азота как химического элемента и простого вещества Серная кислота и её соли. Качественная реакция на сульфат-ион
Серная кислота и её соли. Качественная реакция на сульфат-ион Химиялық қоспалар
Химиялық қоспалар Презентация на тему Ионные уравнения реакций (8 класс)
Презентация на тему Ионные уравнения реакций (8 класс)  Соли
Соли Презентация на тему Викторина по химии "Что это?"
Презентация на тему Викторина по химии "Что это?"  Структура неорганических ионных соединений. Лекция 12
Структура неорганических ионных соединений. Лекция 12 Неекономiчний фермент
Неекономiчний фермент Презентация на тему Лайнус Полинг
Презентация на тему Лайнус Полинг  Элемент протактиний
Элемент протактиний Ароматические кислородсодержащие соединения
Ароматические кислородсодержащие соединения Основания. Классификация
Основания. Классификация Строение атома
Строение атома Явление аллотропии
Явление аллотропии Теория гидродинамического подобия
Теория гидродинамического подобия Расчет энтропии образования и теплоемкости органических веществ методом Бенсона
Расчет энтропии образования и теплоемкости органических веществ методом Бенсона Нефть
Нефть Вуглеводні. Метан як представник насичених вуглеводнів
Вуглеводні. Метан як представник насичених вуглеводнів Hydroxidy. Vlastnosti
Hydroxidy. Vlastnosti